您的购物车当前为空
您的购物车当前为空

- 具有直观的搜索结果
- 更便捷高效地比较产品细节
- 快速、简洁的提交订单
- 成为我们TargetMol的一员,阅读和提交您的产品建议和意见
我们很想知道您的意见反馈,所以我们在每个页面上都梳理出一个反馈按钮。
- 首页
- 全部产品
- 抑制剂&激动剂
- 化合物库
- 天然产物
- 重组蛋白
- 热门应用领域
- AI+药物发现平台
- Topscience Database
- 市场资讯
- 会员中心

转录因子P53在细胞周期中发挥着核心作用,并且可以说是最重要的肿瘤抑制因子之一。在细胞受到DNA损伤或致癌压力等信号时,P53通过一系列磷酸化事件和其它后转录修饰(PTM)被激活,导致P53靶基因的表达,这些基因参与细胞周期停滞、DNA修复,或者如果无法修复,则会引发细胞凋亡。
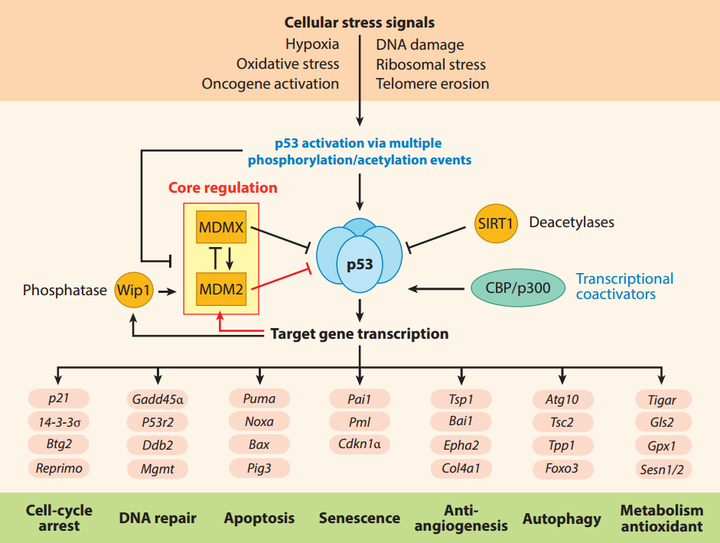 ▲p53通过多种磷酸化事件在细胞应激下被激活
▲p53通过多种磷酸化事件在细胞应激下被激活
P53研究历史
p53的研究历程可以追溯到1979年,当时p53蛋白被多个研究团队独立发现,这些研究团队在关于猴病毒40(SV40)的研究中发现了p53蛋白。最初人们认为p53是参与细胞转化的癌基因,但在1989年,一系列论文揭示了野生型(WT)p53实际上是一种肿瘤抑制基因。
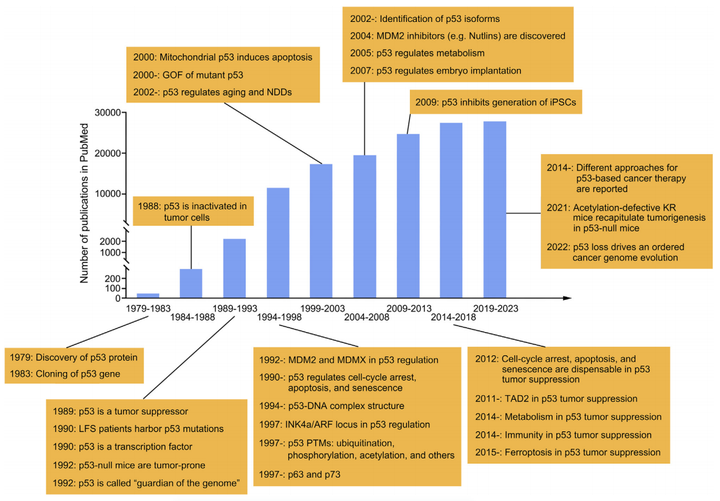 ▲P53研究历史
▲P53研究历史
人类P53基因家族包括三个成员:P53、P63、P73。P53蛋白主要作为转录因子(TF)发挥作用,人类中的全长p53蛋白(FLp53)包括393个氨基酸,分为五个不同的结构域:N-末端转录活化结构域(TAD)、富含脯氨酸结构域(PRD)、中央DNA结合结构域(DBD)、四聚体化结构域(TD)和C-末端调节结构域(CTD)。
在未受到压力的细胞中,p53蛋白呈现单体、二聚体和四聚体状态的混合,其中二聚体占主导地位。在各种类型的应激信号(包括DNA损伤、致癌基因激活、核糖体应激、端粒侵蚀、营养匮乏和缺氧)作用下,大多数p53蛋白通过其TD迅速组装成功能四聚体(二聚体的二聚体)。通过使用DBD,这种四聚体识别位于靶基因的启动子或增强子上的p53结合位点以调节转录。
此外,p53的转录活化结构域(TAD)和调节结构域(CTD)本质上是无序的,这有助于它们与转录介质的相互作用。这两个结构域也是主要经历翻译后修饰(PTMs)的区域。
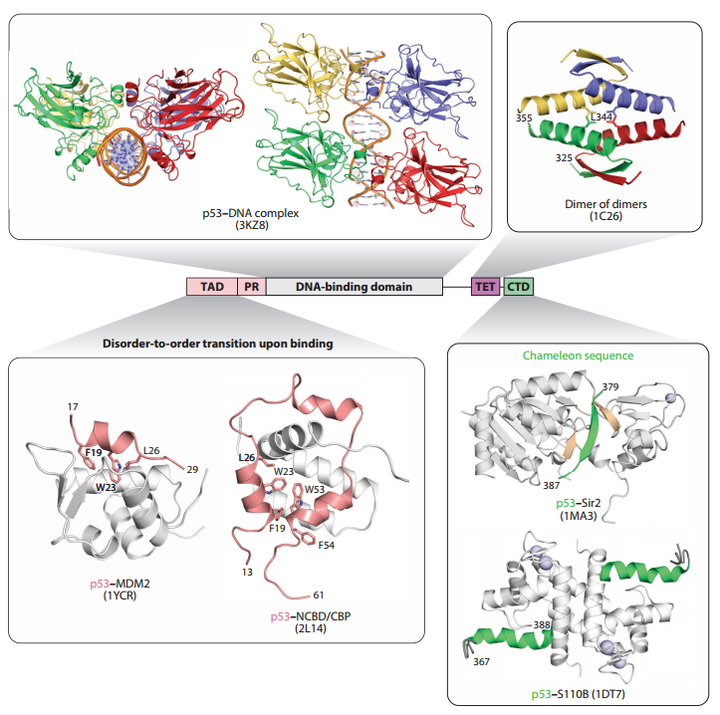 ▲P53结构
▲P53结构
P53的调控
p53的表达和活性受到DNA、RNA和蛋白质水平上多层次的调控。
在DNA水平上,p53基因可能发生SNP和突变。p53具有两个启动子,可以被甲基化并沉默。p53基因的转录受到各种转录因子(例如,HOXA5)的激活或抑制。
在RNA水平上,p53 mRNA的细胞定位、稳定性和翻译由RNA结合蛋白(如TIA1)和非编码RNA(如miR-380-5p)调节。p53前体mRNA和mRNA可以分别进行替代剪接和替代翻译。
在蛋白质水平上,p53的折叠、稳定性、细胞定位、DNA结合、转录激活能力和靶向选择主要由翻译后修饰(例如,泛素化、磷酸化和乙酰化)和辅因子(例如,MDM2、MDMX和CBP)介导。各种压力信号(如DNA损伤)可以激活p53,其作为转录因子的活性具有高度的动态性。p53在细胞质中还表现出TF独立功能(例如,通过与Bcl-XL相互作用促进凋亡)。
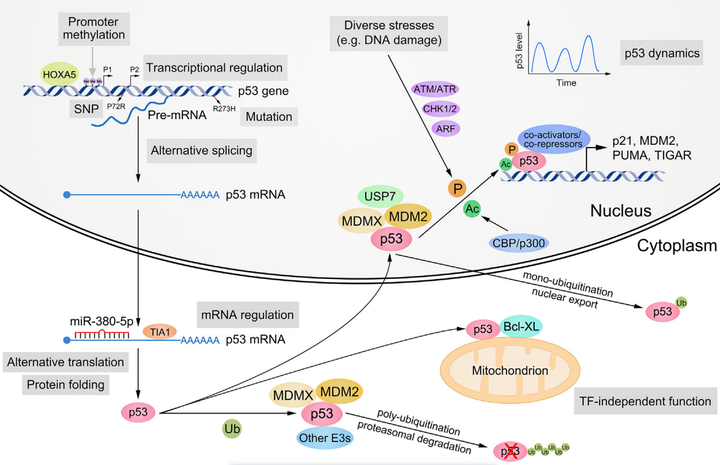 ▲P53的调控
▲P53的调控
P53的功能
p53表现出多样且复杂的功能——
经典功能:包括诱导细胞周期阻滞、凋亡和衰老,以及维持基因组稳定性等。
其他功能:如介导新陈代谢、铁死亡、干细胞动态、细胞竞争、转移和免疫等。
由于其广泛的功能,p53在许多生理过程(如生殖、发育、再生、修复和衰老)和病理疾病(如神经退行性疾病、辐射中毒、化疗毒性、缺血损伤、代谢性疾病和癌症)中起着关键作用。
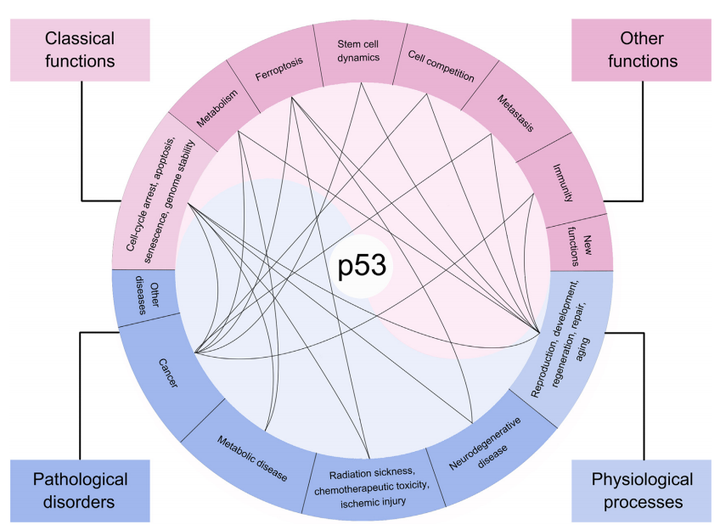 ▲P53的功能以及其在病理中的作用
▲P53的功能以及其在病理中的作用
举个例子:细胞周期阻滞、细胞凋亡、衰老和基因组稳定性
p53的细胞周期阻滞、凋亡和衰老诱导是最早发现的功能之一。各种压力信号都可以诱导p53发挥这些功能,其中DNA损伤是最强的”触发器“。
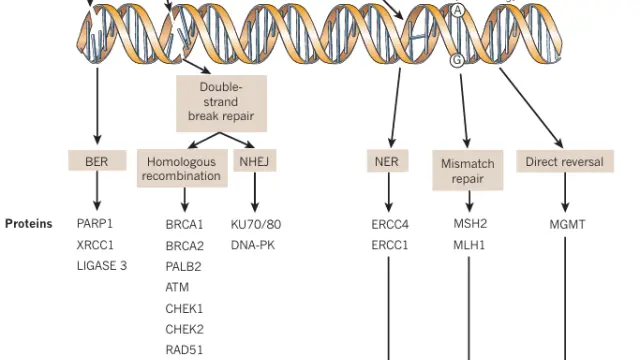
在DNA损伤时,p53被稳定并激活以阻止细胞周期,为细胞提供了一个时间窗口和足够的物质和能量,以修复受损的DNA。如果损伤过于严重无法修复,p53将通过诱导凋亡和衰老来消除受损细胞。值得注意的是,p53激活的结果也取决于细胞类型和DNA损伤类型。这三种活动被广泛接受为防止肿瘤发生的主要障碍。另一方面,未能消除受损细胞会导致基因组不稳定性。p53的丧失,包括等位基因丧失(LOH)和双等位基因失活或缺失,促进了基因组不稳定性,并推动了肿瘤细胞基因组的演化。
然而,目前尚不清楚p53介导的这些与DNA修复相关的靶点的激活是否足以独立于其他p53活动来抑制肿瘤发生。
再举个例子:代谢和铁死亡
p53在调节葡萄糖、脂质、氨基酸、核苷酸、铁以及氧化还原过程等多种代谢方面起着主导作用。它还调节自噬,并与AMPK、AKT和mTOR等主要代谢调节因子有广泛的交互作用。这使得p53与几种代谢性疾病,尤其是癌症有关。
一般来说,p53抑制合成代谢过程(例如新生脂肪生成和核苷酸合成),同时促进分解代谢过程(包括氧化磷酸化、脂解和脂肪酸氧化)。增强的糖酵解在癌细胞中产生多种分子物质用于生物合成,因此也被p53抑制。这些p53的活动抵消了癌细胞快速增殖的需求,从而导致肿瘤抑制。
铁死亡是一种铁依赖性的调控性细胞死亡形式,在脂质过氧化物过量的情况下发生,与代谢途径密切相关。P53的一些代谢靶点直接参与调节铁死亡,如SLC7A11、VKORC1L1、GLS2和PLTP。P53介导的铁死亡也被认为是肿瘤抑制的重要武器。
靶向P53治疗癌症
目前已经开发出了多种方法来针对p53进行癌症治疗。在保留WT p53的肿瘤中,RG7388、APG-115和ALRN-6924被用来干扰p53与MDM2或MDMX之间的蛋白相互作用,而RITA、tenovin-6、ML364和UNC0379则针对p53的其他负调控因子。
在含有p53错义突变的肿瘤中,APR-246、COTI-2 和PAT等能够恢复许多p53突变体的WT构象。特定的药物如PhiKan083、PK7088和MS78则针对p53 Y220C突变,而ZMC1用于p53 R175H突变。
此外,基因组编辑可能有助于纠正p53基因突变。NSC59984、ganetespib、MCB-613和纳米受体能够降解突变p53。像ReACp53和ADH-6这样的药物则能解决突变p53的聚集,部分恢复WT p53功能。识别突变p53衍生的新抗原的抗体如P1C1TM和H2-scDb,通过免疫细胞介导肿瘤细胞消除。p53MVA和p53-SLP则是免疫治疗中使用的p53疫苗。突变p53新抗原也可用于开发细胞免疫治疗。突变p53 DNA片段和蛋白(包括其聚集体)可用于肿瘤诊断和预后。
在存在 p53 无义突变的肿瘤中,G418、2,6-DAP、CC-90009和NMDI14,可以诱导 p53 突变型 mRNA 的诱导翻译通读(readthrough),或抑制 NMD。在p53-null肿瘤中,提供p53蛋白、mRNA和DNA可以恢复p53表达并消灭肿瘤细胞。
总之,P53 蛋白是一种转录因子和肿瘤抑制蛋白,可结合 DNA 并调控多种转录靶标,响应细胞应激或 DNA 损伤,协调细胞周期阻滞、DNA 修复、代谢改变、凋亡等过程,防止肿瘤形成。陶术可提供多种激动剂、抑制剂助力P53相关研究,欢迎私信咨询~

参考文献:
Liu et al., Understanding the complexity of p53 in a new era of tumor suppression, Cancer Cell (2024).
Lane, D. P. (1992). Cancer. p53, guardian of the genome. Nature, 358(6381), 15-16.
Levine, A. J., & Oren, M. (2009). The first 30 years of p53: growing ever more complex. Nature Reviews Cancer, 9(10), 749-758.
Vousden, K. H., & Prives, C. (2009). Blinded by the Light: The Growing Complexity of p53. Cell, 137(3), 413-431.
Joerger, A. C., & Fersht, A. R. (2016). The p53 pathway: origins, inactivation in cancer, and emerging therapeutic approaches. Annual Review of Biochemistry, 85, 375-404.
Muller, P. A., & Vousden, K. H. (2013). p53 mutations in cancer. Nature Cell Biology, 15(1), 2-8.
Vogelstein, B., Lane, D., & Levine, A. J. (2000). Surfing the p53 network. Nature, 408(6810), 307-310.

 嗨!有任何问题?点我咨询
嗨!有任何问题?点我咨询

版权所有©2015-2026 TargetMol Chemicals Inc.保留所有权利.
沪ICP备20019793号-4 | 沪公网安备 31010602006700号 | 沪(静)应急管危经许[2024]203441
| 沪(静)应急管危经许[2024]203441