 您的购物车当前为空
您的购物车当前为空
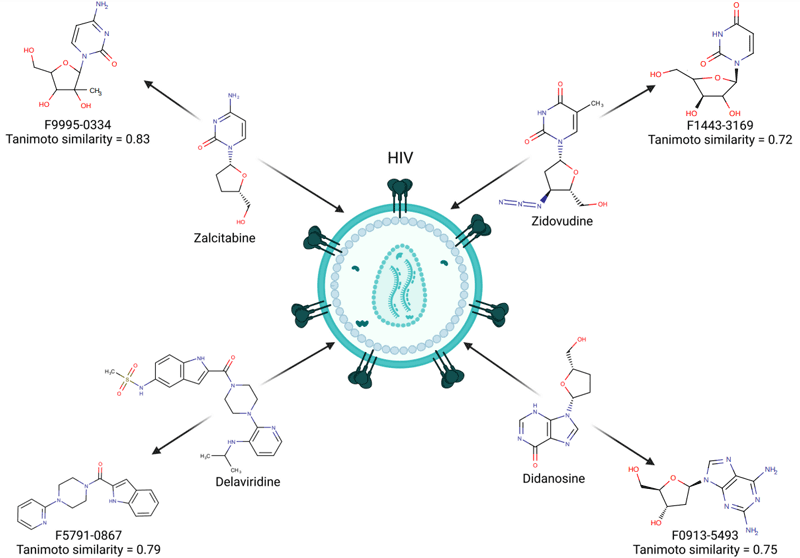
背景
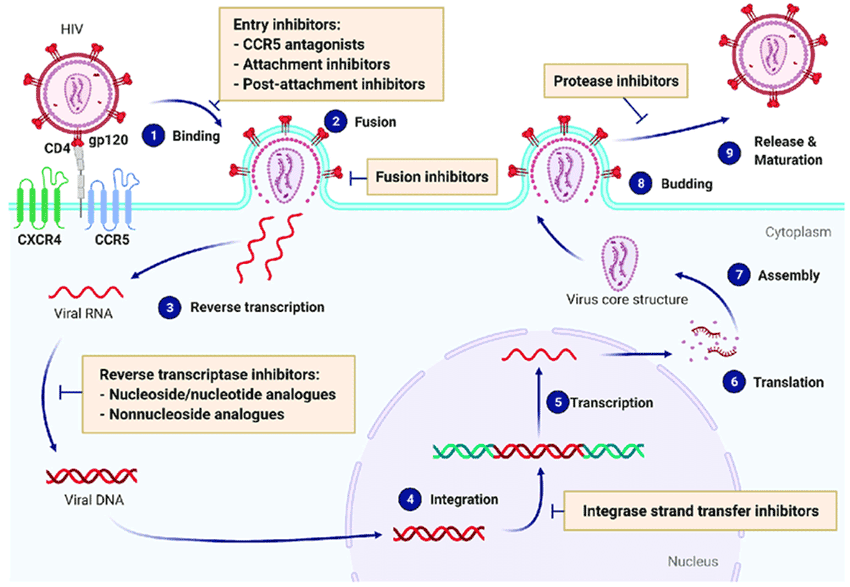
多年来,多药联合治疗策略已变得高度有效且易于实施,成功提升了HIV阳性患者的生活质量。目前约有50种获批的HIV药物可作为个性化治疗方案中的组分。根据病毒作用靶点及活性成分的不同,这些药物可分为七大主要类别。各类药物通过作用于HIV生命周期的不同阶段发挥作用:有的阻止病毒进入免疫系统细胞;有的则能阻断HIV复制所需的酶——逆转录酶、蛋白酶和整合酶。
这种丰富的治疗选择源于三十余年来持续深入的研究工作。然而,将HIV作为慢性病进行控制仅是迈向完全治愈的一步。实现根治仍是医学领域最重大的挑战之一,这也推动着人们不断探索新型抗HIV药物及治疗策略。
抗HIV聚焦库
该筛选库采用二维指纹相似性方法设计,包含超过19,600种具有潜在抗逆转录病毒活性的类药筛选化合物。
参考化合物集选自ChEMBL和BindingDB数据库。经过严格筛选的分子构成了针对HIV相关蛋白、细胞系或完整病毒(图2)的靶向特异性HIV抑制剂研究的基础。这些化合物从内部数据库中选出,采用MDL公共键指纹的75%相似度截断值(Tanimoto)。
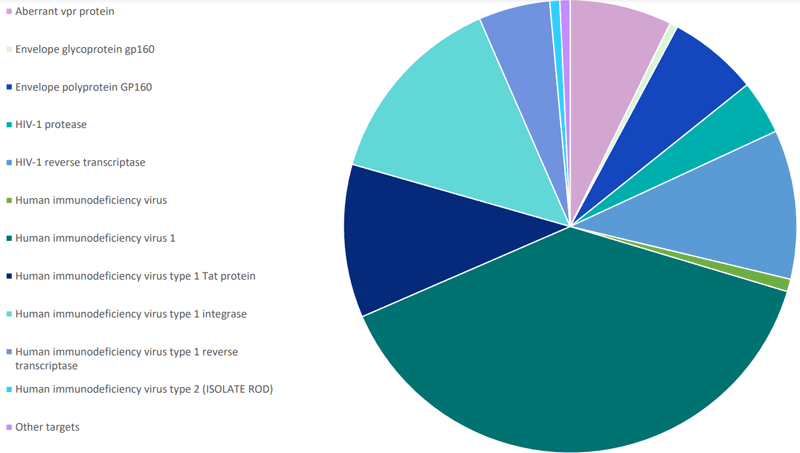
抗HIV靶向化合物库
本筛选套装包含约3,900种结构多样的筛选分子,这些分子对以下与HIV相关的药物靶点可能具有潜在活性:
• 黏膜相关淋巴组织淋巴瘤易位蛋白1(MALT1)
• 原癌基因酪氨酸蛋白激酶Src(SRC)
• HIV-1蛋白酶
• HIV-1逆转录酶
• HIV-1整合酶
这些类药化合物是通过基于药效团假说的高通量虚拟筛选方法筛选出来的。关于针对特定抗逆转录病毒蛋白靶点的各化合物子集的更详细描述,请参见下文。
已知该病毒可在中枢神经系统中潜伏并繁殖,从而导致神经系统疾病。这可能是由于抗HIV药物无法穿过血脑屏障并在大脑中抑制HIV,而这对逆转或改善HIV相关的神经认知障碍至关重要。因此,本抗HIV靶向化合物库中的化合物根据其吸附和穿透血脑屏障的能力进行了筛选,同时也考虑了代谢参数,即它们从体内排出的能力。
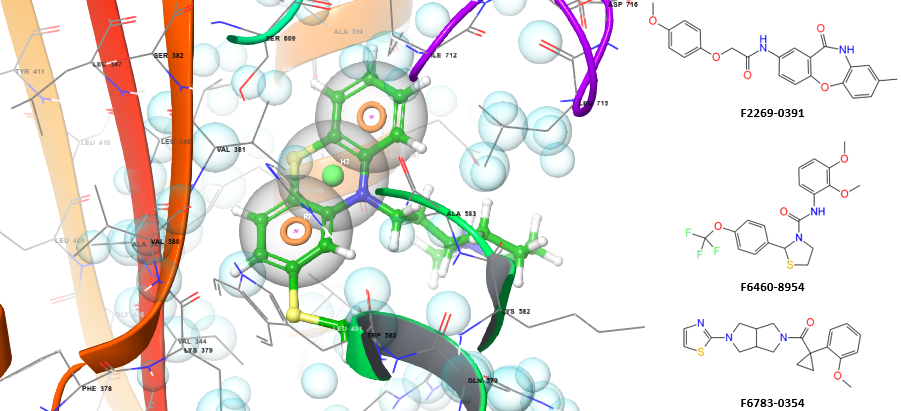
黏膜相关淋巴组织淋巴瘤易位蛋白1(MALT1)
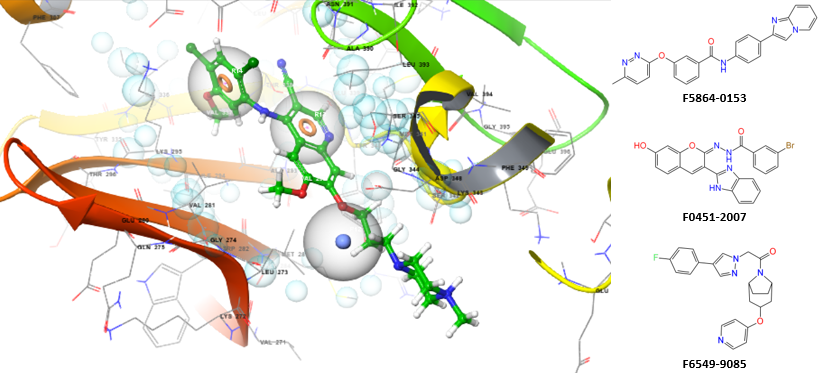
黏膜相关淋巴组织淋巴瘤易位蛋白1(MALT1)是一种蛋白酶,能够增强BCL10诱导的激活作用,从而激活NF-κB和p38 MAP激酶,进而促进编码促炎细胞因子和趋化因子基因的表达。该蛋白酶还参与辅助性T细胞17(Th17)分化的诱导过程,并在T细胞受体(TCR)介导的激活后介导T细胞中N4BP1的切割,导致N4BP1失活。由于N4BP1能够抑制人类免疫缺陷病毒1型(HIV-1)的复制,因此MALT1介导的N4BP1失活有助于潜伏的HIV-1前病毒的再激活。因此,MALT1是靶向HIV治疗中的一个重要靶点。
关键特征:
• 方法:高通量虚拟筛选
• 使用的X射线数据:4MXO
• 应用的筛选条件:代谢、QPPCaco、QPlogBB、QPPMDCK、人体口服吸收百分比(PercentHuman-OralAbsorption)
• 筛选出的化合物数量:821个
原癌基因酪氨酸蛋白激酶Src(SRC)
原癌基因酪氨酸蛋白激酶Src是一种非受体型酪氨酸激酶。它是多种调控细胞内不同过程的信号通路中的组成部分,尤其涉及基因转录、免疫应答、细胞黏附、细胞周期进程、凋亡、迁移及转化等过程。研究还发现,原癌基因酪氨酸蛋白激酶Src在HIV感染发展过程中可能也发挥一定作用。已知在与人类CD4细胞接触后,HIV会诱导细胞内蛋白酪氨酸激酶2β(PTK2B)的自磷酸化。PTK2B在Tyr402位点的自磷酸化是在c-SRC的参与下发生的,这会导致CD4细胞的焦点黏附和细胞骨架重塑。因此,抑制原癌基因酪氨酸蛋白激酶Src的活性或表达可以减少HIV感染,使该蛋白成为治疗HIV的一个有前景的靶点。
主要特点:
• 方法:高通量虚拟筛选
• 使用的X射线数据:4I1R
• 应用的筛选条件:代谢特性、QPPCaco、QPlogBB、QPPMDCK、人体口服吸收百分比
• 筛选出的化合物数量:780种
HIV-1蛋白酶
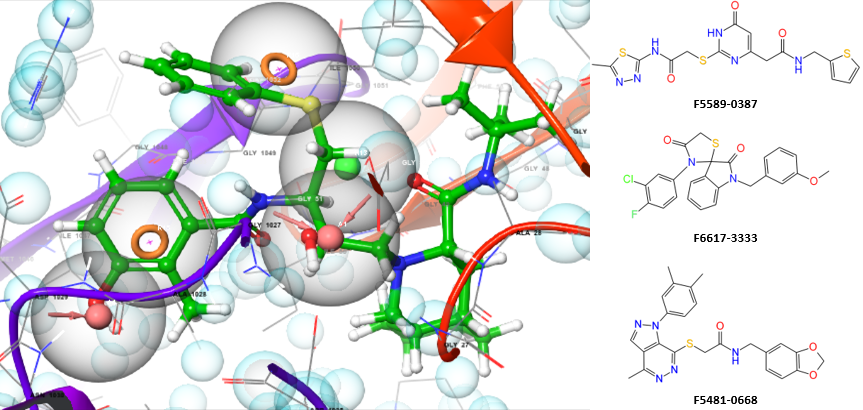
HIV蛋白酶是一种参与逆转录病毒肽键水解的酶。它在HIV生命周期中起着至关重要的作用,能够将蛋白质分解为更小的单元,并利用这些单元构建具有感染性的HIV病毒颗粒的成熟蛋白组分。抑制HIV蛋白酶会破坏该逆转录病毒的复制和感染其他细胞的能力。
成熟的HIV蛋白酶是一个22 kDa的同源二聚体,每个亚基由99个氨基酸组成。其活性位点位于两个相同的亚基之间,包含催化三联体(Asp25、Thr26和Gly27)的序列。HIV蛋白酶主要执行两个关键功能:HIV前蛋白酶负责自我加工,而成熟的蛋白酶能够在Gag-Pol多聚蛋白上的九个特定位点水解肽键,将这些产生的亚基转化为成熟且功能完整的蛋白质。HIV蛋白酶主要通过两种方式发生突变:在活性位点以及蛋白外围区域,从而影响与抑制剂的结合。鉴于这一事实,在制药行业中寻找针对HIV蛋白酶的新型有效药物具有重要意义。
关键特征:
• 方法:高通量虚拟筛选
• 使用的X射线数据:7DOZ
• 应用的筛选条件:代谢、QPPCaco、QPlogBB、QPPMDCK、人体口服吸收百分比
• 筛选出的化合物数量:517种
HIV-1逆转录酶
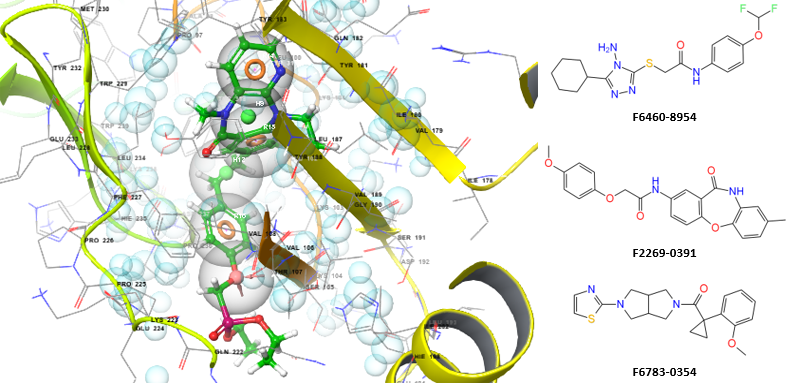
HIV逆转录酶(HIV RT)是逆转录病毒用于自我复制的关键酶之一。该酶催化将单链病毒RNA转化为前病毒DNA,进而整合并感染宿主细胞DNA。抑制该酶的活性可有效阻碍病毒复制。相应的靶向药物(核苷类与非核苷类逆转录酶抑制剂)通过阻断其功能或改变其结构,从而将逆转录酶排除在感染过程之外。
HIV逆转录酶由51 kDa和66 kDa两个亚基组成。该酶具有三种连续的生化活性:依赖RNA的DNA聚合酶活性、核糖核酸酶H(RNase H)活性以及依赖DNA的DNA聚合酶活性。这些活性协同作用,使该酶能够将单链RNA转化为双链互补DNA。目前,HIV逆转录酶是艾滋病治疗中最重要的靶点之一。然而,HIV-1 RT结构的突变可能导致耐药性病毒株的出现,这使得新药的研发与临床试验显得尤为迫切。
关键特征:
• 方法:高通量虚拟筛选
• 使用的X射线数据:4I7F
• 应用的筛选条件:代谢特性、QPPCaco、QPlogBB、QPPMDCK、人体口服吸收百分比
• 筛选出的化合物数量:538个
HIV整合酶
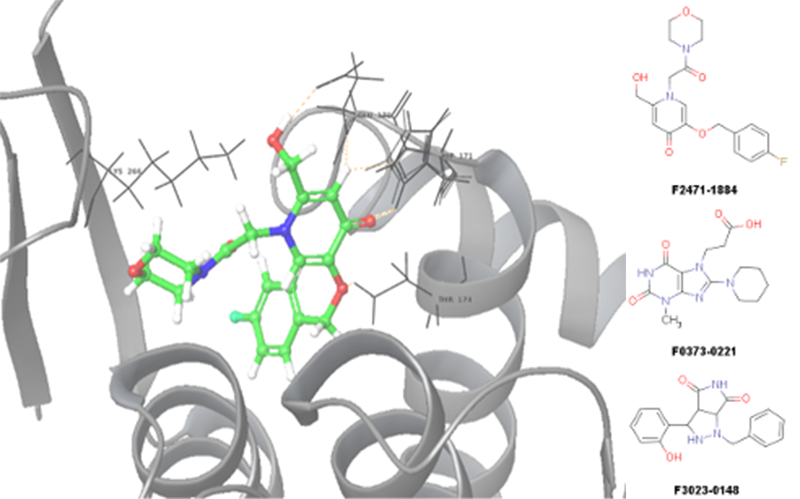
HIV整合酶是人类免疫缺陷病毒(HIV)生命周期中的一种关键酶。该酶促进病毒DNA与宿主细胞基因组的整合,这是病毒复制和持续感染的重要步骤。从结构上看,HIV整合酶属于整合酶家族,其特点是能够结合并加工DNA。该酶主要通过三个步骤发挥作用:1)3'端加工,即切割病毒DNA末端;2)链转移,即将病毒DNA连接到宿主DNA上;3)缺口修复,完成整合过程。HIV整合酶由三个结构域组成:N端锌指结构域、催化核心结构域和C端DNA结合结构域。每个结构域在整合过程中都发挥特定作用,使得整合酶成为抗逆转录病毒治疗的主要靶点。
针对HIV整合酶的靶向治疗至关重要,因为该酶在HIV复制中不可或缺。抑制HIV整合酶可以有效阻止病毒整合到宿主基因组中,从而防止有效感染的发生。
为了设计此类筛选,我们使用了HIV整合酶I的晶体结构数据(PDB编号:8buv)以及Al-Mawsawi等人描述的结合位点。该蛋白通过Schrödinger软件进行了准备和优化。采用Glide对接(Schrödinger)方案对高通量化合物库进行对接和筛选,最终筛选出_种化合物作为潜在的治疗药物。
关键特征:
• 方法:高通量虚拟筛选
• 使用的X射线数据:8BUV
• 筛选出的化合物数量:1310种





 很棒
很棒

 |
|