您的购物车当前为空
您的购物车当前为空

- 具有直观的搜索结果
- 更便捷高效地比较产品细节
- 快速、简洁的提交订单
- 成为我们TargetMol的一员,阅读和提交您的产品建议和意见
我们很想知道您的意见反馈,所以我们在每个页面上都梳理出一个反馈按钮。
- 首页
- 全部产品
- 抑制剂&激动剂
- 化合物库
- 天然产物
- 重组蛋白
- 热门应用领域
- AI+药物发现平台
- Topscience Database
- 市场资讯
- 会员中心

众所周知,肿瘤有多种分类方法,除了良性、恶性之外,还有转移性肿瘤、原位肿瘤,以及科学研究中的”冷肿瘤“、”热肿瘤“之分。但这里的冷热可不是指温度,而是肿瘤里面包含免疫细胞的多少。
冷肿瘤 通常指的是在肿瘤微环境中 缺乏充足的免疫细胞浸润 的肿瘤。这些肿瘤通常不太容易受到免疫治疗的影响,因为它们缺乏与免疫系统的有效互动。
与之相反,热肿瘤 是指肿瘤微环境中 存在大量免疫细胞浸润和活跃 的肿瘤。这些肿瘤通常对免疫治疗更为敏感,它们能够激发免疫系统对肿瘤细胞的攻击。
因此,使”冷肿瘤“转化为”热肿瘤“也是目前肿瘤治疗领域的热点之一。那么,如何让冷肿瘤能顺利转化变身呢?
在 Science Immunology 期刊的一篇新论文中,德克萨斯大学西南医学中心 JINMING GAO 教授团队在线发表了一种新型方法,通过将 cGAMP 嵌入到 PC7A 纳米粒子中形成聚合 STING 激活纳米颗粒(PolySTING),创造了一种“ shock-and-lock ”的双重 STING 激活机制,结合了 cGAMP 引发的爆发性 STING 激活和 PSC7A 引发的非经典、持续活性,可有效消除肿瘤。这种方法同样适用于”冷肿瘤“类型。
▲点击图片可跳转原文
小贴士
cGAS-STING 信号通路是细胞内的一套预警系统,当病毒或癌细胞染色体的 DNA 进入细胞质中时, cGAS(cyclic GMP-AMP synthase)能直接识别病原体来源的DNA,将ATP和GTP催化合成为cGAMP,cGAMP能够结合并活化STING蛋白,从而激活下游免疫信号通路,介导I型干扰素的产生,引发免疫应答。
最新研究中,研究人员开发的 PolySTING 纳米粒子具有较小的直径(25 ± 3 nm)和球形形态。在 THP1-Lucia ISG 细胞中表现出强大的 IFN-β 表达(>250倍生理盐水对照组),与 cGAMP 或 PSC7A NP(另一种cGAMP载体)相比具有更持久的 STING 激活效果。
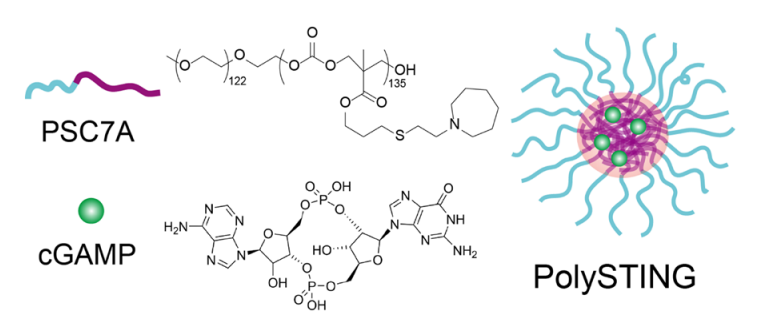
▲PolySTING合成示意图
PolySTING是对冷、热肿瘤均有效的STING激动剂
实验中,研究者利用青霉素 5(Cy5)标记的 PolySTING 来量化 MC38 结肠癌肿瘤内注射后的纳米粒子生物分布。根据分析,PolySTING 在肿瘤和肿瘤引流淋巴结(tDLNs)中积聚丰富,免疫细胞对纳米粒子的摄取明显高于癌细胞。
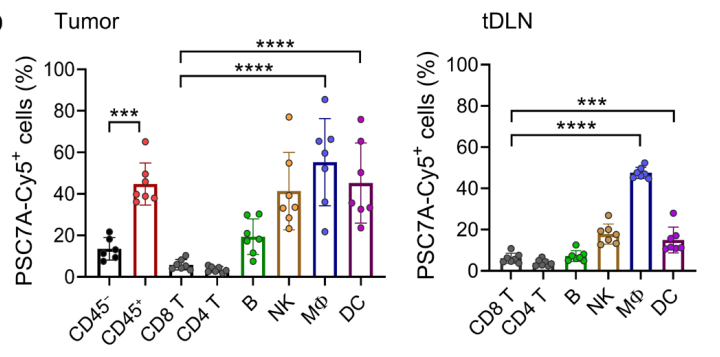
▲在对Cy5标记的PolySTING进行肿瘤内注射后,在MC38肿瘤和肿瘤引流淋巴结(tDLNs)中,Cy5阳性细胞在细胞群体中的百分比
此外,PolySTING 治疗不仅在原发性肿瘤上抑制了生长,还在肺部生成了系统免疫,对转移性 4T1 病灶的形成也有抑制作用。PolySTING 治疗比 PD-1 阻断剂对减少转移更有效。在 MC38 和 B16F10 远端肿瘤模型中,PolySTING 在注射在原发性肿瘤后抑制了远端肿瘤的生长。与 PD-1 的联合治疗产生了治疗协同作用。治愈的小鼠显示出长期的 T 细胞记忆。
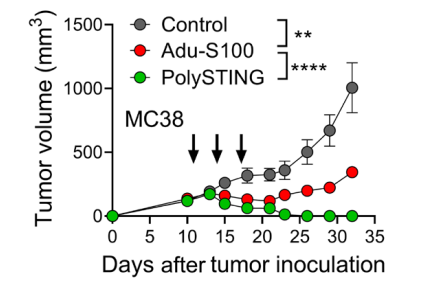
▲PolySTING治疗导致肿瘤完全消失
数据分析表明,PolySTING 治疗产生了强效的系统免疫,诱导了长期免疫记忆,有着广泛的抗肿瘤效应。
全新作用途径
除了确定 PolySTING 的抗肿瘤效应外,研究者还在小鼠实验中发现,PolySTING 介导效应至关重要的免疫细胞亚群——1型常规树突状细胞 (cDC1s)。
PolySTING 注射后,在 MC38-OVA 肿瘤中可 诱导较强的 cDC1 活化水平和细胞毒性 T 细胞反应。
与 Adu-S100(另一种STING激动剂)相比,PolySTING 组中 MC38-OVA 肿瘤中的 cDC1 数量增加了 2.4 倍,与葡萄糖对照组增加了 7.1 倍。cDC1 中的抗原呈递能力显著增强,包括 CD8α+和CD103+ cDC1 的抗原呈递能力提高。此外,PolySTING 处理还提高了 cDC1 的共刺激因子(如CD86)的表达水平,相较 Adu-S100 组超过 15 倍。
并且,PolySTING 激活的 DC 还导致肿瘤微环境和 tDLNs 中 OVA 特异性 CD8+ T 细胞的产生显著增加。
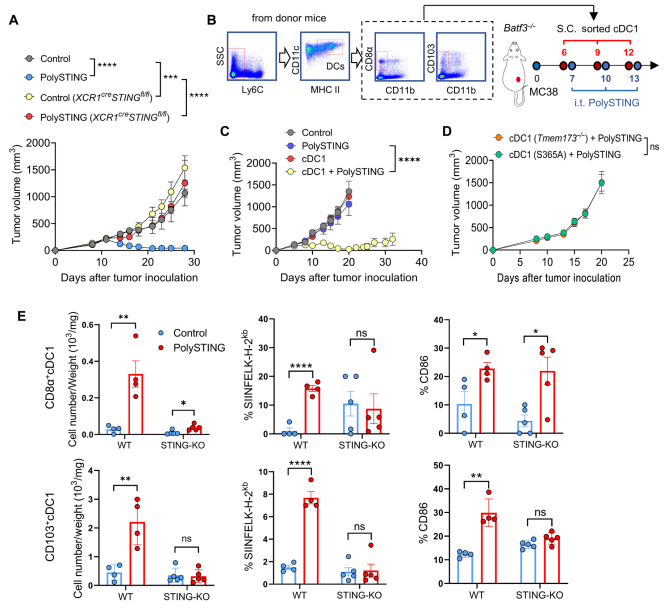
![]() ▲cDC1驱动STING介导的肿瘤排斥反应
▲cDC1驱动STING介导的肿瘤排斥反应
总的来说,PolySTING 特异性靶向 cDC1 并依赖 cDC1 中 STING-I-IFN 激活产生抗肿瘤免疫效果,其机制涉及对 cDC1 的选择性激活、STING-I-IFN 的激活、促进 DC 细胞的活化和抗原呈递,增强 CD8+ T 细胞的活性,引发肿瘤特异性免疫反应,从而实现抗肿瘤效果,且其效用相较于已知的 STING 激动剂(如Adu-S100)更好。
研究还进一步通过接受临床化疗的患者发现了 cDC1 中 STING 激活的免疫标志物组合——XCR1+STING+CXCL9+,可能作为癌症患者对治疗反应的预后临床生物标志物。
小结
综上,该研究开发了一种具有“ shock-and-lock ”双重激活机制的聚合物STING激动剂(PolySTING),并系统性地探讨了PolySTING在肿瘤清除中的贡献,强调了1型常规树突状细胞 (cDC1s)对于STING介导的肿瘤至关重要,为STING介导的癌症免疫治疗提供了一种有希望的方法
TargetMol® 可为您提供 STING蛋白、cGAMP、2',3'-cGAMP、STING agonist-4 等产品助力相关研究。欢迎点击下方产品跳转产品页查看,如感兴趣或有疑问可私聊 T 仔咨询噢~




参考资料:
[1]Jian Wang et al. ,STING licensing of type I dendritic cells potentiates antitumor immunity.Sci. Immunol.9,eadj3945(2024).DOI:10.1126/sciimmunol.adj3945
[2] Zhao B, Du F, Xu P, Shu C, Sankaran B, Bell SL, Liu M, Lei Y, Gao X, Fu X, Zhu F, Liu Y, Laganowsky A, Zheng X, Ji JY, West AP, Watson RO, Li P. A conserved PLPLRT/SD motif of STING mediates the recruitment and activation of TBK1. Nature. 2019 May;569(7758):718-722. doi: 10.1038/s41586-019-1228-x. Epub 2019 May 22. PMID: 31118511; PMCID: PMC6596994.
[3]Imler Jean-Luc, Cai Hua, Meignin Carine and Martins Nelson 2024Evolutionary immunology to explore original antiviral strategiesPhil. Trans. R. Soc. B3792023006820230068.

 嗨!有任何问题?点我咨询
嗨!有任何问题?点我咨询

版权所有©2015-2026 TargetMol Chemicals Inc.保留所有权利.
沪ICP备20019793号-4 | 沪公网安备 31010602006700号 | 沪(静)应急管危经许[2024]203441
| 沪(静)应急管危经许[2024]203441