 您的购物车当前为空
您的购物车当前为空
TargetMol疾病造模——Lipopolysaccharides(Cat. No. T11855),让免疫细胞全线进入战备
1. 产品介绍
Lipopolysaccharides,货号T11855,别名脂多糖、LPS。Lipopolysaccharides(LPS)来源于大肠杆菌O55:B5,是革兰氏阴性菌外膜的重要成分,由脂质A、核心寡糖和O-特异性多糖组成,具有高免疫原性,能激活免疫细胞TLR4受体,诱导细胞迁移体分泌,常用于炎症模型的构建,如关节炎、慢性阻塞性肺病(COPD)、急性呼吸窘迫综合征(ARDS)、以及消化系统等疾病模型的构建。
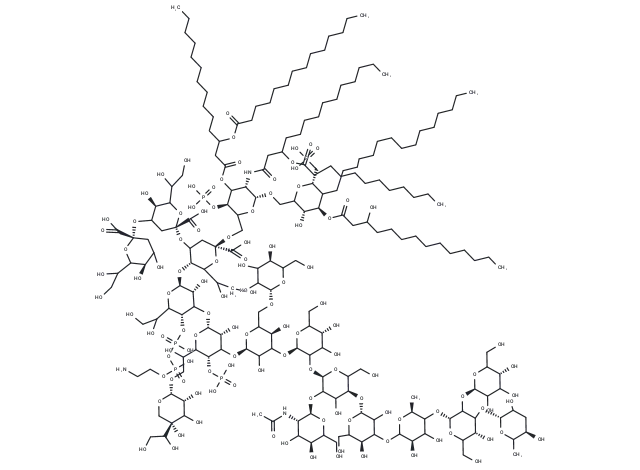
Lipopolysaccharides分子结构式
2. 背景介绍
脂多糖(Lipopolysaccharide, LPS)是革兰氏阴性菌外膜的重要组成成分,广泛存在于如大肠杆菌O55:B5等细菌中,由脂质A、核心寡糖及O-特异性多糖组成,其中脂质A是其主要的免疫活性结构基础。LPS具有高度保守的分子模式,能够作为典型的病原相关分子模式(PAMP),被宿主先天免疫系统识别并迅速诱导炎症反应。在免疫识别过程中,LPS首先由血清中的LPS结合蛋白(LPS binding protein, LBP)提取并转运至CD14,再递交至TLR4/MD-2受体复合物,从而触发下游信号级联反应。TLR4作为关键模式识别受体(PRR),是介导LPS诱导炎症反应的核心靶点,其激活可驱动多种感染及炎症相关疾病模型的建立,包括关节炎、COPD及ARDS等[1]。
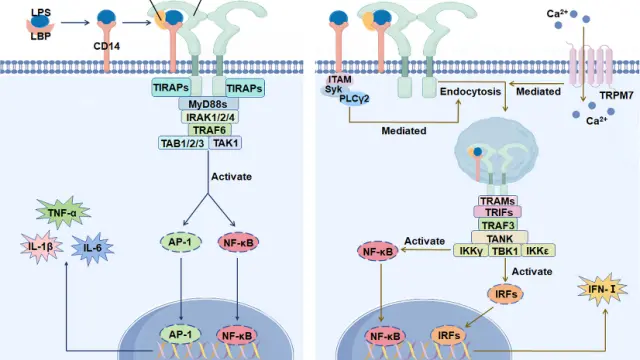
LPS介导的免疫激活主要依赖TLR4信号转导通路的逐级放大过程。在细胞外,LPS经LBP转运后结合CD14,并被递送至TLR4–MD-2复合物,诱导受体二聚化并启动胞内信号转导。随后TLR4通过MyD88依赖性与非依赖性两条经典通路激活下游信号网络:MyD88依赖通路主要激活IRAKs与TRAF6,进一步启动NF-κB与AP-1转录因子,从而诱导TNF-α、IL-6等促炎因子表达;而TRIF依赖通路则激活IRF3并促进I型干扰素产生。该双通路协同作用导致巨噬细胞M1极化及强烈炎症级联反应,是LPS诱导急性炎症损伤及多种炎症疾病(如ARDS、败血症)的关键机制基础[2]。
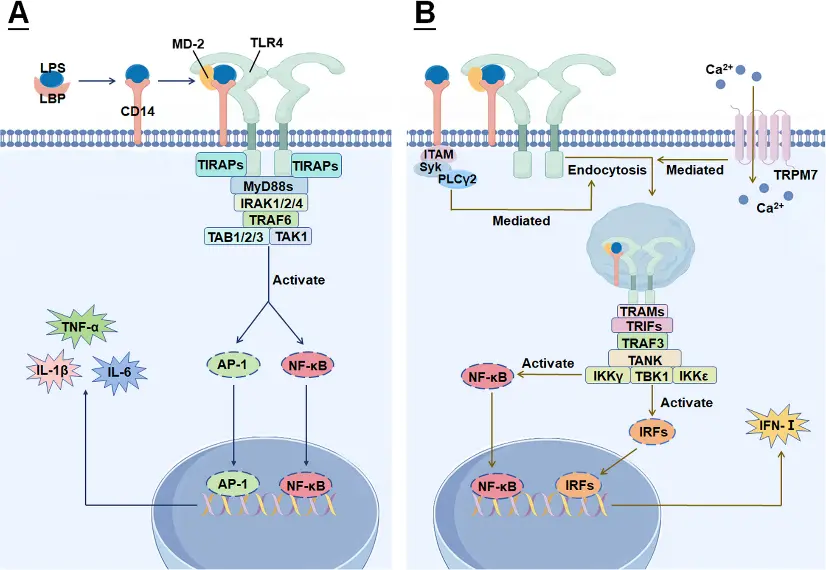
LPS-TLR4介导信号转导通路[2]
3. 应用文献精选
文章标题:Hyperglycemia enhances brain susceptibility to lipopolysaccharide-induced neuroinflammation via astrocyte reprogramming

研究概览:
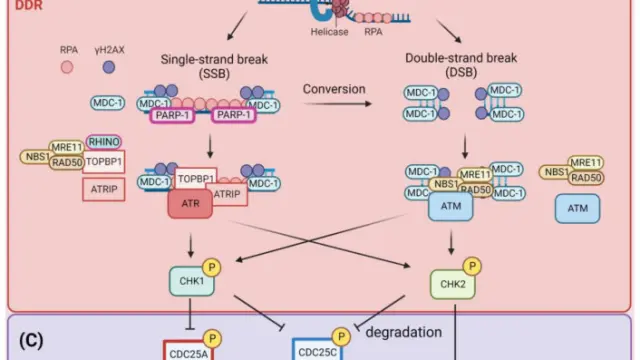
该研究通过体内外实验系统探讨了高血糖状态如何放大Lipopolysaccharide诱导的中枢神经炎症反应。作者在大鼠模型中联合高血糖处理与Lipopolysaccharide刺激,发现高糖环境显著增强了脑组织对炎症刺激的敏感性,表现为更强的炎症因子释放、胶质细胞活化以及神经组织损伤。机制上,研究重点揭示了星形胶质细胞在高糖条件下发生代谢与表型“重编程”,由稳态支持型细胞转变为促炎反应放大型细胞,从而在Lipopolysaccharide作用下显著放大TLR4介导的炎症级联反应。体外培养的星形胶质细胞实验进一步验证了高糖可增强其对Lipopolysaccharide的反应性,促进炎症相关信号通路和细胞因子表达[3]。
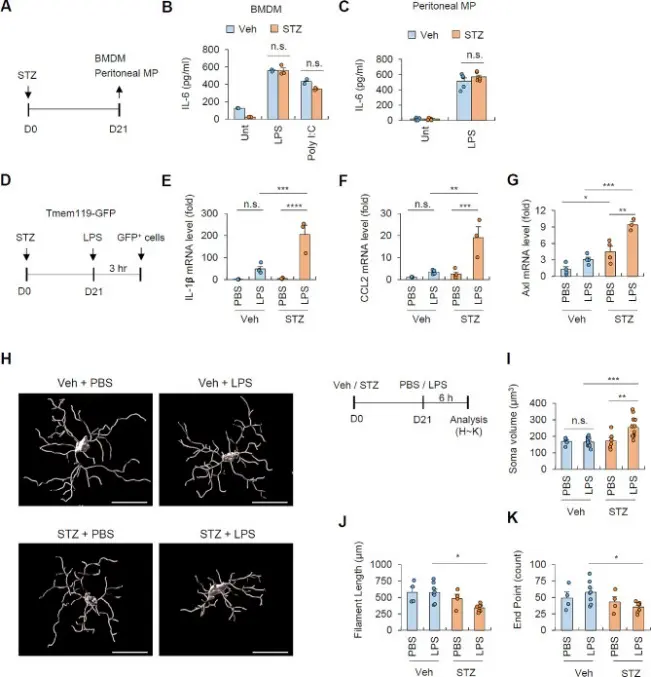
高血糖状况会增加小胶质细胞对全身LPS给药的敏感性[3]
文章标题:Circadian Gene BMAL1 Regulation of Cellular Senescence in Thyroid Aging

研究概览:
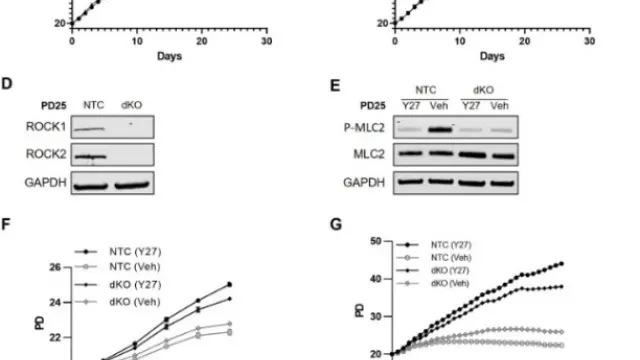
该研究围绕昼夜节律核心基因BMAL1在甲状腺衰老中的作用展开,通过体内与体外实验揭示其对细胞衰老进程的调控机制。比较了不同年龄阶段甲状腺组织中BMAL1的表达变化,发现随年龄增长其表达显著下降,并与细胞衰老标志物升高密切相关。进一步在甲状腺上皮细胞模型中,通过干预BMAL1表达,证实其可调控细胞周期停滞、氧化应激水平及炎症相关因子的表达,从而影响细胞衰老表型。机制研究显示,BMAL1通过调节氧化还原稳态及相关信号通路,维持甲状腺细胞功能稳定,延缓衰老进程。该研究表明,昼夜节律紊乱加速甲状腺细胞衰老并加剧甲状腺功能衰退,为理解甲状腺衰老机制和维持甲状腺功能稳定性提供了新的理论基础[4]。
在该研究中,Lipopolysaccharides(Cat. No. T11855)主要被用作一种细胞刺激剂来诱导细胞炎性反应和细胞衰老相关过程。这一实验帮助区分了BMAL1下降是衰老上游事件,而不是由Lipopolysaccharides激活的炎症引起,从机制上支持BMAL1在细胞衰老调控中的独立作用。
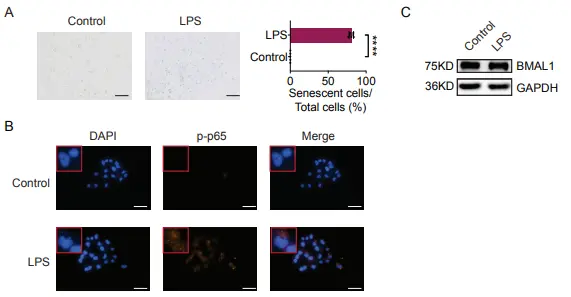
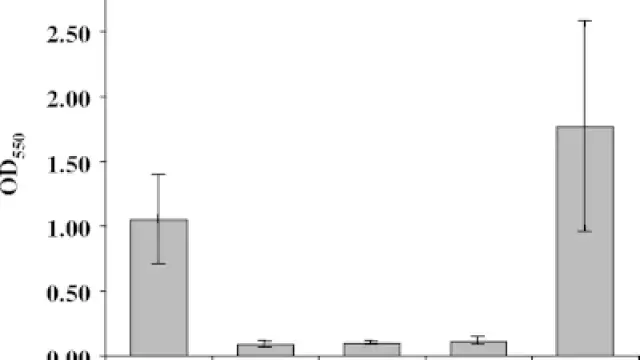
LPS诱导HTori-3.1细胞衰老和NF-κB活化,但不能抑制BMAL1的表达[4]
4. 参考文献
[1] Park BS, Lee JO. Recognition of lipopolysaccharide pattern by TLR4 complexes. Exp Mol Med. 2013 Dec 6;45(12):e66. doi: 10.1038/emm.2013.97. PMID: 24310172; PMCID: PMC3880462.
[2] Luo R, Yao Y, Chen Z, Sun X. An examination of the LPS-TLR4 immune response through the analysis of molecular structures and protein-protein interactions. Cell Commun Signal. 2025 Mar 18;23(1):142. doi: 10.1186/s12964-025-02149-4. PMID: 40102851; PMCID: PMC11921546.
[3] Lee KS, Yoon SH, Hwang I, Ma JH, Yang E, Kim RH, Kim E, Yu JW. Hyperglycemia enhances brain susceptibility to lipopolysaccharide-induced neuroinflammation via astrocyte reprogramming. J Neuroinflammation. 2024 May 27;21(1):137. doi: 10.1186/s12974-024-03136-1. PMID: 38802820; PMCID: PMC11131277.
[4] Zong D, Sun B, Ye Q, Cao H, Guan H. Circadian Gene BMAL1 Regulation of Cellular Senescence in Thyroid Aging. Aging Cell. 2025 Aug;24(8):e70119. doi: 10.1111/acel.70119. Epub 2025 May 28. PMID: 40434135; PMCID: PMC12341809.





 |
|