 您的购物车当前为空
您的购物车当前为空
TargetMol通用试剂——Doxorubicin hydrochloride(Cat. No. T1020, CAS. 25316-40-9),DNA嵌入型细胞杀手
1. 产品介绍
Doxorubicin hydrochloride,货号T1020,CAS号25316-40-9,别名盐酸多柔比星、NSC 123127、Hydroxydaunorubicin hydrochloride、DOX hydrochloride、Adriamycin HCl。Doxorubicin hydrochloride是一种具有细胞毒性和抗肿瘤活性的蒽环类抗生素,是人类DNA拓扑异构酶II的有效抑制剂,IC50分别为0.8 μM和2.67 μM。它可诱导细胞发生凋亡和自噬。在动物实验中,Doxorubicin hydrochloride常被用于诱导急性肾衰竭、慢性肾损伤以及心力衰竭模型。
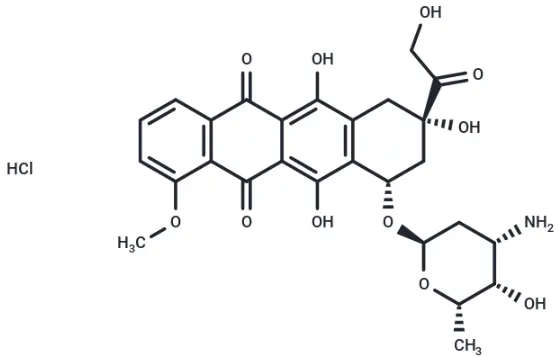
Doxorubicin hydrochloride分子结构式
2. 背景介绍
DNA拓扑异构酶(Topoisomerase, Topo)是调控DNA超螺旋状态与拓扑结构稳态的关键酶类,在DNA复制、转录、重组与修复过程中发挥核心作用。Topo I通过可逆的单链切割缓解扭转张力,Topo II则通过可逆的双链断裂解决DNA缠结与染色体分离问题。由于肿瘤细胞具有高度增殖特性,对拓扑异构酶活性依赖显著增强,因此该酶成为重要的抗肿瘤治疗靶点。拓扑异构酶抑制剂通过稳定“Topo–DNA切割复合物”,阻断DNA断裂后的重新连接,造成持续性DNA损伤并激活细胞死亡通路[1]。
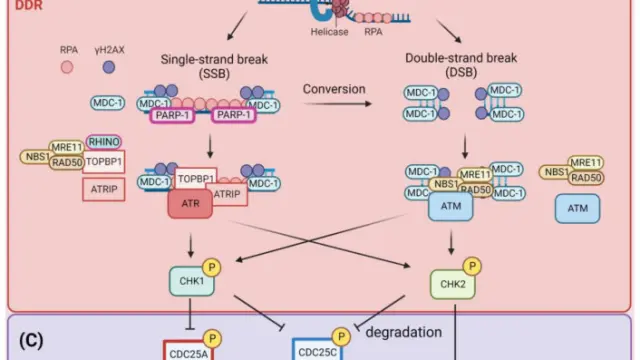
Doxorubicin hydrochloride作为经典蒽环类抗肿瘤药物,具有多通路协同的细胞毒性机制。其蒽环平面结构可嵌入DNA碱基对之间干扰双螺旋构象,同时稳定Topo II–DNA切割复合物,导致双链DNA断裂累积,抑制DNA复制与转录。此外,该药物还能通过线粒体损伤与活性氧(ROS)生成诱导凋亡,并在多种模型中调节自噬过程。更进一步,研究表明Doxorubicin会干扰细胞能量代谢信号,影响AMPK及其下游ACC的磷酸化状态,加剧能量应激并促进程序性细胞死亡。这些机制共同构成其广谱而强效的抗肿瘤活性基础[2]。
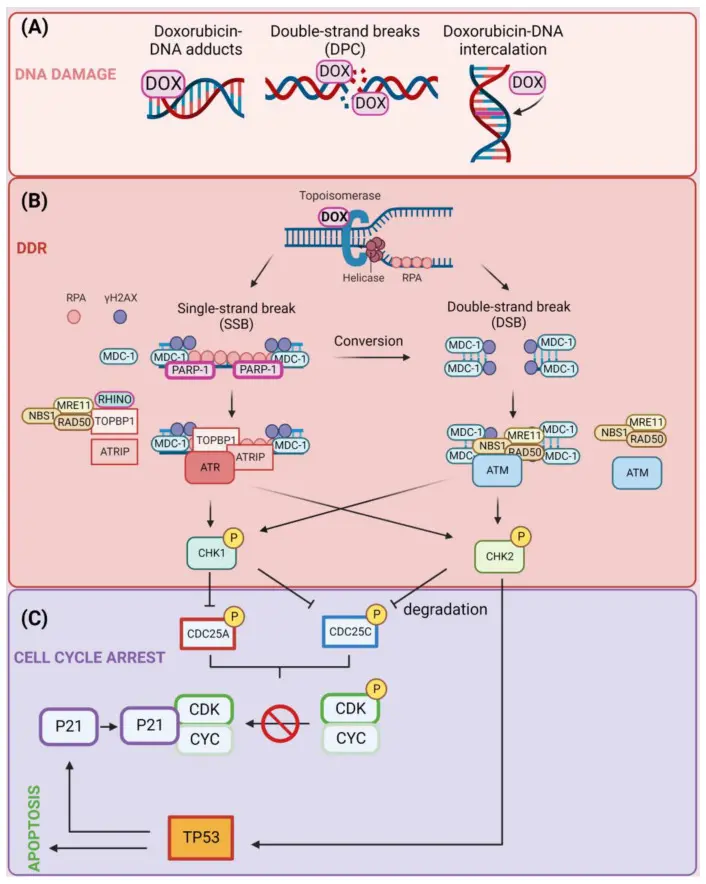
Doxorubicin(DOX)对DNA损伤的诱导[2]
3. 应用文献精选
文章标题:Doxorubicin downregulates autophagy to promote apoptosis-induced dilated cardiomyopathy via regulating the AMPK/mTOR pathway

研究概览:
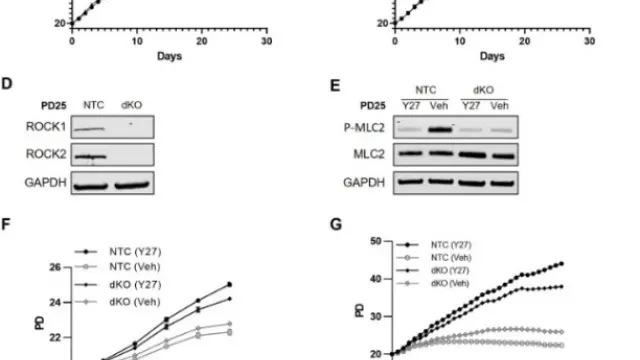
该研究通过体内小鼠模型和体外心肌细胞实验系统阐明了Doxorubicin诱导扩张型心肌病的关键分子机制。研究发现,Doxorubicin处理显著增加心肌细胞内ROS水平并导致线粒体功能障碍,同时抑制能量感应通路AMPK的活化及其下游mTOR信号调控,进而抑制具有保护作用的自噬过程。自噬受阻后,受损线粒体和氧化应激无法有效清除,最终加剧caspase依赖的细胞凋亡,导致心肌结构和功能损伤。进一步通过药理或遗传方式恢复AMPK活性或增强自噬,可明显减轻Doxorubicin诱导的心肌细胞凋亡和心功能异常。该研究揭示了“AMPK/mTOR-自噬-凋亡”轴在Doxorubicin心脏毒性中的核心调控作用,为缓解其心肌毒性提供了潜在干预靶点[3]。
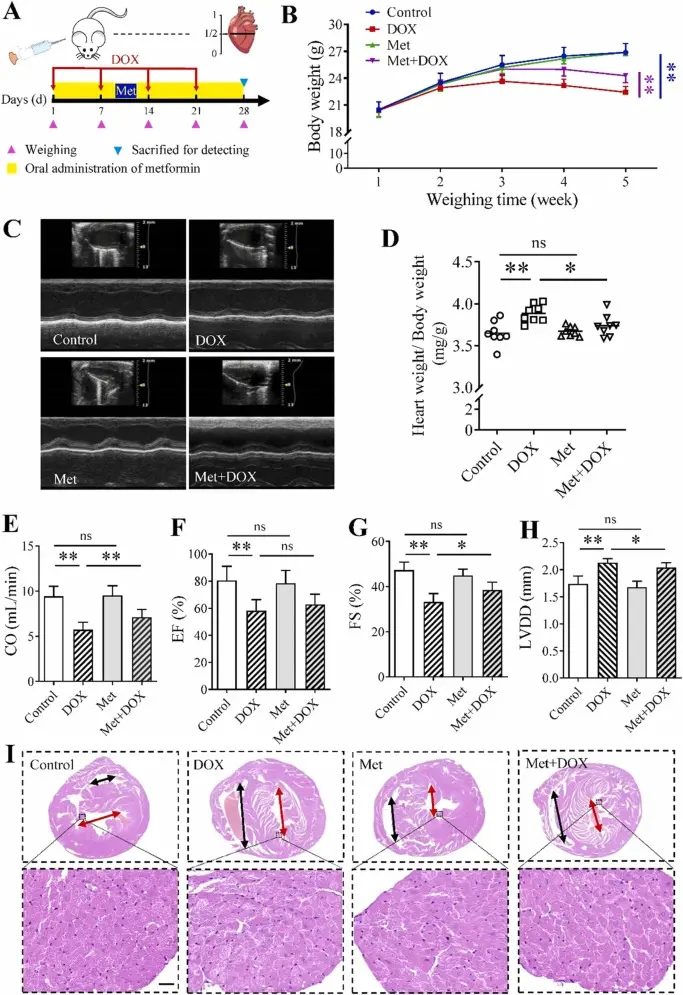
DOX抑制AMPK活性通过下调自噬促进细胞凋亡诱导扩张型心肌病[3]
文章标题:USP13 dictates Ran turnover and vulnerability to ferroptosis in diffuse large B cell lymphoma (DLBCL)

研究概览:
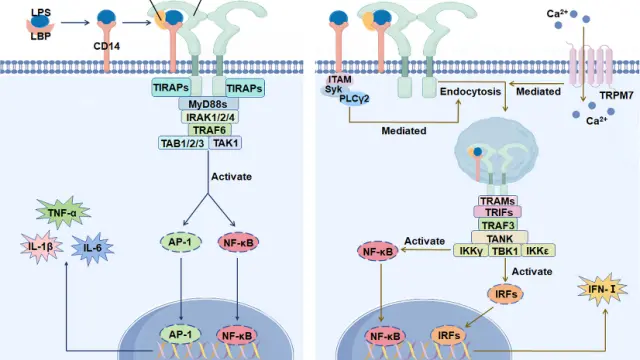
该研究在弥漫性大B细胞淋巴瘤(DLBCL)模型中揭示了去泛素化酶USP13通过调控小GTP酶Ran的蛋白稳定性而影响细胞对铁死亡(ferroptosis)敏感性的关键机制。作者发现,USP13可去除Ran的泛素化修饰,维持其蛋白稳态;当USP13被抑制或敲低时,Ran蛋白发生加速降解,导致核质转运稳态受损并引发细胞内铁稳态紊乱和脂质过氧化积累,从而显著增强DLBCL细胞对铁死亡诱导剂的敏感性。进一步的体内外实验表明,USP13–Ran轴是调控DLBCL细胞抗铁死亡能力的重要分子通路,靶向USP13可作为提高肿瘤对铁死亡治疗策略响应性的潜在新途径[4]。
在该研究中,Doxorubicin(Cat. No. T1020)被用作DLBCL细胞的常规化疗药物对照与联合处理工具。利用Doxorubicin诱导DNA损伤和细胞应激,评估在USP13被抑制或敲低的背景下,DLBCL细胞对化疗应答的变化。
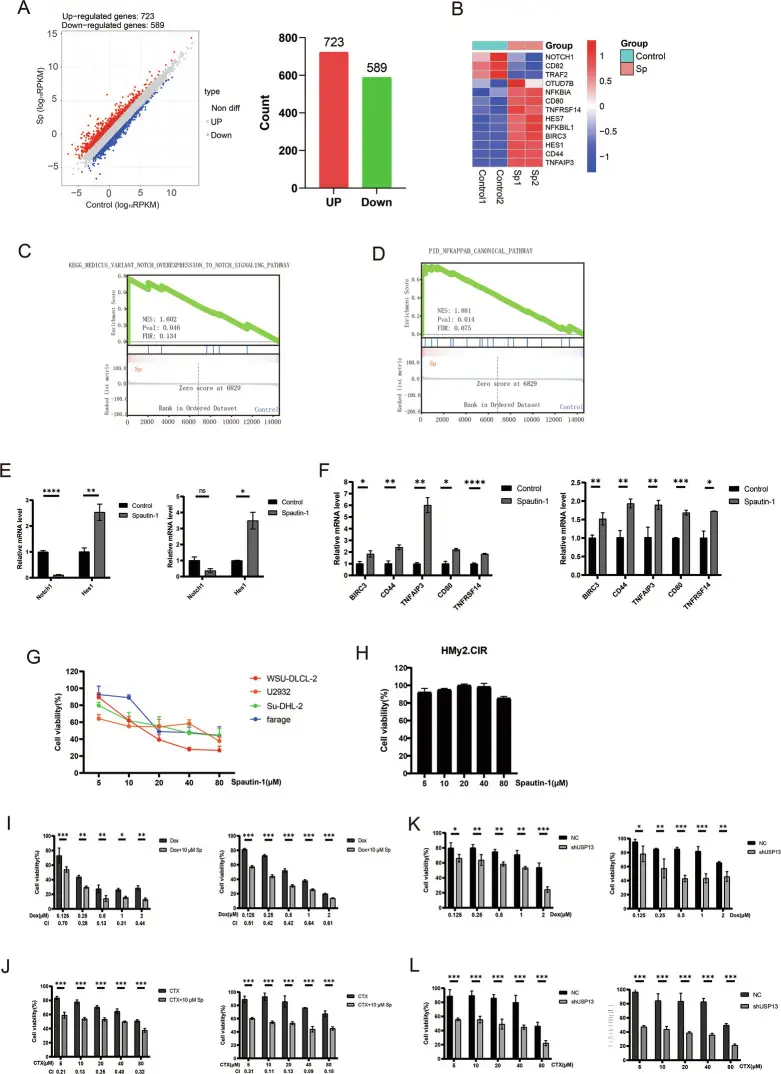
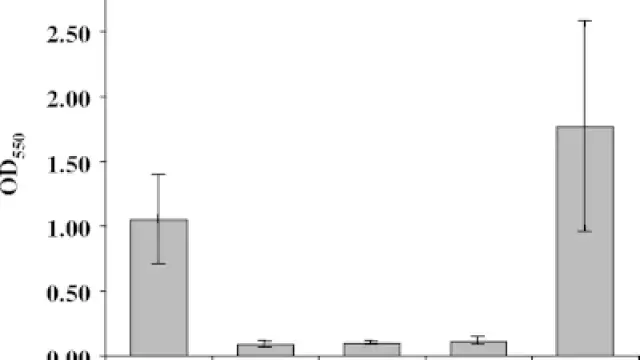
Spautin-1抑制DLBCL细胞存活,与Doxorubicin(Dox)或Cyclophosphamide(CTX)具有协同作用[4]
4. 参考文献
[1] Pommier Y. Topoisomerase I inhibitors: camptothecins and beyond. Nat Rev Cancer. 2006 Oct;6(10):789-802. doi: 10.1038/nrc1977. PMID: 16990856.
[2] Kciuk M, Gielecińska A, Mujwar S, Kołat D, Kałuzińska-Kołat Ż, Celik I, Kontek R. Doxorubicin-An Agent with Multiple Mechanisms of Anticancer Activity. Cells. 2023 Feb 19;12(4):659. doi: 10.3390/cells12040659. PMID: 36831326; PMCID: PMC9954613.
[3] Zhang S, Wei X, Zhang H, Wu Y, Jing J, Huang R, Zhou T, Hu J, Wu Y, Li Y, You Z. Doxorubicin downregulates autophagy to promote apoptosis-induced dilated cardiomyopathy via regulating the AMPK/mTOR pathway. Biomed Pharmacother. 2023 Jun;162:114691. doi: 10.1016/j.biopha.2023.114691. Epub 2023 Apr 14. PMID: 37060659.
[4] Qiao X, Yang X, Diao Y, Li Q, Wang X, Li C, Yang Z, Chng WJ, Li B. USP13 dictates Ran turnover and vulnerability to ferroptosis in diffuse large B cell lymphoma (DLBCL). Cell Death Dis. 2025 Nov 28;16(1):870. doi: 10.1038/s41419-025-08207-6. PMID: 41315297; PMCID: PMC12663190.





 |
|