 您的购物车当前为空
您的购物车当前为空
背景
肿瘤免疫治疗的出现为癌症治疗带来了革命性突破,但PD-1/PD-L1抑制剂、CAR-T细胞疗法等现有主流方案,在实体瘤治疗中仍面临响应率低、易产生耐药性的现实瓶颈,如何突破这一困境成为领域内的研究热点。

2026年3月发表于 Cancer Cell 的综述 "Macrophages: Targets for next-generation cancer immunotherapy" ,聚焦肿瘤微环境中的核心免疫细胞——肿瘤相关巨噬细胞(TAMs),系统剖析其生物学特性、促肿瘤机制及靶向治疗策略,为下一代肿瘤免疫治疗提供了研究方向与思路。

TAM 群体具有高度复杂性与异质性
肿瘤微环境中的 TAM 主要来自两大发育谱系:
-
组织驻留巨噬细胞(RTMs)
-
单核细胞来源巨噬细胞(mo‑macs)
研究表明,在肿瘤早期抑制 RTM 驱动的炎症可能具有预防或阻断肿瘤进展的潜力。但由于 RTMs 在正常组织中承担重要稳态功能,治疗必须精准靶向其促癌的特定分子程序,避免影响正常生理功能。
相比之下,向骨髓来源巨噬细胞的转变对治疗更具价值。
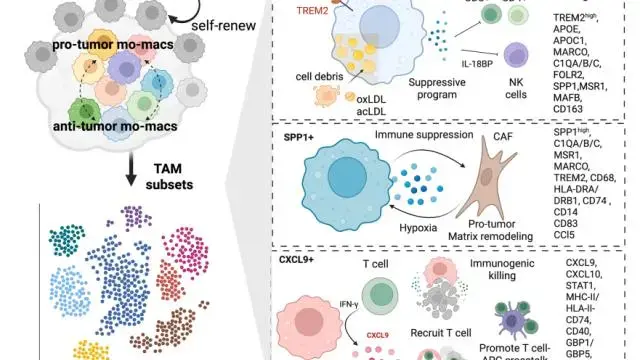
目前最具代表性、跨癌种反复出现的三类 TAM 亚群:
-
CXCL9+ TAMIFN‑γ 激活的巨噬细胞,具有免疫原性,与良好预后相关。
-
SPP1+ TAM经典免疫抑制表型,富集于缺氧 / 坏死区域,与不良预后相关。
-
TREM2+ TAM多数肿瘤中发挥免疫抑制作用,与更差生存相关;但在肝癌中呈现促免疫应答作用。
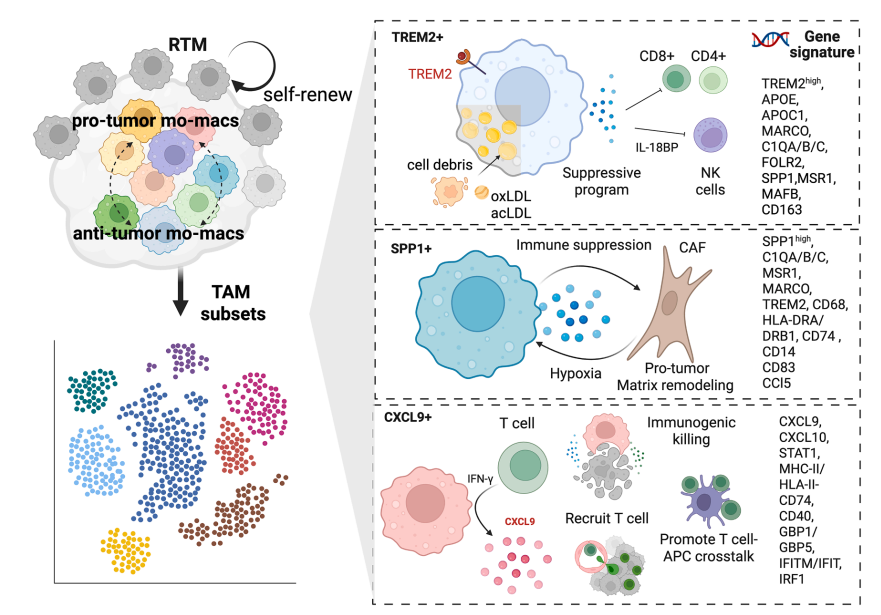
TAM 多样性与实体瘤中常见的分子程序

肿瘤可在局部与骨髓源头调控 TAM
肿瘤不仅在局部促使单核细胞形成 TAM,还能系统性调控骨髓与脾脏的造血过程。
肿瘤分泌的可溶性因子(IL‑1α/β、IL‑6、IL‑8、CCL2、CSF‑1 等)可作用于骨髓,产生两方面效应:
-
直接动员免疫抑制性髓系祖细胞向肿瘤迁移
-
对髓系祖细胞进行表观遗传修饰,使其倾向于分化为促瘤巨噬细胞
脾脏也会被肿瘤利用,成为髓系前体细胞扩增的重要场所。深入理解这一系统调控机制,有助于开发从源头阻断促瘤 TAM 产生的全新治疗策略。
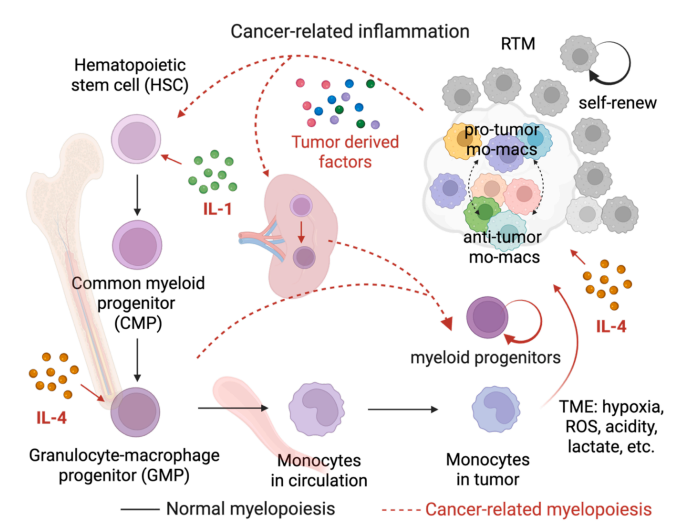
肿瘤在局部和全身层面调控巨噬细胞

巨噬细胞的促瘤与抗肿瘤功能
(一)促瘤功能
-
分泌 EGF、IL‑6 等促进肿瘤细胞增殖
-
分泌 VEGFA、SEMA4D 促进血管生成
-
表达基质金属蛋白酶(MMPs)重塑细胞外基质
-
通过 ARG1、IDO1 耗尽微环境营养物质
-
高表达 PD‑L1,分泌 TGF‑β、IL‑10 介导免疫抑制
(二)抗肿瘤功能
-
释放 TNF‑α、NO/ROS 直接杀伤肿瘤细胞
-
吞噬损伤 / 凋亡的肿瘤细胞
-
通过抗原呈递、分泌趋化因子与细胞因子激活 CD8+ T 细胞与 NK 细胞
-
可杀伤 MHC 缺陷型肿瘤,在 T 细胞治疗无效时仍能发挥作用
越来越多证据表明:PD‑1/PD‑L1 抑制剂等 T 细胞靶向疗法的疗效,高度依赖巨噬细胞。IFN‑γ 激活的巨噬细胞(CXCL9+)富集与免疫检查点阻断疗效显著正相关。阻断巨噬细胞上的 PD‑1 也能恢复其吞噬能力。这意味着:不激活巨噬细胞,单纯激活 T 细胞往往难以达到最佳效果。

巨噬细胞靶向治疗策略
(一)TAM 清除或减少聚集
选择性清除促瘤 TAM通过靶向 TAM 特异性标志物,如 TREM2、FOLR2(FRβ),利用抗体、CAR‑T 等实现精准清除。
研究证实:清除 FOLR2+ 或 TREM2+ TAM 可增强内源性抗肿瘤免疫,并与 CAR‑T、免疫检查点抑制剂协同。
(二)巨噬细胞治疗性效应化
效应化的目标是快速激活巨噬细胞的杀伤功能,包括吞噬、释放毒性因子、启动 T 细胞应答。
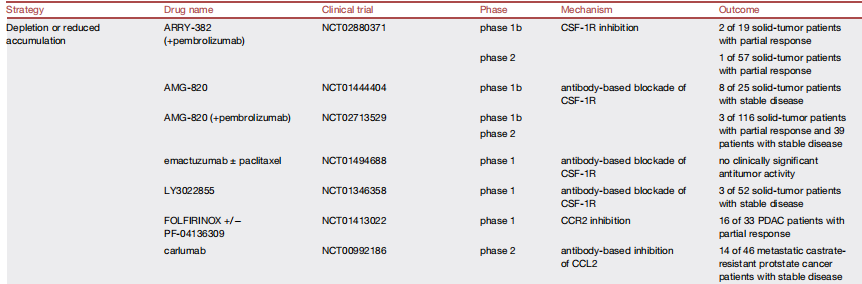
巨噬细胞靶向癌症治疗临床试验现状
(三)巨噬细胞重编程
重编程的目标是从根源上将促瘤 TAM 转变为抗肿瘤表型,效果更持久。

巨噬细胞靶向癌症治疗的演进范式
更多具体内容可以点击文章链接进行了解
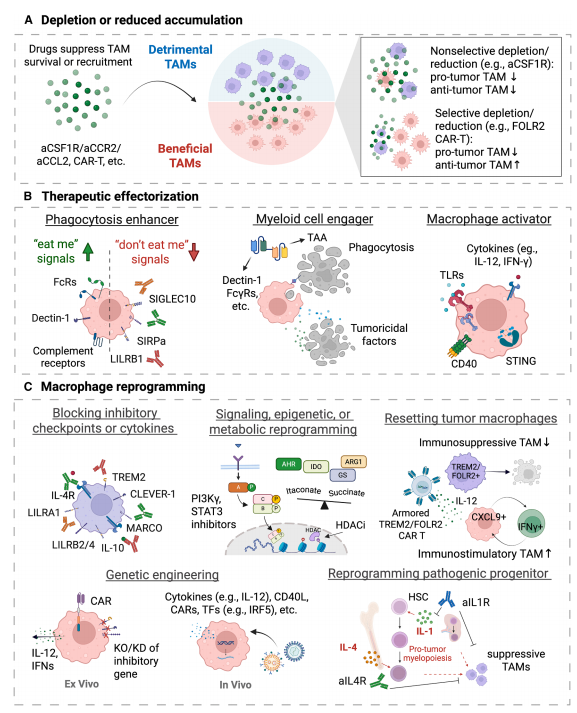
巨噬细胞靶向癌症治疗的演进范式

未来发展方向
建立多维 TAM 模型(6D 模型)
理性设计新一代治疗(4D 设计)
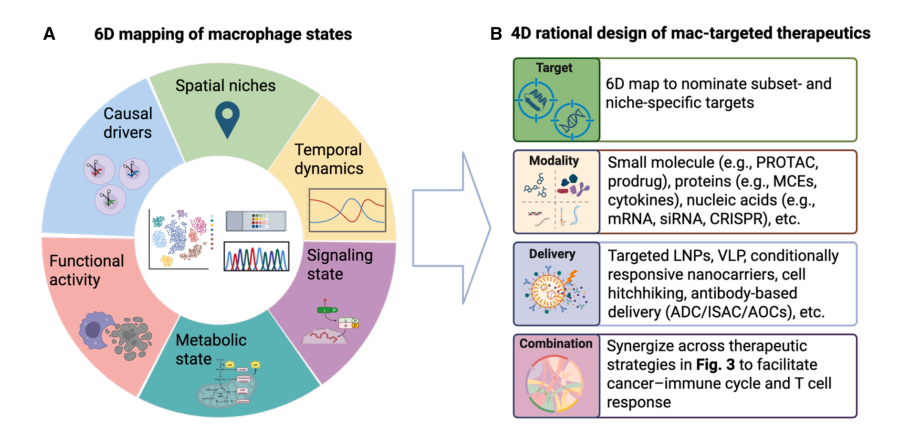
面向新一代巨噬细胞靶向治疗的多维设计
临床开发策略
-
基于 TAM 标志物进行患者分层
-
治疗中连续监测 TAM 状态
-
开发 TAM 中心型临床试验

总结
其他文章
订阅TargetMol新闻
科学新闻、观点和分析的重要汇总,每个工作日都会发送到您的收件箱.




 |
|