 您的购物车当前为空
您的购物车当前为空
TargetMol天然产物——Bafilomycin A1(Cat. No. T6740, CAS. 88899-55-2),自噬流研究的核心利器
1. 产品介绍
Bafilomycin A1,货号T6740,CAS号88899-55-2,别名巴弗洛霉素A、巴佛洛霉素A1、Baf A1。Bafilomycin A1属于大环内酯类天然产物,是一种V-ATPase抑制剂(IC50 = 0.44 nM),具有特异性。Bafilomycin A1是自噬流抑制剂,抑制溶酶体酸化,阻断自噬降解,阻断自噬流。Bafilomycin A1高浓度可引发溶酶体应激与非凋亡性细胞死亡。
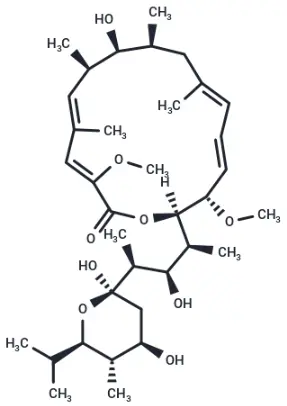
Bafilomycin A1分子结构式
2. 背景介绍
液泡型质子泵(Vacuolar-type H+-ATPase, V-ATPase)是一类广泛存在于真核细胞内的多亚基ATP依赖性质子泵,通过消耗ATP驱动质子(H+)跨膜转运,维持溶酶体、内体等胞内膜性细胞器的酸性环境。这种酸化对于溶酶体内蛋白酶的激活、内体与溶酶体的成熟与分化、以及自噬性降解过程的正常进行至关重要。V-ATPase的质子泵活性不仅影响内体/溶酶体的pH,还调控蛋白质降解、受体-配体分离、以及细胞内物质的转运与信号传导等关键细胞过程,其异常功能与多种疾病状态(如神经退行性疾病和肿瘤细胞稳态失衡)密切相关[1]。
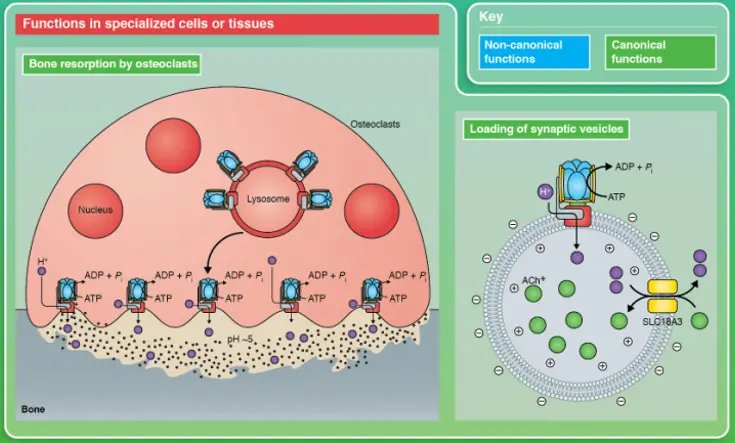
V-ATPase在特定的细胞或组织中行使功能[1]
Bafilomycin A1是一种源自Streptomyces属的大环内酯类抗生素,广泛用于细胞生物学研究中作为V-ATPase的高效、特异性且可逆的抑制剂。其作用靶向V-ATPase复合体的V0域(尤其是c环亚基),阻断V-ATPase介导的质子转运,从而抑制内体/溶酶体的酸化。由于溶酶体酸性条件是多个自噬终末步骤(包括自噬体与溶酶体融合及自噬通量维持)的关键,Bafilomycin A1通过抑制V-ATPase功能阻断了这些过程,致使成熟自噬体无法与溶酶体融合,导致自噬流终止和自噬体积累[2]。
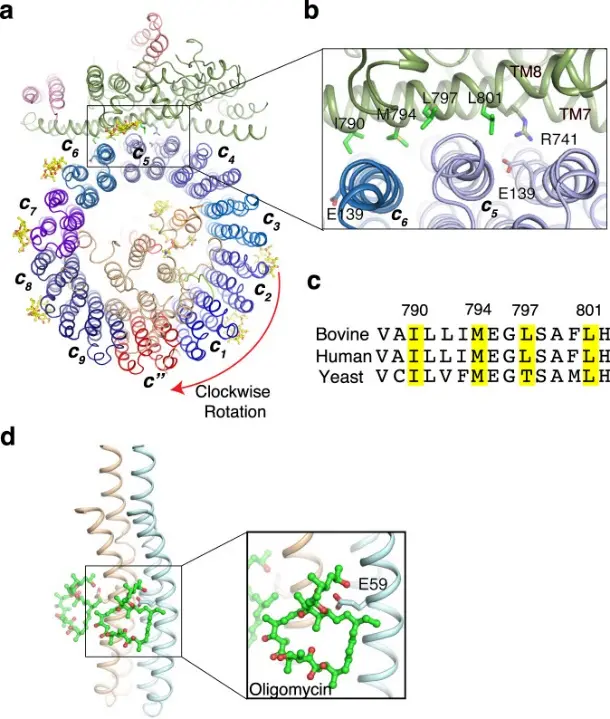
Bafilomycin A1抑制c环旋转的机制[2]
3. 应用文献精选
文章标题:Bafilomycin A1 induces colon cancer cell death through impairment of the endolysosome system dependent on iron

研究概览:
该研究探讨了Bafilomycin A1(BA1)对结肠癌和正常结肠成纤维细胞(CCD-18Co)细胞的影响,发现在极低纳摩尔浓度下,Bafilomycin A1能选择性抑制多种结肠癌细胞的存活与增殖,并通过破坏晚期内溶酶体系统(包括溶酶体数量/大小异常、膜通透性改变、以及自噬流受阻)引起溶酶体应激和细胞内铁稳态失衡,最终导致癌细胞死亡。此外,补充铁(III)-柠檬酸盐能部分逆转这些效应,表明内溶酶体功能紊乱引发的铁缺乏是Bafilomycin A1介导细胞死亡的重要因素,同时该机制与内质网应激及脂滴积累相关,并提出靶向内溶酶体及铁稳态有望作为结肠癌治疗的新策略[3]。
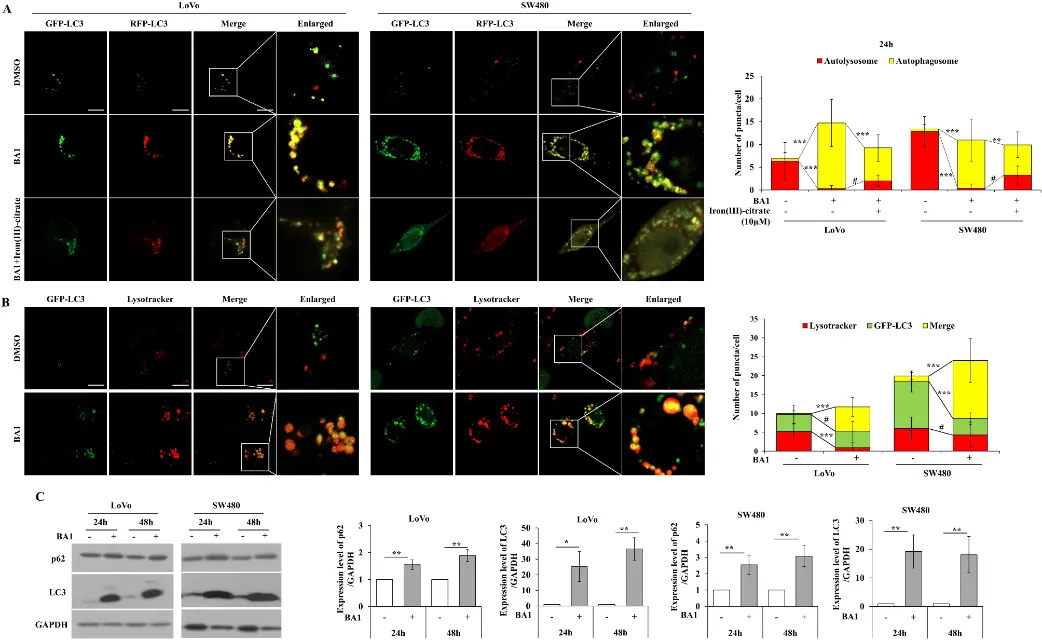
Bafilomycin A1破坏了包括自噬在内的内溶酶体系统[3]
文章标题:Osimertinib activates TFEB to trigger hepatocyte cytoplasmic vacuolation-associated cell death

研究概览:
这项研究系统性揭示了Osimertinib导致肝细胞损伤和独特的细胞死亡机制的分子基础:研究发现Osimertinib不仅能在临床上治疗带有EGFR突变的非小细胞肺癌患者,其在肝细胞中也直接触发明显的胞质液泡形成,与传统的凋亡或坏死不同,这种液泡化伴随细胞死亡是由过度激活的自噬-溶酶体通路引起的。其分子机制在于Osimertinib促进了转录因子TFEB的去磷酸化和核转位,激活TFEB介导的溶酶体与自噬基因表达,从而增强自噬-溶酶体生物合成,引发大量溶酶体/自溶酶体的形成并最终导致液泡积聚及细胞死亡;研究还证明可以通过抑制TFEB的激活(例如S-腺苷-L-蛋氨酸)缓解这种细胞损伤,从而为临床上控制Osimertinib肝毒性提供了潜在策略,同时拓宽了对药物诱导性肝损伤机制的理解[4]。
这项研究中,Bafilomycin A1(Cat. No. T6740)被用作经典的溶酶体酸化抑制剂与自噬晚期抑制剂,用于功能性验证Osimertinib诱导的细胞液泡化是否依赖于自噬-溶酶体通路的过度激活。
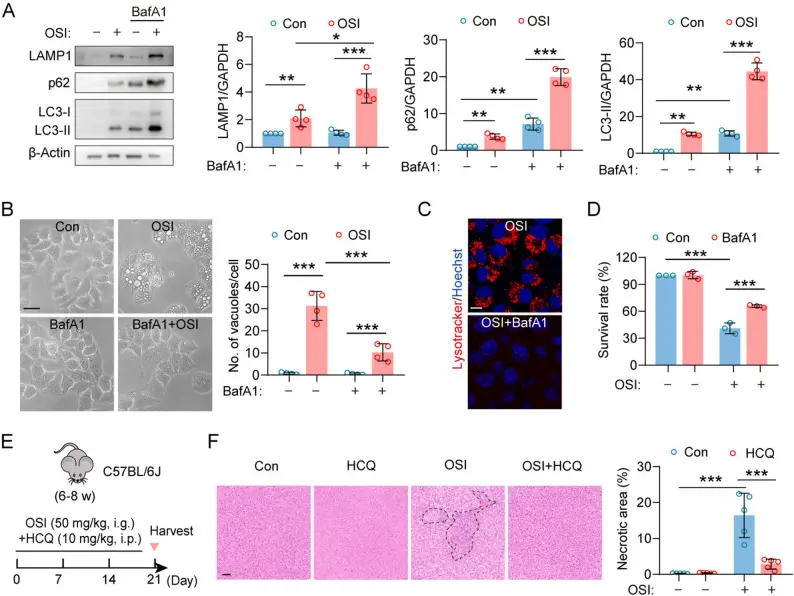
Hydroxychloroquine通过抑制自噬溶酶体通路,挽救Osimertinib引起的肝损伤[4]
4. 参考文献
[1] Maxson ME, Grinstein S. The vacuolar-type H⁺-ATPase at a glance - more than a proton pump. J Cell Sci. 2014 Dec 1;127(Pt 23):4987-93. doi: 10.1242/jcs.158550. PMID: 25453113.
[2] Wang R, Wang J, Hassan A, Lee CH, Xie XS, Li X. Molecular basis of V-ATPase inhibition by bafilomycin A1. Nat Commun. 2021 Mar 19;12(1):1782. doi: 10.1038/s41467-021-22111-5. PMID: 33741963; PMCID: PMC7979754.
[3] Min DH, Kim D, Hong ST, Kim J, Kim MJ, Kwon SH, Kim A, Lee JY. Bafilomycin A1 induces colon cancer cell death through impairment of the endolysosome system dependent on iron. Sci Rep. 2025 Feb 12;15(1):5148. doi: 10.1038/s41598-025-89127-5. PMID: 39934167; PMCID: PMC11814099.
[4] Qiu Y, Liu Y, Ding H, Xin W, Lu S, Hu Y, Chen J, Weng Q, Wang J, Fang L. Osimertinib activates TFEB to trigger hepatocyte cytoplasmic vacuolation-associated cell death. Cell Commun Signal. 2026 Jan 30;24(1):142. doi: 10.1186/s12964-026-02688-4. PMID: 41612351; PMCID: PMC12934022.





 |
|