 您的购物车当前为空
您的购物车当前为空

2025年12月,新加坡科技研究局(A*STAR)分子与细胞生物学研究所(IMCB)的 Nick Barker 带领的研究团队在 Science 上发表了题为"AQP5: A functional gastric cancer stem cell marker in mouse and human tumors" 的文章,明确了AQP5 作为胃癌 CSCs 标志物的有效性,阐明其作用机制,并验证靶向治疗潜力。


实验过程
AQP5 是胃癌特异性标志物
首先,研究团队借助 AQP5-Cre/APK 等小鼠遗传模型展开实验,发现小鼠体内的 AQP5 蛋白,仅在肿瘤上皮细胞的特定亚群中表达,而且与 Lgr5 这类已知细胞标志物分属不同的细胞族群。
为了验证这一发现的普适性,团队进一步延伸到人类样本研究。他们进行了公共数据库的单细胞 RNA 测序(scRNA-seq)数据分析、组织芯片免疫组化(IHC)检测、流式细胞术(FACS)分选,以及实时荧光定量 PCR(qPCR)验证 。最终得出结论:在人类肠型胃癌中,AQP5 的表达水平升高最为显著,且主要集中在 MUC6 阳性的黏液细胞群中。
更关键的是,通过流式细胞术分选后对比发现,AQP5 阳性细胞的蛋白表达量,明显高于 AQP5 阴性细胞。这一结果与小鼠实验完全吻合,有力证明了AQP5 作为胃癌相关标志物具有跨物种的保守性。
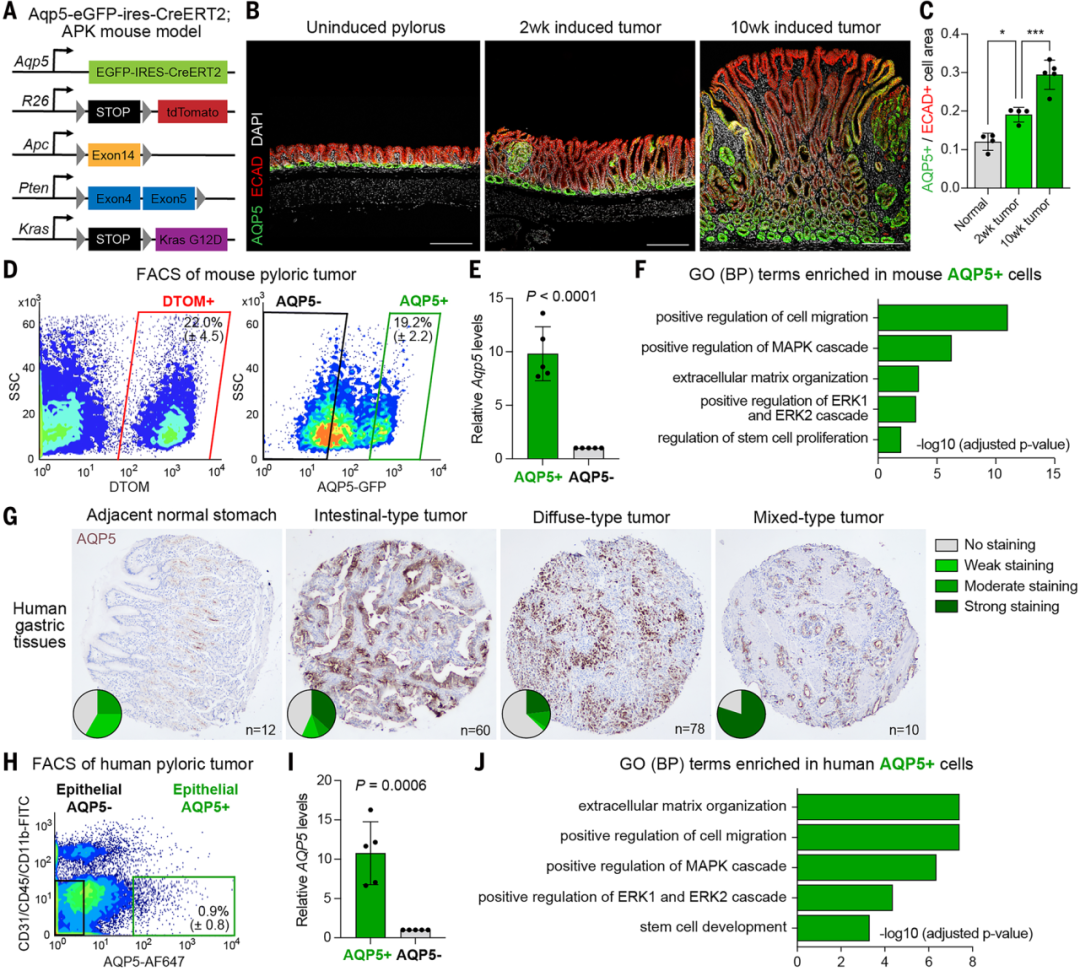
AQP5 在小鼠和人类幽门肿瘤中特异性表达及干细胞相关特征
AQP5 + 细胞具备完整的 CSCs 功能
-
“体外功能” 验证:通过类器官培养实验,证明AQP5 + 细胞可长期传代(>10 代),具备自我更新能力;而 AQP5 - 细胞传代 2-3 代后消亡,无干细胞特性。
-
“体内功能” 验证:通过免疫缺陷小鼠原位移植实验,证实 AQP5 +细胞能形成更大体积、高侵袭性的肿瘤,且可重构原始肿瘤的异质性(分化出 AQP5 + 和 AQP5 - 细胞),满足 CSCs “肿瘤起始” 核心功能。
-
“分化能力” 验证:通过人类细胞谱系的追踪,发现AQP5 +细胞可分化为多种胃上皮谱系细胞,具备多向分化潜能。
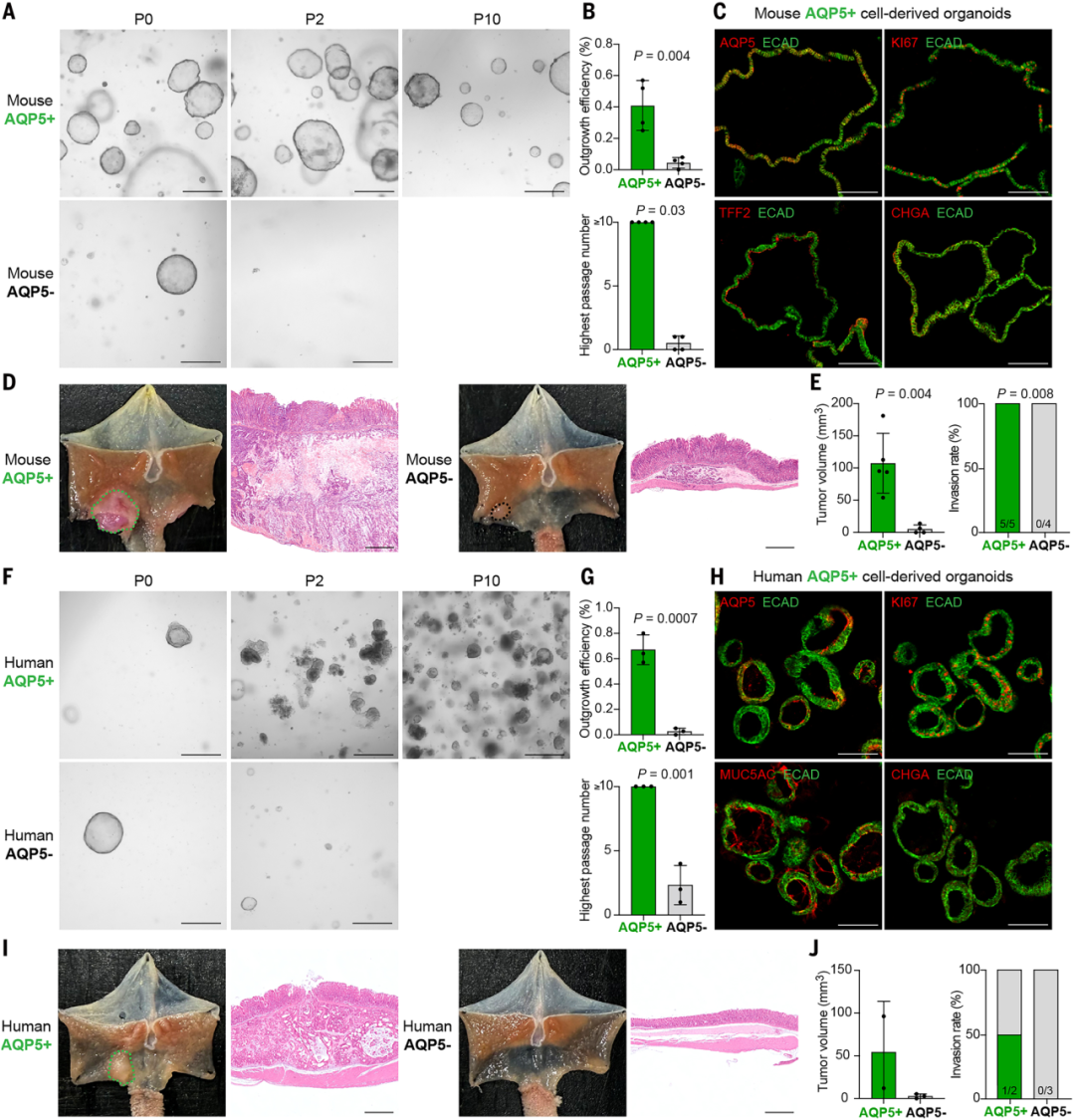
小鼠和人类 AQP5 + 细胞的胃癌干细胞功能验证
AQP5 的功能机制及靶向治疗潜力
-
研究人员通过 AQP5 敲除(KO)、过表达(OE)实验,结合通路检测,发现 AQP5 阻断 WNT、PI3K、MAPK 信号通路(均使用了TargetMol 提供的特异性抑制剂,阻断通路来观察类器官增殖变化),从而促进癌细胞增殖、侵袭;证实AQP5可驱动胃癌进展。
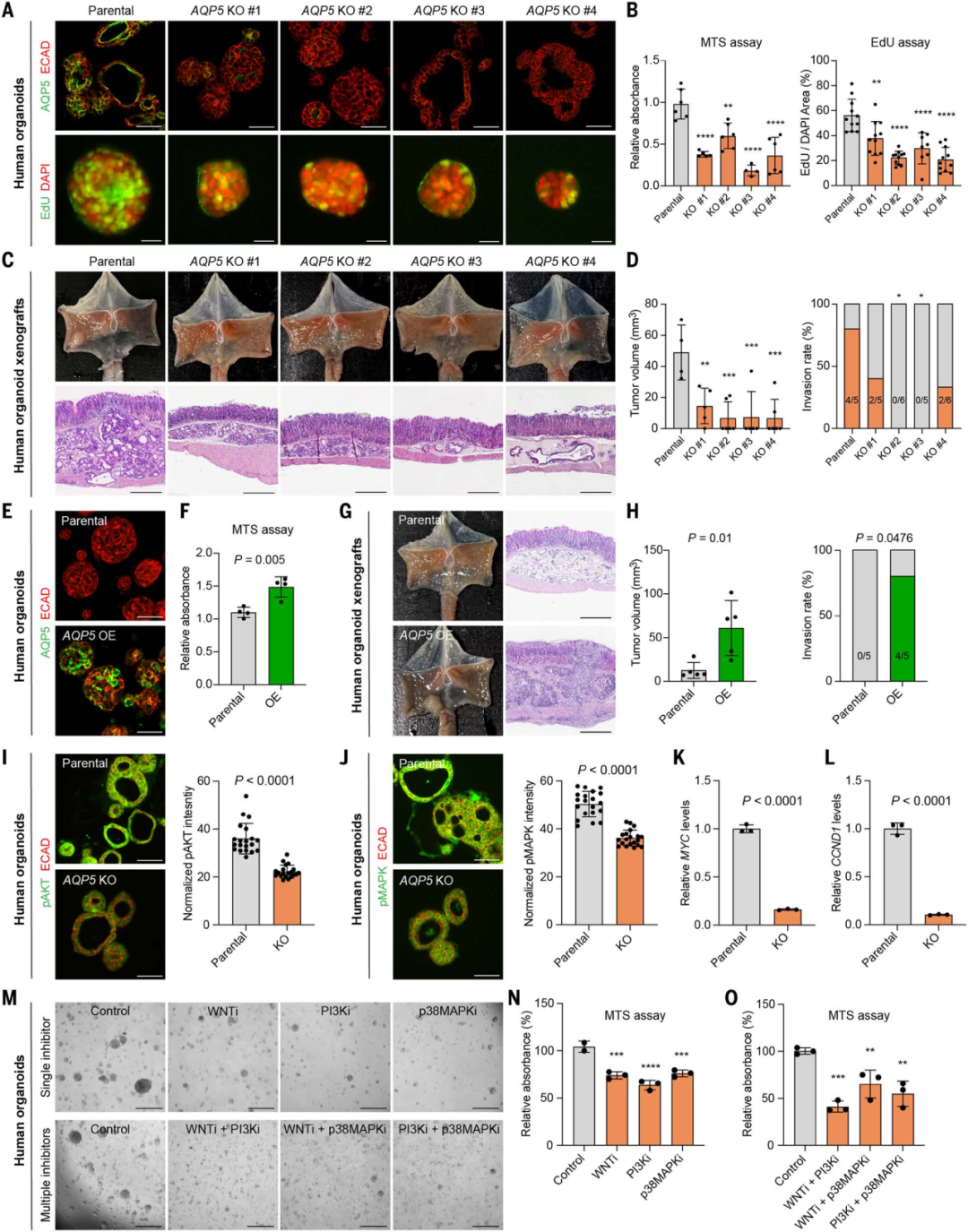
AQP5 通过 WNT/PI3K/MAPK 通路驱动胃癌进展
-
研究人员在小鼠模型中用白喉毒素(DT)特异性清除AQP5 +细胞,从而阻断肿瘤起始、促进已建立肿瘤消退;
在人类类器官中用同源二聚化剂诱导 AQP5 + 细胞凋亡,显著抑制类器官生长,证明靶向 AQP5 +细胞对于胃癌治疗的可行性。
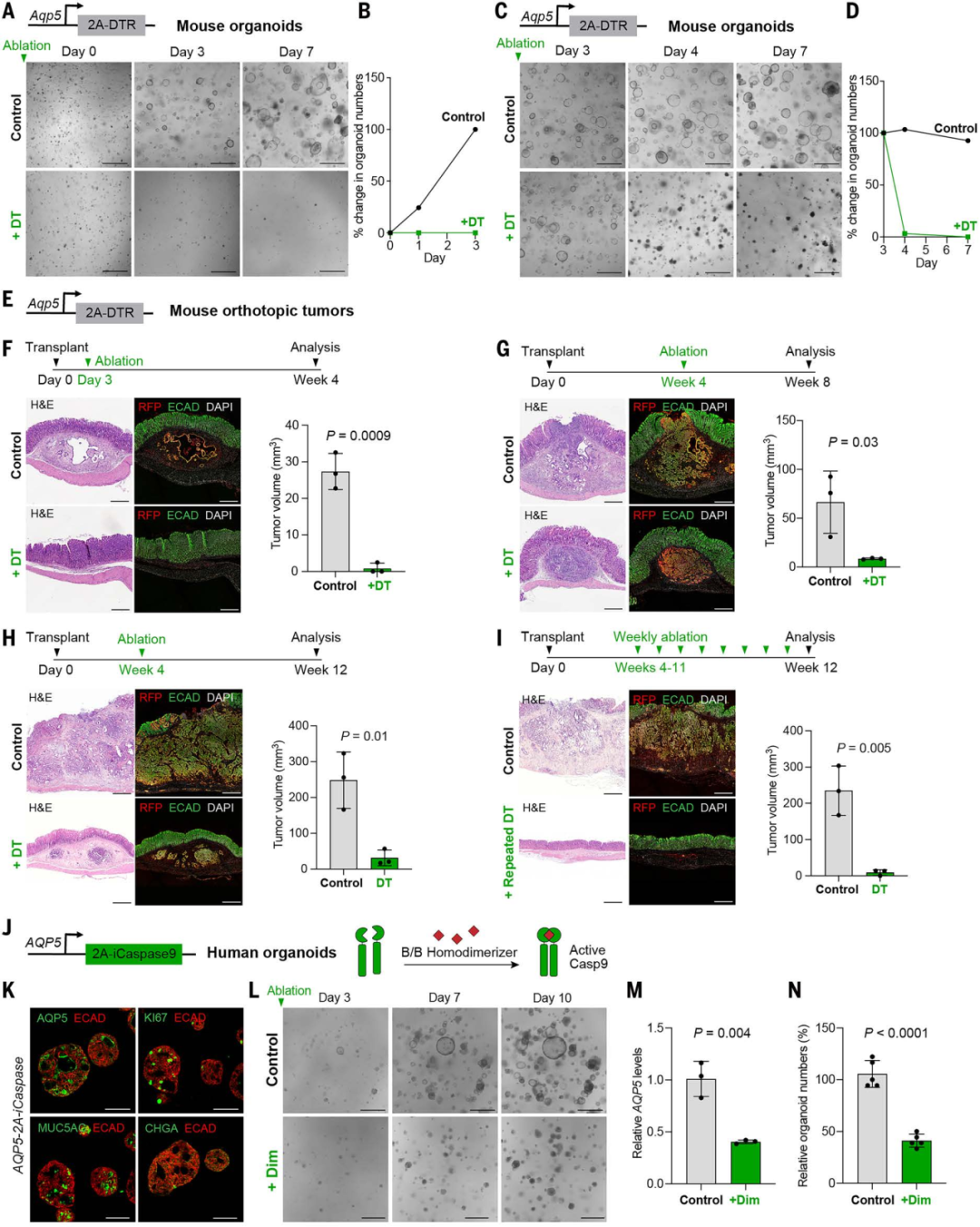
靶向消融 AQP5 + 细胞对肿瘤进展的抑制作用
-
研究人员通过构建转移性胃癌模型,发现转移灶中的 AQP5 +细胞仍具备类器官的形成能力,且 AQP5 KO 可阻断远处转移,因此上述研究结果也适用于 “转移性胃癌”。
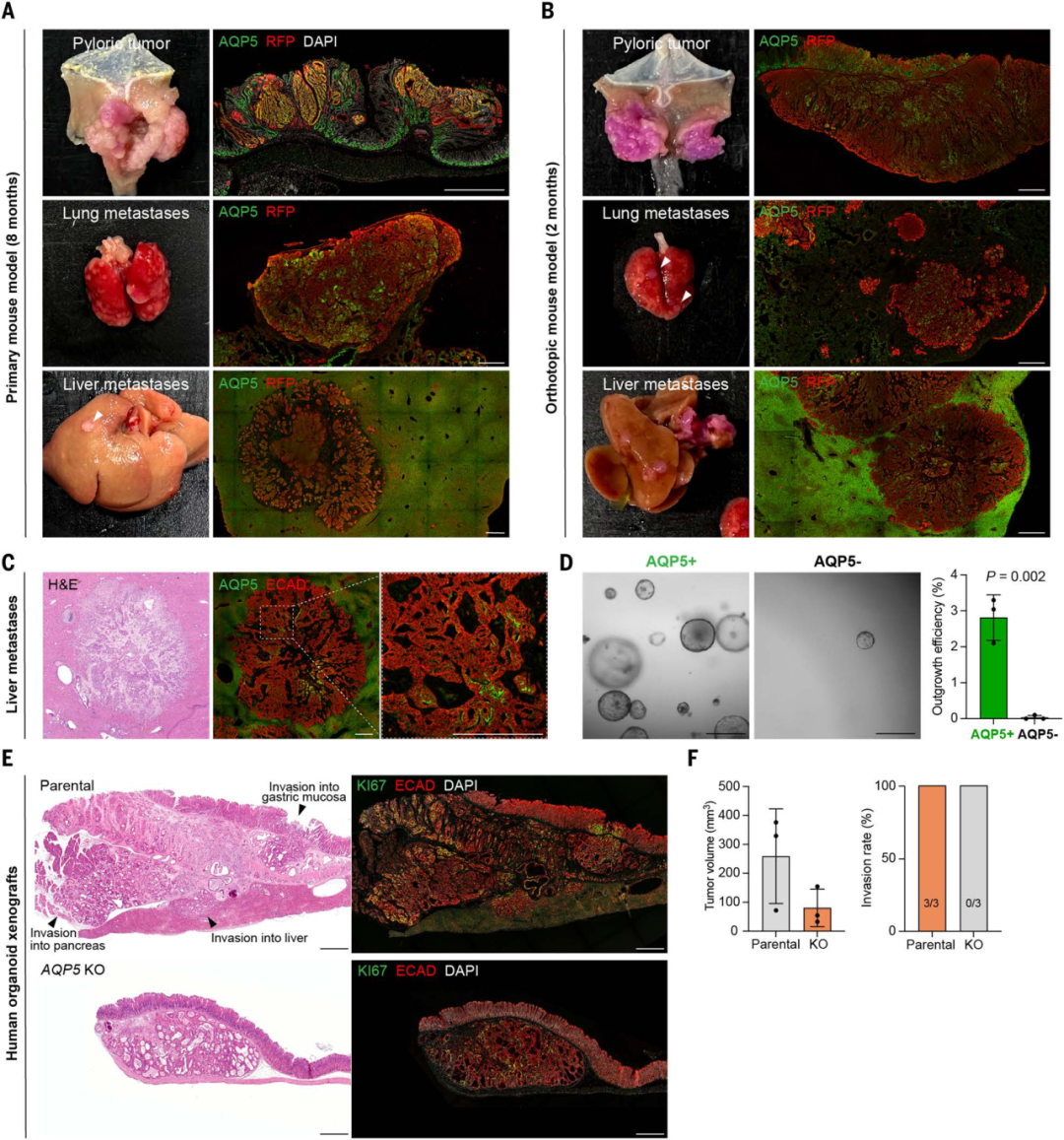
AQP5 + 细胞在转移性胃癌中的 CSCs 功能

总结
AQP5 是小鼠和人类胃癌(含转移灶)的功能性 CSCs 标志物,通过 WNT、PI3K、MAPK 通路驱动肿瘤进展,靶向 AQP5 + 细胞具有显著治疗潜力。为胃癌基础研究提供新工具,为临床转化开辟新路径。
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
其他文章

订阅TargetMol新闻
科学新闻、观点和分析的重要汇总,每个工作日都会发送到您的收件箱.




 |
|