 您的购物车当前为空
您的购物车当前为空
TargetMol染料——D-Luciferin potassium(Cat. No. T4139, CAS. 115144-35-9),照亮活体内部的灯泡
1. 产品介绍
D-Luciferin potassium,货号T4139,CAS号115144-35-9,别名D-萤光素钾盐、D-荧光素钾盐、D-Luciferin potassium Salt、D-Luciferin K Salt。D-Luciferin potassium(D-Luciferin K Salt)是一种荧光素酶(Luc)的底物,能够催化生物发光昆虫产生典型的黄绿光(560 nm)。D-Luciferin potassium可以用于荧光素酶实验。
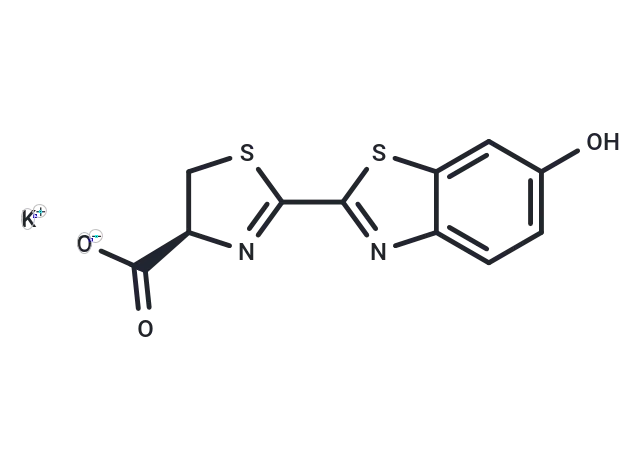
D-Luciferin potassium分子结构式
2. 背景介绍
萤火虫荧光素酶(Firefly luciferase)是一种存在于Photinus pyralis等萤火虫胚胎和组织中的ATP依赖性氧化酶。萤火虫荧光素酶能够催化荧光素底物的氧化反应,将化学能转化为可见光信号,因此常被用作分子生物学和细胞成像中的报告基因靶点。该酶具有高度的专一性和高量子产率,使其在体外和体内检测中广泛应用于基因表达、蛋白质相互作用、药物筛选等研究领域。此外,通过对荧光素酶基因的工程改造,还可以获得针对不同发光波长和发光强度的优化变体,进一步拓展其在多重生物成像中的应用范围[1]。
D-Luciferin potassium是萤火虫荧光素酶反应的关键底物,其作用机制本质上是作为发光化学反应的直接供体。D-Luciferin在荧光素酶催化下,与ATP和氧气发生酰胺化和随后的氧化环化反应,生成氧化产物(氧化荧光素)并伴随光子发射。这一反应严格依赖于ATP,因为ATP不仅参与底物激活,还通过与荧光素酶构象变化紧密耦合来增强催化效率。D-Luciferin的钾盐形式提高了其水溶性和稳定性,便于在体外实验和细胞/动物体内成像中使用。其发光强度与底物浓度、ATP水平和酶活性直接相关,因此常用于监测细胞能量代谢、实时追踪基因表达以及药物作用效应[2]。
3. 应用文献精选
文章标题:Luciferase-based bioluminescence revealed the facilitated diffusion of D-luciferin mediated by SLC17A3

研究概览:
该研究通过实验表明,在表达不同荧光素酶系统的细胞中,D-Luciferin的摄取和生物发光强度与膜转运蛋白SLC17A3有关,说明D-Luciferin的体内分布和跨膜扩散可能受特定载体调控。该研究采用了细胞系表达荧光素酶的体外模型,并结合生物化学和生物物理学方法实测了D-Luciferin与底物之间的动力学关系,为理解底物在细胞环境中的行为提供了实验数据支持[3]。
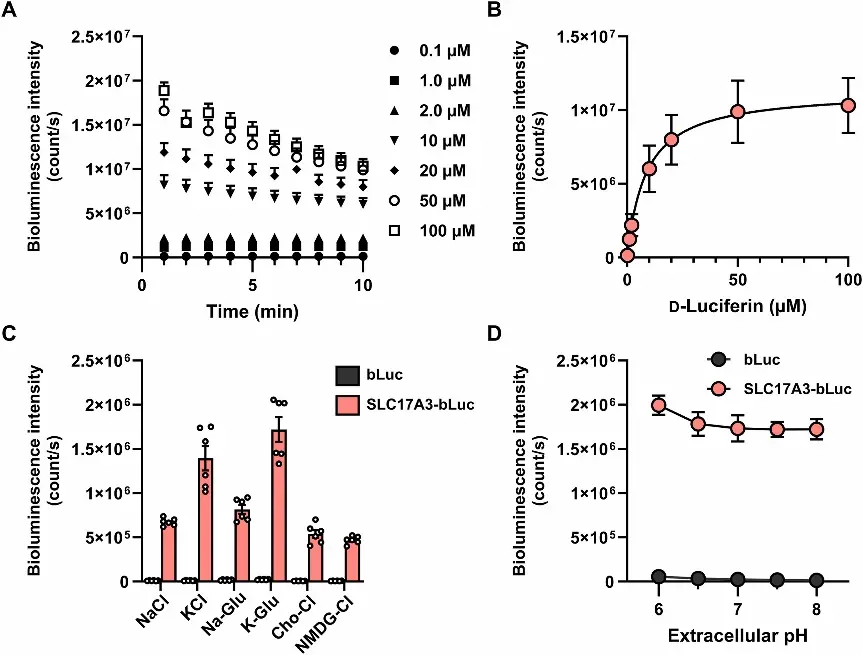
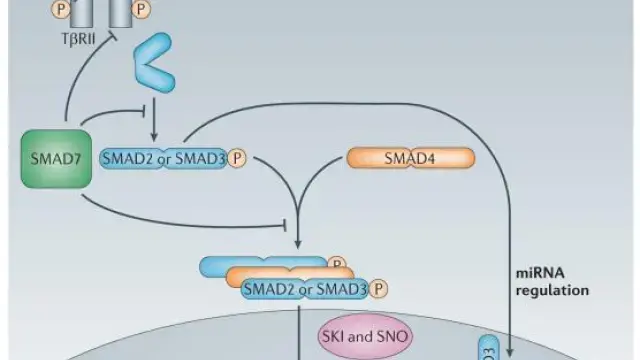
基于SLC17A3-bLuc和D-Luciferin细胞生物发光的机SLC17A3功能特性[3]
文章标题:AR+TREM2+ macrophage induced pathogenic immunosuppression promotes prostate cancer progression

研究概览:
该研究揭示了一类在前列腺癌肿瘤微环境中共表达雄激素受体(AR)和髓系细胞触发受体-2(TREM2)的肿瘤相关巨噬细胞(TAMs)具有显著的免疫抑制和促肿瘤功能;机制上,肿瘤微环境中的载脂蛋白E(APOE)可结合TREM2并诱导巨噬细胞中AR的表达,进而上调IL-10、TGF-β、IL-23A与CCL2等免疫抑制与促肿瘤基因的转录;在多种前列腺癌小鼠模型中,联合遗传敲除TREM2与药理性阻断AR显著延缓肿瘤进展,并增强抗-PD-1免疫治疗的疗效,同时这些标志物在前列腺癌患者中表达升高且与不良预后相关,提示针对TREM2-AR轴的调控可作为新的免疫调节治疗策略[4]。
在该文章中,D-Luciferin potassium(Cat. No. T4139)主要用于活体和体外的生物发光成像。在小鼠前列腺癌模型中使用携带萤火虫荧光素酶标记(luciferase-tagged)的RM1细胞,注射D-Luciferin potassium后,通过IVIS活体成像系统监测肿瘤生长和转移情况。此外,在体外实验中,在给药后将主要器官取出再激发成像,以定量分析肿瘤负荷和转移灶的生物发光信号,从而评估不同基因或治疗干预对肿瘤发展的影响。
4. 参考文献
[1] Feeney KA, Putker M, Brancaccio M, O'Neill JS. In-depth Characterization of Firefly Luciferase as a Reporter of Circadian Gene Expression in Mammalian Cells. J Biol Rhythms. 2016 Dec;31(6):540-550. doi: 10.1177/0748730416668898
[2] Zhang Y, Pullambhatla M, Laterra J, Pomper MG. Influence of bioluminescence imaging dynamics by D-luciferin uptake and efflux mechanisms. Mol Imaging. 2012 Nov-Dec;11(6):499-506. PMID: 23084250
[3] Morita K, Sato K, Tomabechi R, Yamaya R, Takada T, Kishimoto H, Higuchi K, Inoue K. Luciferase-based bioluminescence revealed the facilitated diffusion of D-luciferin mediated by SLC17A3. Biochem Biophys Res Commun. 2025 Feb 16;749:151360. doi: 10.1016/j.bbrc.2025.151360. Epub 2025 Jan 17. PMID: 39837223.
[4] Wang Q, Wu Y, Long Y, Li R, Shi Y, Zheng Y, Chen X, Li X, Zhou Y, Huang X, Jiang G. AR+TREM2+ macrophage induced pathogenic immunosuppression promotes prostate cancer progression. Nat Commun. 2025 Jul 29;16(1):6964. doi: 10.1038/s41467-025-62381-x





 |
|