 您的购物车当前为空
您的购物车当前为空
背景
CAR-T、TIL 等 T 细胞疗法在血液肿瘤中大放异彩,但在肺癌、胰腺癌、乳腺癌等实体瘤中却疗效受限,核心症结在于肿瘤微环境的免疫抑制性:肿瘤细胞通过基因组改变(如抑癌基因缺失)塑造出一个 “陷阱”—— 髓系抑制细胞大量富集、细胞外基质(ECM)过度沉积形成物理屏障,导致杀伤性 CD8+T 细胞无法有效浸润至肿瘤核心,最终引发免疫逃逸和治疗耐药。

2026年2月,中国科学院的王广川研究员,上海交通大学的陈洛南教授,广州实验室的景乃禾研究员所带领的团队在 Cell 上发表了题为 "CLIM-TIME identifies metastatic microenvironment modulators for T cell therapy response" 的研究型论文,核心开发了CLIM-TIME高通量扰动映射平台,首次系统性揭示了抑癌基因(TSG)缺失重塑转移肿瘤微环境(TME)的分子机制,鉴定出LOXL2为转移性免疫抑制微环境的关键调控因子,并构建了免疫治疗响应的预测模型,为实体瘤 T 细胞治疗的优化提供了全新的靶点和策略,是肿瘤免疫微环境与精准免疫治疗领域的重要突破。

👆点击阅读全文

核心创新——
CLIM-TIME 平台,实现基因与空间 TME 的精准映射
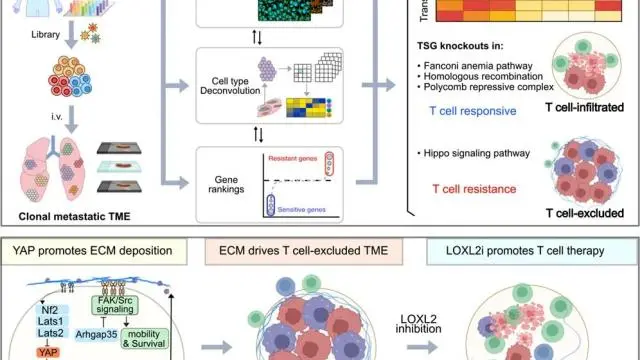
研究团队整合CRISPR 基因筛选、激光捕获显微切割(LCM)、空间转录组、免疫荧光等多项技术,开发出全新的CLIM-TIME 平台,实现了单细胞分辨率下高通量的 “基因扰动 - 空间 TME 表型” 关联分析。
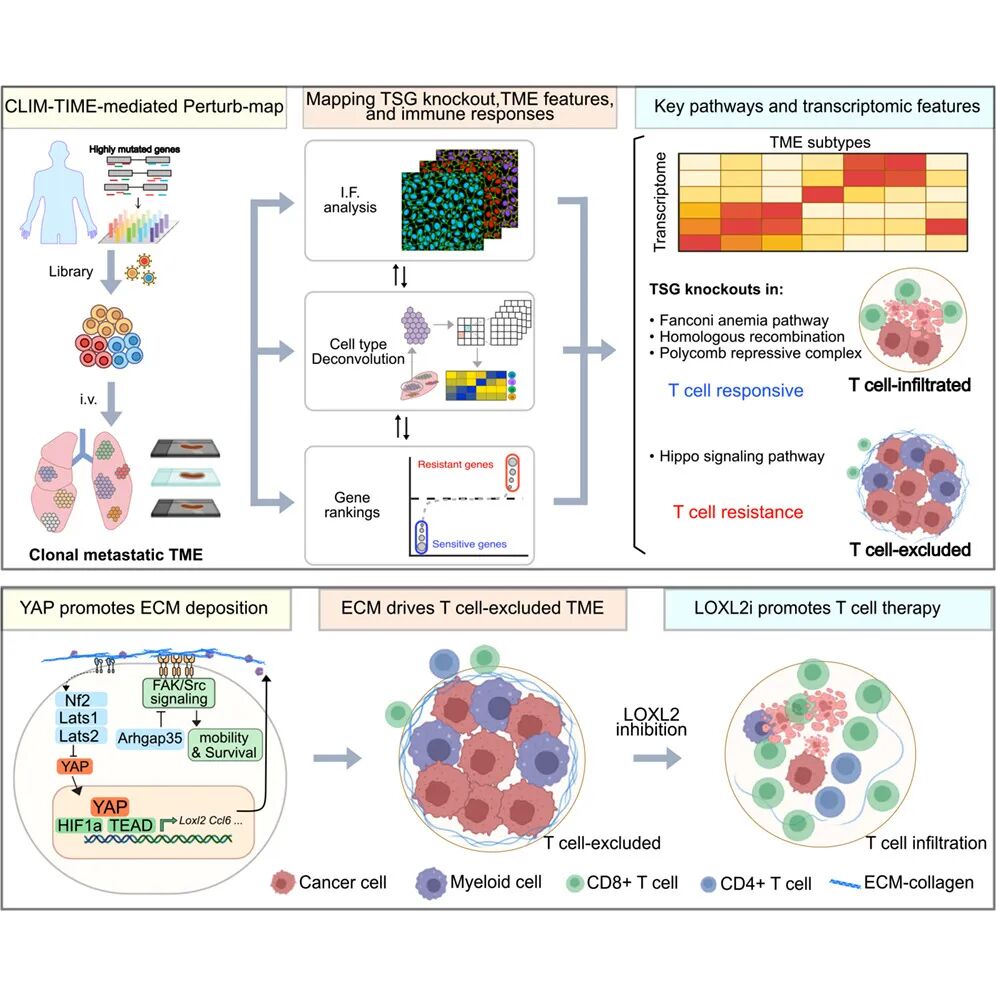

关键发现——
抑癌基因缺失的 “通路特异性”,决定 TME 亚型与治疗响应
借助 CLIM-TIME 平台,研究团队对 360 个抑癌基因缺失后的转移性 TME 进行了系统性分析,鉴定出 7 种转移性 TME 亚型,分 “敏感型” 和 “耐药型”,并通路特异性决定治疗响应,分析出Hippo 通路是耐药核心。
接着,研究团队以 Hippo 通路核心抑癌基因Nf2为模型,深入解析了耐药型 TME 的形成机制,发现Hippo-YAP-LOXL2-ECM-FAK轴是塑造免疫抑制微环境的核心分子链。

临床转化——
LOXL2 为实体瘤免疫治疗的可药靶点,构建高精度预测模型
研究团队针对 LOXL2 开展了一系列干预实验,证实其为实体瘤免疫治疗的全新潜力靶点。首先,通过基因敲除、LOXL2 催化位点突变(Y689F)、小分子抑制剂(PXS5505)三种方式抑制 LOXL2,发现均能逆转免疫抑制;接着发现联用 LOXL2 抑制,能够增强多癌种 T 细胞治疗效果;最后,使用LOXL2 介导的 ECM 交联会激活 FAK 信号通路,研究发现 FAK 抑制剂(VS4718)可模拟 LOXL2 抑制的效果。
TargetMol 科研助力
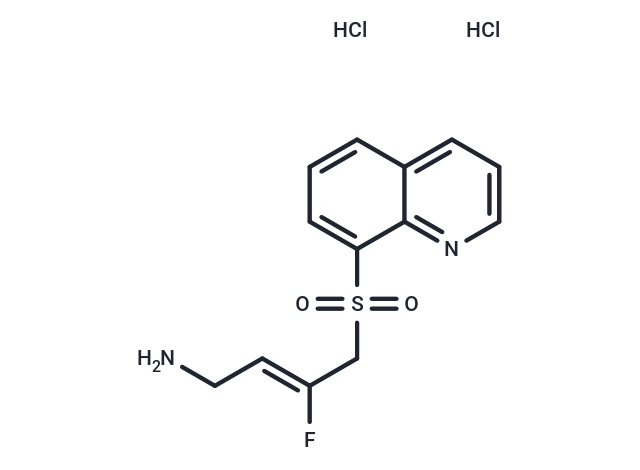
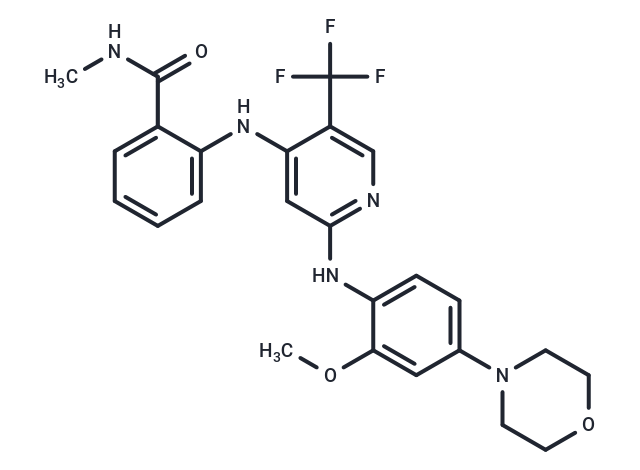

总结
不仅开发了创新性的 CLIM-TIME 技术平台,更重要的是揭示了 Hippo-YAP-LOXL2 轴调控转移性 TME 的核心机制,鉴定出 LOXL2 这一潜力靶点,并构建了高精度的免疫治疗响应预测模型,为实体瘤免疫治疗的优化提供了从基础研究到临床转化的完整解决方案。
其他文章

订阅TargetMol新闻
科学新闻、观点和分析的重要汇总,每个工作日都会发送到您的收件箱.




 |
|