 您的购物车当前为空
您的购物车当前为空
TargetMol天然产物——Bleomycin Sulfate(Cat. No. T6116, CAS. 9041-93-4),切割DNA的剪刀
1. 产品介绍
Bleomycin Sulfate,货号T6116,CAS号9041-93-4,别名硫酸博莱霉素、硫酸博来霉素、NSC125066、Blenoxane。Bleomycin Sulfate是一种糖肽类抗生素,具有抗肿瘤活性,是常用的DNA损伤剂和DNA合成抑制剂。它通过引起DNA链断裂而不影响RNA链,从而发挥作用。Bleomycin Sulfate常用于抗肿瘤研究,也被广泛应用于建立肺纤维化动物模型。
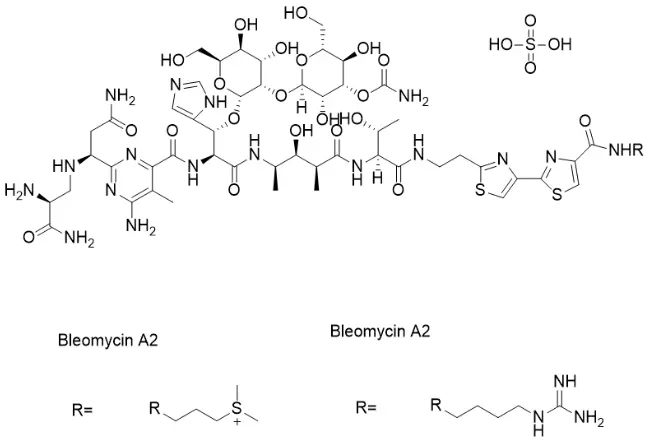
Bleomycin Sulfate分子结构式
2. 背景介绍
许多抗肿瘤药物的作用靶点往往是细胞内关键的生物大分子或信号通路,其失调会导致细胞增殖失控、凋亡抑制等肿瘤特征。其中,DNA作为细胞分裂和基因表达的核心载体,是极具杀伤力的抗肿瘤药物靶点。DNA破坏型药物通过与DNA结合、引发链断裂或交联,干扰DNA复制与转录,从而阻止肿瘤细胞增殖并诱导其死亡。此类策略在临床上应用广泛,主要利用肿瘤细胞分裂活跃、对DNA损伤敏感的特性实现疗效。其典型代表包括烷化剂、铂类化合物及抗肿瘤抗生素(如放线菌素等),它们通过不同的化学反应方式直接破坏DNA结构,进而激发细胞应激反应并诱导凋亡[1]。
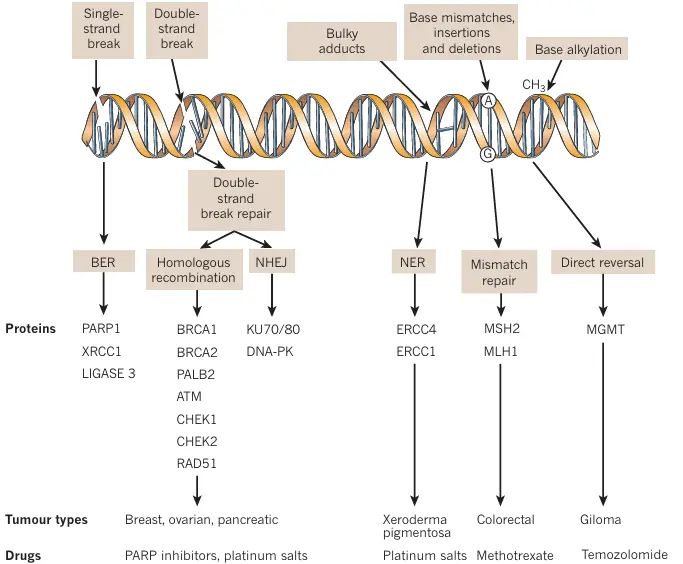
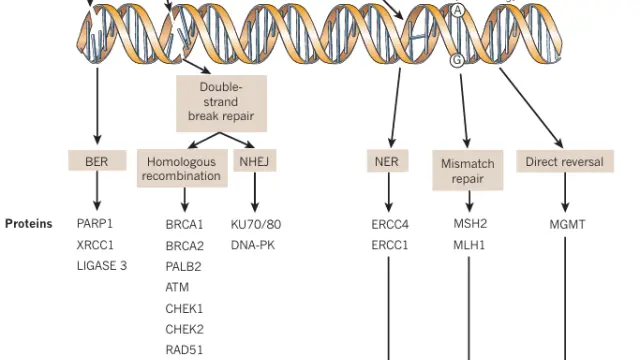
多种DNA修复机制维持着基因组的稳定性[1]
Bleomycin Sulfate是一类糖肽类抗生素,对多种淋巴瘤、头颈癌和生殖细胞肿瘤具有强效的抗肿瘤活性。博来霉素的治疗效果受肺纤维化的发生限制。博来霉素的细胞毒性和诱变效应被认为与其介导单链和双链DNA损伤的能力有关,这需要特定的辅因子(过渡金属、氧气和单电子还原剂)的存在。对博来霉素治疗效果机制及其生物合成途径的理解进展,为开发更强效、毒性更低的治疗药物奠定了基础[2]。
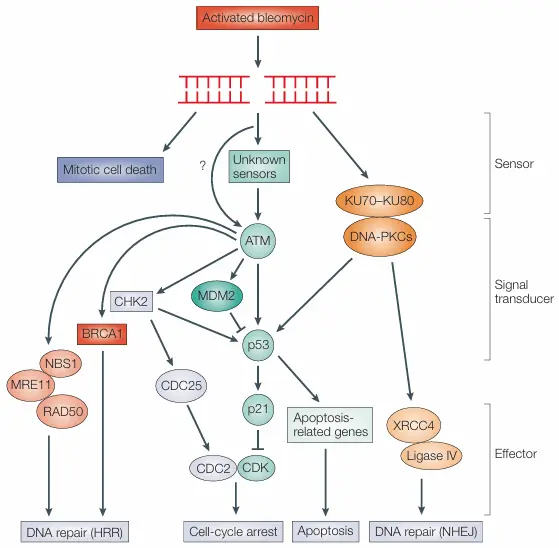
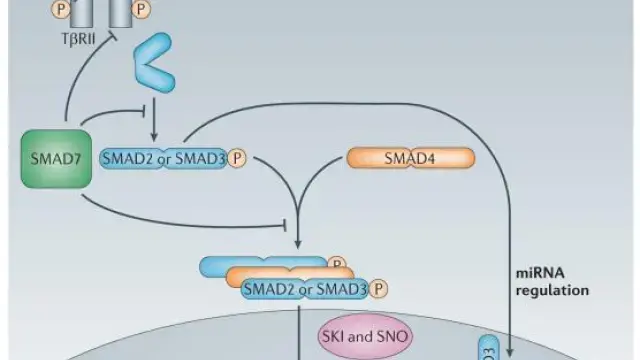
细胞内对Bleomycin损伤的反应网络[2]
3. 应用文献精选
文章标题:ROS-mediated lysosomal membrane permeabilization and autophagy inhibition regulate bleomycin-induced cellular senescence

研究概览:
该研究探究了Bleomycin(博来霉素)诱导的细胞衰老机制,Bleomycin活化过程中产生的活性氧(ROS)通过诱导溶酶体膜通透(lysosomal membrane permeabilization, LMP)并阻碍溶酶体降解,从而阻碍自噬通量。通过体外细胞模型发现,Bleomycin处理显著提升细胞内ROS水平,进而触发溶酶体膜破裂,使溶酶体内的蛋白酶释放至胞质,导致溶酶体功能障碍。同时,ROS过量及LMP事件抑制了自噬通量,使受损细胞器和代谢废物无法被有效清除,形成持续的细胞应激状态。该研究揭示了Bleomycin诱导细胞衰老并非仅依赖其经典的DNA断裂作用,而是通过ROS介导的溶酶体稳态破坏与自噬失衡协同放大损伤信号,为理解Bleomycin的细胞毒性及其在纤维化、衰老相关疾病模型中的作用机制提供了新的分子层面证据[3]。
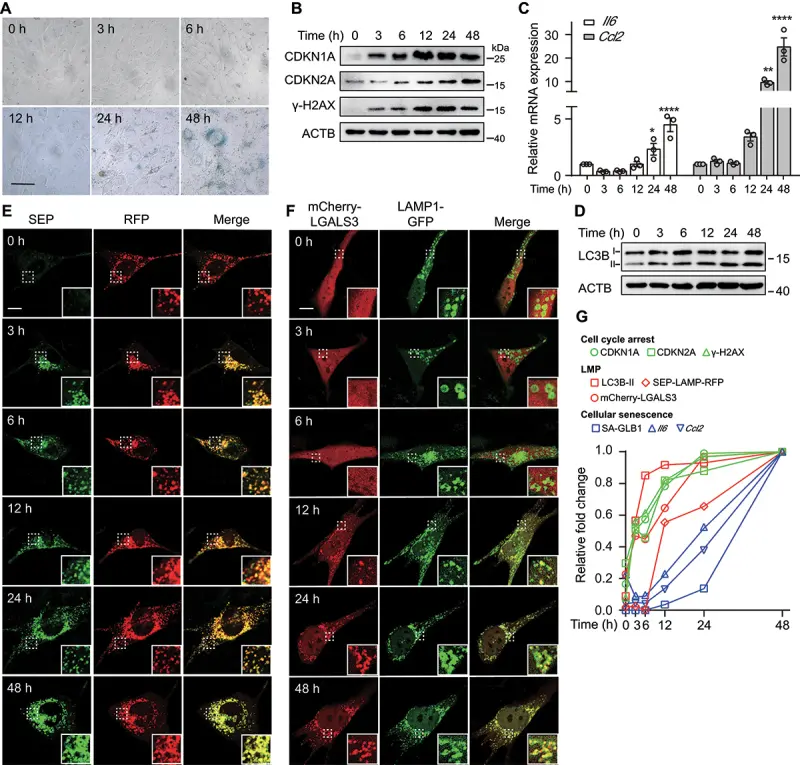
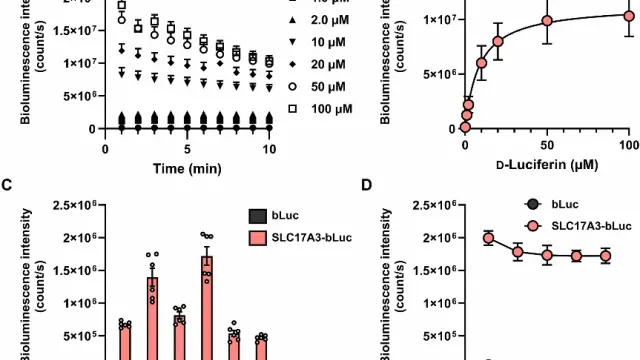
Bleomycin诱导的LMP和自噬缺陷先于细胞衰老[3]
文章标题:Asparaginase and Autophagy Inhibitors Effectively Remove Senescent Cells by Synergistically Limiting Asparagine Supply

研究概览:
该研究探讨了通过代谢限制与自噬抑制协同清除衰老细胞(senescent cells)的新策略。研究发现,衰老细胞在代谢层面高度依赖天冬酰胺(asparagine)以维持蛋白质稳态和存活能力,而外源性天冬酰胺的供给在其中起关键作用。利用天冬酰胺酶(Asparaginase)耗竭细胞外天冬酰胺的同时,联合自噬抑制剂阻断细胞通过自噬途径回收氨基酸的能力,能够在双重层面限制衰老细胞的天冬酰胺来源。实验结果表明,这种“营养剥夺 + 自噬阻断”的协同干预显著降低了衰老细胞的存活率,而对正常细胞影响较小。机制上,该策略导致蛋白质合成受阻、代谢应激加剧及细胞内氨基酸稳态崩溃,最终选择性诱导衰老细胞死亡。该研究提出了一种基于代谢脆弱性的潜在衰老细胞清除(senolytic)策略,为衰老相关疾病的干预提供了新的实验依据[4]。
在该研究中,Bleomycin(Cat. No. T6116)被作为构建氧化应激-DNA损伤型细胞衰老模型的工具药物,用于揭示溶酶体稳态与自噬失衡在衰老发生中的机制作用。研究者利用Bleomycin作为经典的DNA损伤与氧化应激诱导药物,在体外细胞模型中稳定触发ROS过量产生和DNA断裂,从而建立可重复的衰老模型。
4. 参考文献
[1] Lord CJ, Ashworth A. The DNA damage response and cancer therapy. Nature. 2012 Jan 18;481(7381):287-94. doi: 10.1038/nature10760
[2] Chen J, Stubbe J. Bleomycins: towards better therapeutics. Nat Rev Cancer. 2005 Feb;5(2):102-12. doi: 10.1038/nrc1547
[3] Qi Z, Yang W, Xue B, Chen T, Lu X, Zhang R, Li Z, Zhao X, Zhang Y, Han F, Kong X, Liu R, Yao X, Jia R, Feng S. ROS-mediated lysosomal membrane permeabilization and autophagy inhibition regulate bleomycin-induced cellular senescence. Autophagy. 2024 Sep;20(9):2000-2016. doi: 10.1080/15548627.2024.2353548. Epub 2024 May 18. PMID: 38762757; PMCID: PMC11346523.
[4] Huang Z, Liu X, Zhou X, Chen K, Diao H, Wang M, Wei J, Li Z, Yang Y, Mao Z, Yu W. Asparaginase and Autophagy Inhibitors Effectively Remove Senescent Cells by Synergistically Limiting Asparagine Supply. Aging Cell. 2025 Oct;24(10):e70203. doi: 10.1111/acel.70203





 |
|