- 全部删除
 您的购物车当前为空
您的购物车当前为空

- 具有直观的搜索结果
- 更便捷高效地比较产品细节
- 快速、简洁的提交订单
- 成为我们TargetMol的一员,阅读和提交您的产品建议和意见
我们很想知道您的意见反馈,所以我们在每个页面上都梳理出一个反馈按钮。
人类的三个Ras基因,HRAS、KRAS和NRAS,在三分之一的人类癌症中频繁发生突变,其中KRAS突变是三个亚型中最为普遍的(约86%的病例)。由于KRAS的高突变频率以及其在推动人类肿瘤发生和对癌症治疗的抵抗中的关键作用,我们迫切需要寻找能够抑制突变型(mt)KRAS的药物。
随着科学技术的不断突破,我们已经发现了可与 mt KRAS G12C 形成共价结合的小分子,例如 sotorasib 和 adagrasib,这些药物已被用于治疗携带 KRAS G12C 突变的晚期非小细胞肺癌(NSCLC)患者。此外,我们还发现了能够结合 KRAS G12D 的 MRTX1133。然而,目前仍然没有临床批准的用于治疗 KRAS G12D 突变的药物(MRTX1133详情可见往期:TargetMol明星分子——MRTX1133)。
近日,一项发表于 Cancer Research Communications 的研究给我们带来了惊喜,来自 VCU 梅西综合癌症中心的研究团队发现了可靶向 KRAS G12D 的新型药物 KRB-456,能够有效阻止携带 mt KRAS G12D 和 G12V 的胰腺癌患者在化疗和放疗后复发后的皮下和异种移植瘤的体内生长,有望走向临床。

▲点击图片可跳转原文
发现KRB-456
在最新研究中,为了寻找能够结合 mt KRAS G12D 的小分子,研究人员首先使用 AlphaScreen 筛选出了能够干扰 KRAS G12D 与 RAF1 的 RBD(RAS结合结构域)结合的化合物。其中有6个(IB-21G、IB-21L、IIA-15D、IB-21J、IB-5I 和 IIA-13L)显著抑制了 GTP-KRAS G12D 与 GST-RBD 的结合(77% 至 100% 的抑制)。
在这 6 个化合物中,有 4 个(IB-21G、IB-21L、IIA-15D 和 IB-21J)共享相同的药效团,在抑制 KRAS G12D 与 GST-RBD 结合方面最为有效(98%至100%的抑制)。另外两个化合物,IB-5I 和 IIA-13L,具有不同的药效团,分别为 89% 和 77% 的抑制率。

▲KRB-456的筛选
进一步的 GST pull-down 分析显示,化合物 IB-21L(以下简称为KRB-456)是抑制 KRAS G12D/GST-RBD 相互作用最有效的化合物,IC50 值为 260 nM。

▲GST pull-down 分析结果
为更好地了解 KRB-456 与 KRAS G12D 的结合相互作用,研究人员进行了 2D 1H-15N 异核单量子相干(HSQC)NMR 分析,使用 15N 标记的 KRAS G12D 结合 GDP 和不可水解的 GTP 核苷酸类似物 GCP(β,γ-Methyleneguanosine 5′-triphosphate)。结果显示 KRB-456 通过与 switch-I/II 区域内的一个动态变构结合口袋形成相互作用来结合 KRAS G12D。
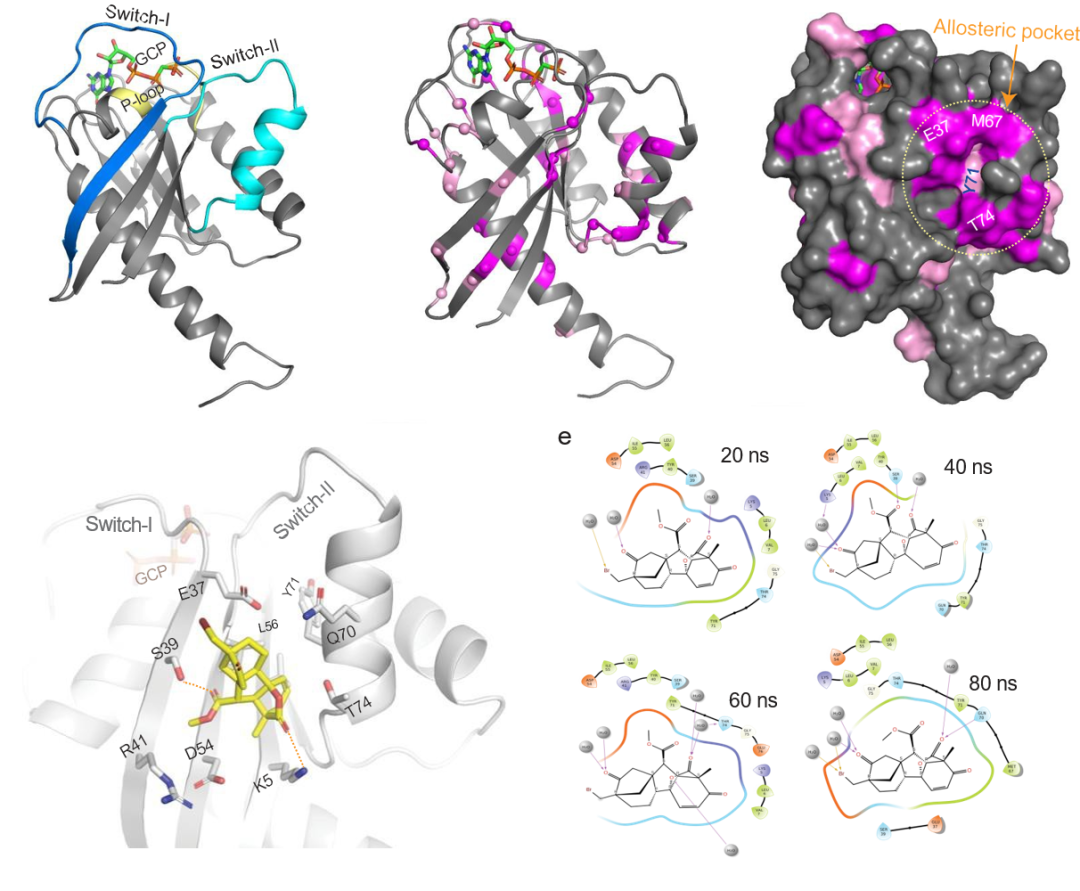
▲KRB-456与KRAS G12D的结合
接下来,研究人员通过使用4名胰腺癌患者的新鲜活检组织确定了 KRB-456 是否能够抑制小鼠中患者源异种移植物(PDX)的生长,其中 3 名患者(G166、G148 和 G160)的肿瘤携带 KRAS G12D 突变,另一名患者(G174)的肿瘤携带 KRAS G12V 突变。
通过将所有 4 名患者的新鲜切除的肿瘤活检皮下(s.c.)植入 NSG 小鼠,并将随即小鼠分为对照组和 KRB-456 组。结果显示,在所有 KRB-456 处理的小鼠中,肿瘤生长在治疗的第 3 天就被显著抑制,到 KRB-456 药物治疗结束时,平均生长仅为52%、177%、300% 和 413%,相比之下,对照组分别为 401%、433%、802%和 791%。KRB-456 显著抑制了胰腺癌患者 PDX 在小鼠皮下植入的肿瘤生长。
进一步,研究人员将患者 G160 的肿瘤活检在 NSG 小鼠中原位植入来确定 KRB-456 是否也能抑制原位肿瘤模型的生长(G160在原位植入时生长速度比皮下植入慢得多)。在肿瘤植入 20 天后,小鼠每天用 KRB-456 进行腹腔注射治疗 ,发现 KRB-456 治疗抑制了患者 G160 原位植入的PDX的生长。证明了 KRB-456 不仅在皮下 PDX 肿瘤生长中有效,而且在源自胰腺癌患者的肿瘤原位生长中也有效,KRB-456 以剂量依赖的方式抑制了这些胰腺癌细胞的生存能力,抑制效果可达到 70%。
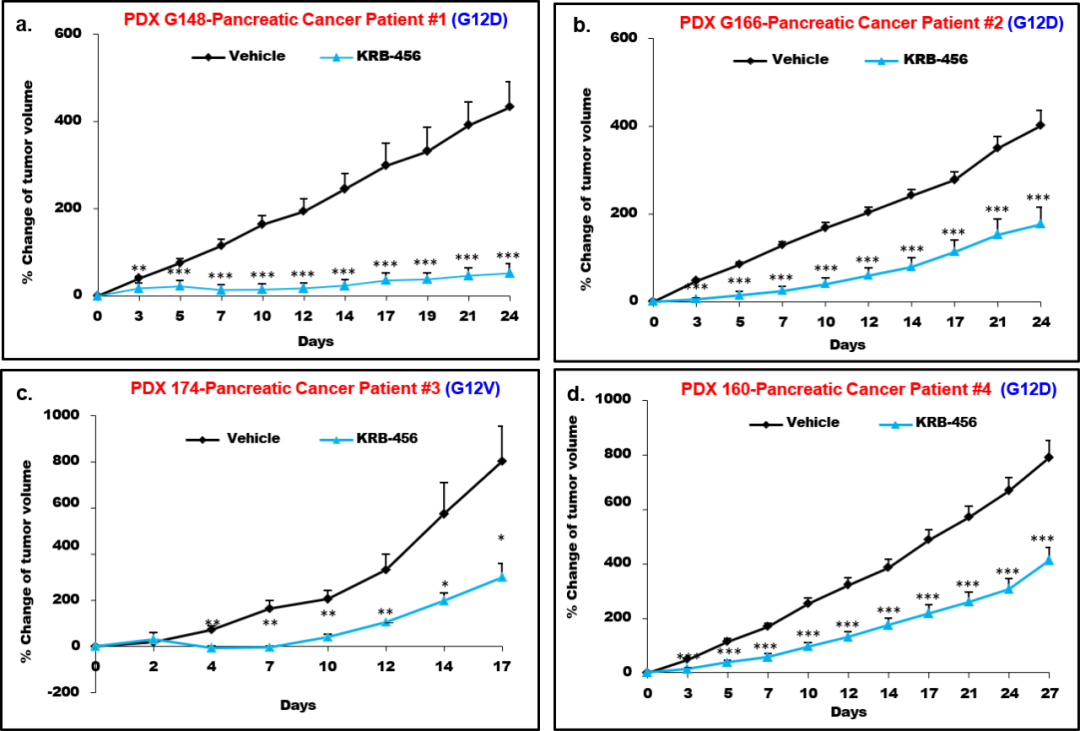
▲KRB-456 对肿瘤的抑制效果
此外, 3D 共培养模型显示,当患者来源的肿瘤细胞单独培养或与促进化疗抵抗的人类胰腺星形细胞共培养时,KRB-456 仍然能以剂量依赖的方式显著抑制这些胰腺癌细胞的生存能力。
总结
综上,该研究首次发现了一种名为 KRB-456 的新型小分子,它能够与 KRAS G12D 形成高亲和力结合,通过作用于 KRAS 蛋白的动态异构性结合口袋,抑制其与 RAF1 的结合,从而有效阻断胰腺癌细胞的 KRAS G12D 介导的肿瘤生长。
KRB-456 在体外和体内研究中表现出优越的抗肿瘤活性,不仅能够显著减少 GTP 结合的 KRAS 水平,还能抑制 P-MEK 的活性,引起细胞凋亡。实验证明 KRB-456 对携带 KRAS G12D 和 KRAS G12V 突变的胰腺癌病人源肿瘤模型均具有显著的抑制效果,尤其对于那些经过化疗和放疗后复发的患者的肿瘤生长,显示出潜在的克服药物耐受性的能力。此外,KRB-456 在 3D 共培养模型中显示出对胰腺癌患者源肿瘤细胞的显著抗活性,为该分子在克服化疗和放疗耐受性方面的临床应用提供了重要线索。总体而言,这项研究为寻找更广泛的 KRAS 突变型抑制剂提供了新思路,尤其是针对 KRAS G12D 和 KRAS G12V,为治疗胰腺癌等高发癌症开辟了新的治疗途径。
此外,该研究中提到的化合物sotorasib 、adagrasib和 MRTX1133 等 TargetMol 都可以提供噢,还有 抗胰腺癌化合物库、抗肿瘤筛选化合物库 等可供选择,有任何问题欢迎私信咨询~





原文文献:
Kazi A, Ranjan A, Kumar M V V, et al. Discovery of KRB-456, a KRAS G12D switch-I/II allosteric pocket binder that inhibits the growth of pancreatic cancer patient-derived tumors. Cancer Res Commun. Published online December 5, 2023. doi:10.1158/2767-9764.CRC-23-0222
其他文章


订阅TargetMol新闻
科学新闻、观点和分析的重要汇总,每个工作日都会发送到您的收件箱.

 嗨!有任何问题?点我咨询
嗨!有任何问题?点我咨询

版权所有©2015-2025 TargetMol Chemicals Inc.保留所有权利.
沪ICP备20019793号-4 | 沪公网安备 31010602006700号 | 沪(静)应急管危经许[2024]203441
| 沪(静)应急管危经许[2024]203441