 您的购物车当前为空
您的购物车当前为空
TargetMol天然产物——3-Methyladenine(Cat. No. T1879, CAS. 5142-23-4),调控自噬通量的开关
1. 产品介绍
3-Methyladenine,货号T1879,CAS号5142-23-4,别名NSC 66389、3-甲基腺嘌呤、3-MA。3-Methyladenine(3-MA)是一种PI3K抑制剂,选择性抑制IB类PI3Kγ(IC50=60 μM)和III类VPS34(IC50=25 μM)。3-Methyladenine具有自噬抑制活性。
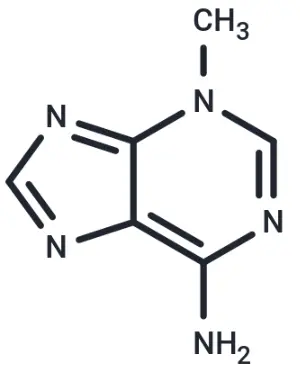
3-Methyladenine分子结构式
2. 背景介绍
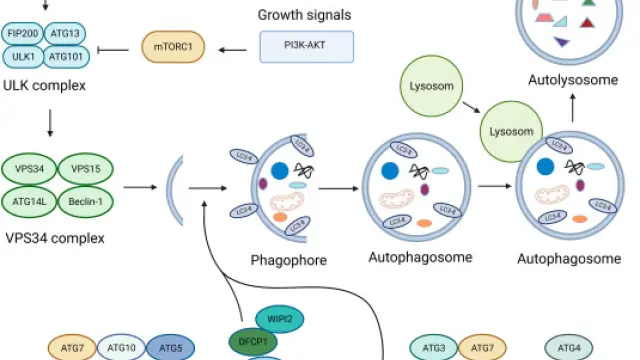
自噬(autophagy)是细胞内高度保守的降解途径,通过形成自噬体并与溶酶体融合,实现受损细胞器、蛋白质以及细胞内大分子的降解和再利用,是维持细胞稳态和应对胁迫的重要机制。该过程包括隔膜起始、延长与闭合、自噬体的形成与成熟以及与溶酶体融合等多个步骤,由一系列自噬相关基因(ATG)编码的蛋白参与调控。哺乳动物细胞中,自噬受营养、能量和应激信号调控,AMPK、mTORC1等信号通路成为核心调节节点,其中经典的宏自噬路径是启动细胞器与大分子包裹形成自噬体的过程。自噬在多种生理和病理过程中发挥关键作用,如细胞存活、免疫反应、神经退行性疾病、肿瘤发生发展等,因此相关分子靶点成为潜在的治疗干预点。PI3K家族中的III类PI3K(VPS34)作为自噬起始阶段的重要酶,参与磷脂酰肌醇3-磷酸生成,从而驱动隔膜膜片(phagophore)形成,是自噬过程的重要调控靶点之一[1]。
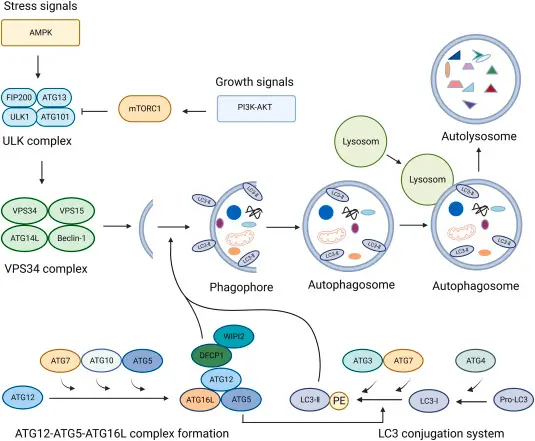
自噬发生的流程图[1]
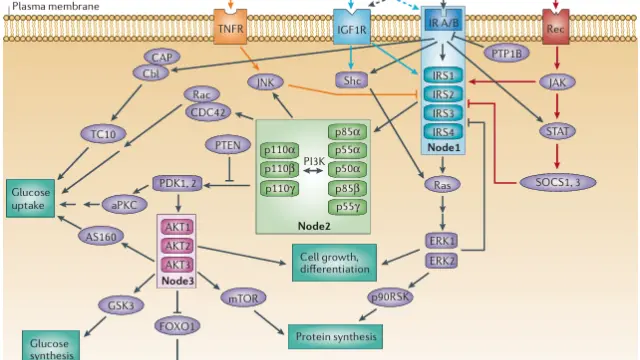
3-甲基腺嘌呤(3-Methyladenine,3-MA)是一种经典的自噬抑制剂,主要通过靶向PI3K家族中的III类PI3K(即VPS34)来抑制自噬的发生。3-Methyladenine能抑制VPS34的脂质激酶活性,阻断PI(3)P的合成,从而干扰自噬隔膜的形成及自噬体的起始阶段,导致自噬通量下降。此外,3-Methyladenine对I类PI3K也有一定的抑制活性,这种双重靶向特性使其在研究PI3K/Akt/mTOR信号轴与自噬之间的互作时成为常用工具化合物。通过抑制VPS34介导的自噬起始,3-Methyladenine常被用于体外和体内模型中探究自噬在细胞存活、代谢调控、肿瘤药物敏感性等过程中的作用,并作为验证自噬依赖性表型的化学干预手段[2]。
3. 应用文献精选
文章标题:Inhibition of autophagy with 3-methyladenine is protective in a lethal model of murine endotoxemia and polymicrobial sepsis

研究概览:
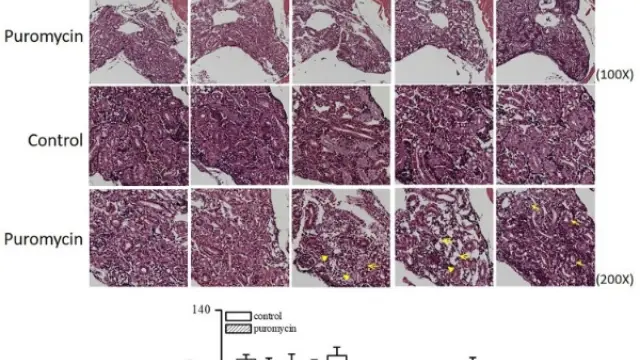
该研究在小鼠体内建立了两种致死性全身炎症模型——LPS诱导的内毒素血症模型和盲肠结扎穿刺(CLP)诱导的多菌性脓毒症模型,系统评估了经典自噬抑制剂3-Methyladenine(3-MA)对疾病进程和生存结局的影响。研究发现,在这两种炎症性休克模型中,自噬水平显著上调,而通过腹腔注射3-Methyladenine抑制自噬后,小鼠的生存率明显提高,伴随炎症因子水平下降、器官损伤减轻及组织病理学改善。机制上,作者证实3-Methyladenine通过抑制VPS34依赖的自噬起始过程,减弱过度炎症反应和细胞损伤,提示在严重感染和脓毒症过程中,自噬并非单纯的保护机制,过度激活反而可能加剧病理损伤。该研究首次在体内系统证实了抑制自噬在致死性脓毒症模型中的保护作用,为理解自噬在炎症性疾病中的双重角色及其作为潜在治疗靶点提供了重要实验依据[3]。
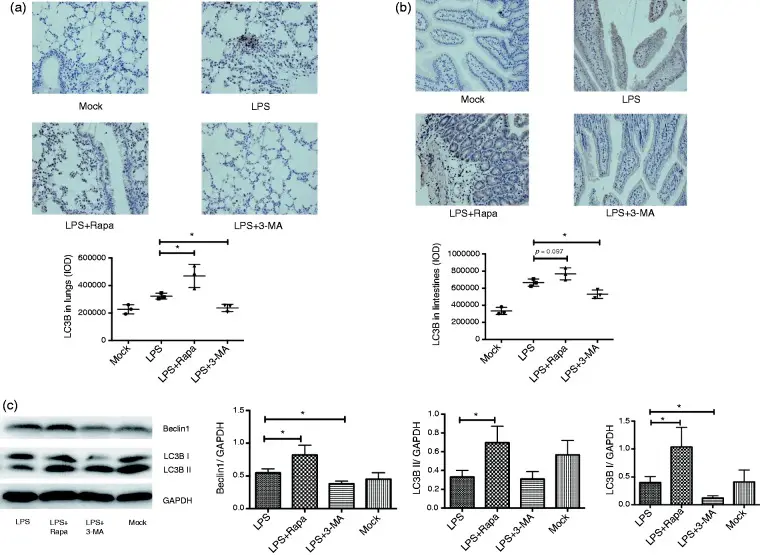
在内毒素休克小鼠中,LPS联合自噬抑制剂3-Methyladenine或LPS联合雷帕霉素分别抑制或增强自噬[3]
文章标题:Modulation of O-GlcNAc cycling influences α-synuclein amplification, degradation, and associated neuroinflammatory pathology

研究概览:
该研究系统探讨了在细胞与小鼠模型中调控O-GlcNAc糖基化循环(由O-GlcNAc转移酶OGT和O-GlcNAcaseOGA媒介)对病理性α-突触核蛋白(α-synuclein)聚集、扩散、降解及相关神经炎症反应的影响。研究者通过向小鼠纹状体或神经/小胶质细胞共同培养体系中注入不同构象的α-syn预成纤维,并结合药理学或基因方法抑制OGT或OGA活性,发现调控O-GlcNAcylation水平显著改变α-syn的聚集程度及其向相邻细胞和连接脑区的传播,同时也影响多巴胺能神经元退行性变、NLRP3介导的神经炎症反应和行为缺陷。在这一过程中,病理性α-syn传播使受体细胞O-GlcNAc水平降低且OGT表达减少,而抑制OGA提高O-GlcNAcylation则缓解α-syn相关病理并促进其通过自噬-溶酶体途径降解[4]。
在该研究中,3-Methyladenine(Cat. No. T1879)被作为经典自噬抑制剂使用,用于验证α-synuclein的清除是否依赖自噬-溶酶体途径。作者在细胞模型中通过药理学手段加入3-Methyladenine抑制VPS34依赖的自噬起始过程,随后观察α-syn聚集体的降解变化。
4. 参考文献
[1] Liu Y, Yang Q, Chen S, Li Z, Fu L. Targeting VPS34 in autophagy: An update on pharmacological small-molecule compounds. Eur J Med Chem. 2023 Aug 5;256:115467. doi: 10.1016/j.ejmech.2023.115467
[2] Klionsky DJ, Abdelmohsen K, Abe A, et al. Guidelines for the use and interpretation of assays for monitoring autophagy (3rd edition). Autophagy. 2016;12(1):1-222. doi: 10.1080/15548627.2015.1100356
[3] Li Q, Li L, Fei X, Zhang Y, Qi C, Hua S, Gong F, Fang M. Inhibition of autophagy with 3-methyladenine is protective in a lethal model of murine endotoxemia and polymicrobial sepsis. Innate Immun. 2018 May;24(4):231-239. doi: 10.1177/1753425918771170. Epub 2018 Apr 19. PMID: 29673286; PMCID: PMC6830927.
[4] Miao Y, Zhang T, Ma Z, Du H, Gu Q, Jiang M, Xiong K, Liu CF, Meng H. Modulation of O-GlcNAc cycling influences α-synuclein amplification, degradation, and associated neuroinflammatory pathology. Mol Neurodegener. 2025 Oct 27;20(1):113. doi: 10.1186/s13024-025-00904-2





 |
|