 您的购物车当前为空
您的购物车当前为空
TargetMol多肽——Insulin(human)(Cat. No. T8221, CAS. 11061-68-0),细胞能量大门的钥匙
1. 产品介绍
Insulin(human),货号T8221,Cas号11061-68-0,别名胰岛素、INSULIN。Insulin(human)是一种多肽激素,可以促进糖原的合成,调节血液中的葡萄糖水平。Insulin(human)具有降血糖活性,临床上用于治疗糖尿病患者的高血糖。
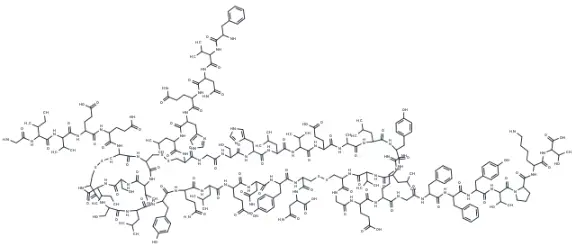
Insulin(human)分子结构式
2. 背景介绍
在代谢性疾病研究中,胰岛素受体(Insulin Receptor, IR)及其下游信号通路是重要的药物靶点。胰岛素受体是一种跨膜受体酪氨酸激酶(receptor tyrosine kinase),由α、β两个亚基组成,分布于肝脏、肌肉、脂肪等组织细胞膜上。当胰岛素与受体结合时,可诱导受体自身酪氨酸激酶活性的激活,进而磷酸化胰岛素受体底物(IRS)等效应分子,触发PI3K/AKT、MAPK等信号传导级联反应。这些通路共同调控葡萄糖摄取、糖原合成、脂质代谢及细胞增殖。在人类2型糖尿病及胰岛素抵抗状态中,IR信号通路功能受损,导致外周组织对胰岛素的反应性下降,是当前代谢性疾病药物开发的关键靶标之一[1]。
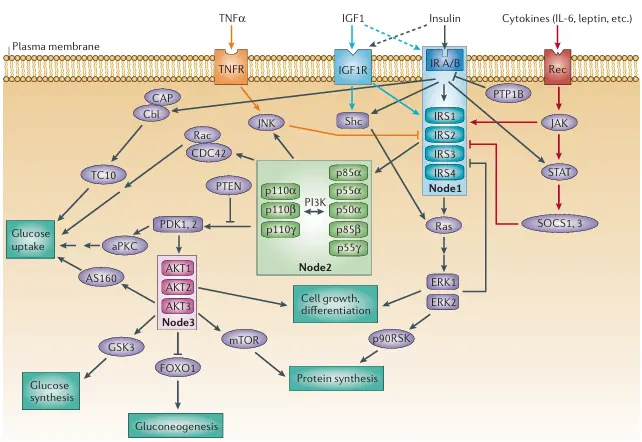
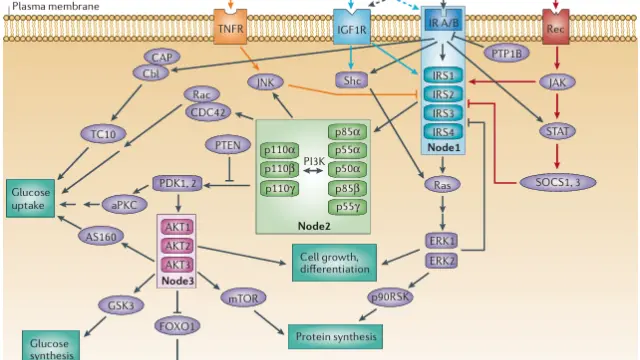
胰岛素信号网络中的关键节点[1]
Insulin(胰岛素)作为主要的代谢激素,其生物学效应主要通过与胰岛素受体结合并激活下游信号通路实现。在靶细胞膜上,胰岛素与受体结合后,促使受体的酪氨酸激酶结构活化,使受体自身及IRS蛋白发生酪氨酸磷酸化。随后,磷酸化的IRS能招募并激活PI3K(磷脂酰肌醇3-激酶),该激酶进一步激活AKT(蛋白激酶B)。AKT活化是调节葡萄糖运输、糖原合成与脂质代谢的核心枢纽。例如,AKT促进GLUT4转运体从细胞内囊泡转运至细胞膜,增强肌肉和脂肪组织对葡萄糖的摄取;同时AKT抑制肝脏糖异生,促进糖原合成。此外,胰岛素还通过MAPK通路影响基因表达和细胞增殖。正常情况下,这一机制确保血糖稳态;而在胰岛素抵抗状态下,这些信号级联被削弱,从而导致高血糖和代谢异常。因此深入理解胰岛素信号网络,对于开发改善胰岛素敏感性的新治疗方法至关重要[2]。
3. 应用文献精选
文章标题:Restoration of Insulin receptor improves diabetic phenotype in T2DM mice

研究概览:
该研究通过在2型糖尿病小鼠模型中恢复胰岛素受体(IR)表达与功能,验证了IR水平对糖代谢稳态的决定性作用。采用基因递送与组织特异性调控策略,在Insulin抵抗背景下提升关键代谢组织中的IR表达,随后结合葡萄糖耐量试验、Insulin耐量试验及分子信号检测,系统评估代谢表型变化。结果显示,IR的恢复显著增强了IRS–PI3K–AKT信号通路活性,促进外周组织葡萄糖摄取并抑制肝脏糖异生,从而有效改善高血糖和Insulin抵抗表型。该研究从因果层面证明了胰岛素受体功能下降是T2DM发生发展的关键驱动因素,并提示通过提升IR功能或表达水平可能成为治疗2型糖尿病的新策略[3]。
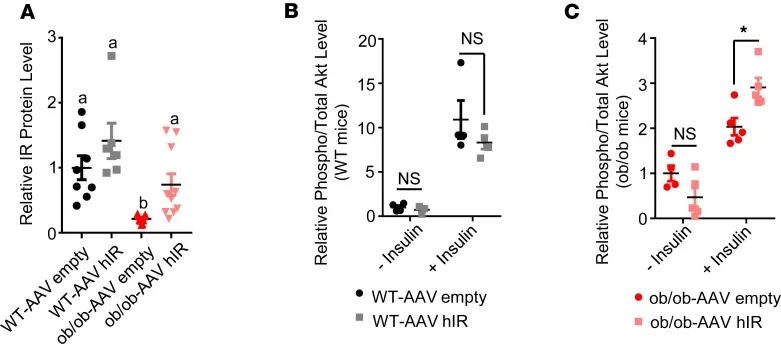
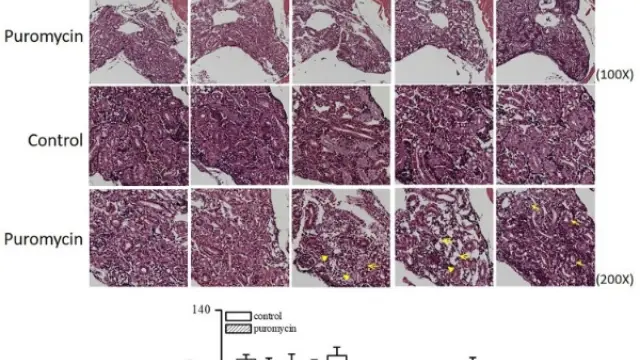
注射AAV-hIR增加了OB/OB小鼠肝脏中的IR蛋白和Insulin刺激的Akt磷酸化[3]
文章标题:Spatially constrained disulfide bond shuffling delays Insulin aggregation and enhances neurotoxicity

研究概览:
该研究聚焦于Insulin(Cat. No. T8221)在异常折叠与聚集过程中的二硫键重排(disulfide bond shuffling, DBS)现象及其生物学后果。研究者通过在分子层面对Insulin二硫键进行空间受限设计与定向改造,构建了一系列限制二硫键重排能力的Insulin变体,并结合体外聚集动力学检测、结构分析与神经细胞毒性实验,系统评估其对蛋白聚集行为与细胞毒性的影响。结果表明,限制二硫键重排可显著延缓Insulin形成淀粉样纤维(amyloid fibrils)的过程,但与此同时却增强了聚集前期寡聚体对神经细胞的毒性。该研究揭示了控制胰岛素中DBS在治疗应用中的重要性,并提供了关于二硫键动力学在蛋白质聚集和细胞毒性中的作用的见解,这对胰岛素和更广泛的蛋白质错误折叠环境具有重要意义[4]。
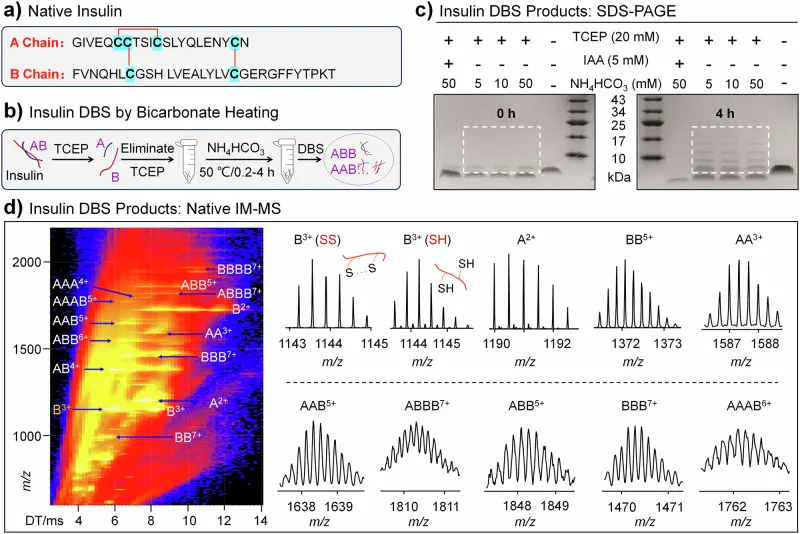
碳酸氢盐加热驱动的Insulin的DBS[4]
4. 参考文献
[1] Taniguchi CM, Emanuelli B, Kahn CR. Critical nodes in signalling pathways: insights into Insulin action. Nat Rev Mol Cell Biol. 2006 Feb;7(2):85-96. doi: 10.1038/nrm1837
[2] Samuel VT, Shulman GI. Mechanisms for Insulin resistance: common threads and missing links. Cell. 2012 Mar 2;148(5):852-71. doi: 10.1016/j.cell.2012.02.017
[3] Wang Y, Zhou H, Palyha O, Mu J. Restoration of Insulin receptor improves diabetic phenotype in T2DM mice. JCI Insight. 2019 Aug 8;4(15):e124945. doi: 10.1172/jci.insight.124945. PMID: 31391336; PMCID: PMC6693840.
[4] Qin W, Li R, Liu J, Liu J, Wang X, Hu B, Zheng Z, Yu Z, Li G. Spatially constrained disulfide bond shuffling delays Insulin aggregation and enhances neurotoxicity. Nat Commun. 2025 Jul 25;16(1):6841. doi: 10.1038/s41467-025-62257-0





 |
|