 您的购物车当前为空
您的购物车当前为空
【TargetMol 明星分子】- Simvastatin: 揭示胆固醇代谢与程序性细胞死亡交叉调控的关键分子
背景介绍:
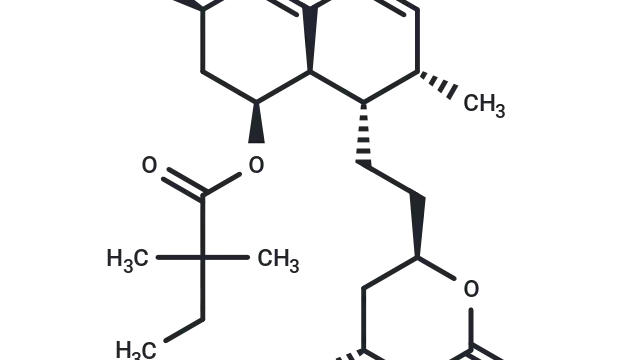
Simvastatin(T0687),CAS: 79902-63-9,是一种高效的HMG-CoA还原酶抑制剂(Ki=0.2 nM),该酶是胆固醇生物合成中限速酶。
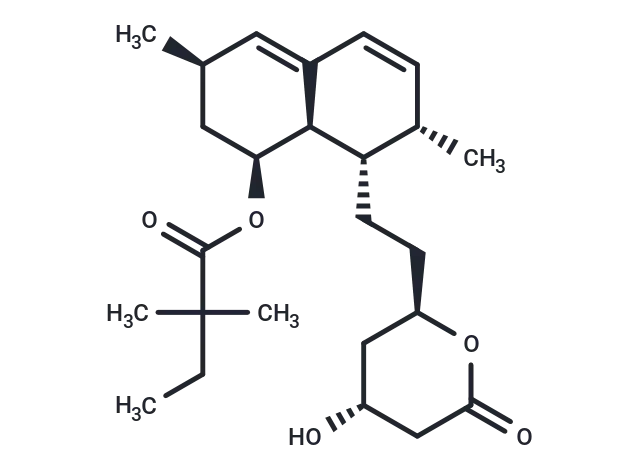
Simvastatin分子结构式
Simvastatin通过竞争性结合HMG-CoA还原酶,显著抑制肝脏胆固醇的合成,从而调节脂质稳态。除其经典的胆固醇代谢调控作用外,Simvastatin还影响多条细胞信号通路,包括凋亡、自噬、铁死亡和线粒体自噬。这些通路在细胞应激反应和代谢调节中具有重要作用。具体而言,Simvastatin通过抑制HMG-CoA还原酶,减少异戊二烯类中间体的合成,这些中间体对于小GTP酶的翻译后修饰至关重要,而小GTP酶参与调控自噬和凋亡信号级联反应。Simvastatin的这种调控作用能够诱导自噬和线粒体自噬,促进细胞通过降解受损细胞器和蛋白质维持稳态,同时增强细胞对铁死亡(一种依赖铁离子并伴随脂质过氧化的程序性细胞死亡形式)的敏感性。Simvastatin与这些信号通路的动态相互作用,使其成为研究脂质代谢与程序性细胞死亡机制交叉调控的重要工具。
在科研领域,Simvastatin广泛用于探讨胆固醇依赖性信号传导及其对细胞命运决策的影响,尤其是在心血管和代谢疾病模型中。此外,Simvastatin调控自噬和铁死亡通路的能力,使其成为研究细胞稳态和应激适应新型调控网络的有力化合物。其对HMG-CoA还原酶的精准靶向及对凋亡和线粒体自噬的下游影响,为体内外研究代谢与细胞死亡信号整合提供了坚实的平台。[1,2]
文献分享:
2.1 Simvastatin inhibits cancer cell growth by inducing apoptosis correlated to activation of Bax and down-regulation of BCL-2 gene expression

Simvastatin (T0687) 在20 µM浓度下作用24至72小时,选择性地诱导癌细胞发生凋亡,而对正常细胞无此作用。Simvastatin诱导的凋亡特征包括DNA断裂增加。在分子水平上,Simvastatin上调促凋亡基因Bax的表达,同时下调具有保护细胞免受凋亡功能的BCL-2基因表达。这些基因表达的变化与癌细胞的凋亡诱导及生长抑制密切相关。此外,Simvastatin的作用可被甲瓦龙酸及其代谢物戊二烯焦磷酸(GGPP)选择性逆转,但胆固醇和法尼基焦磷酸不能逆转药物的效应,表明Simvastatin的作用机制与甲瓦龙酸通路的抑制有关。 [3]
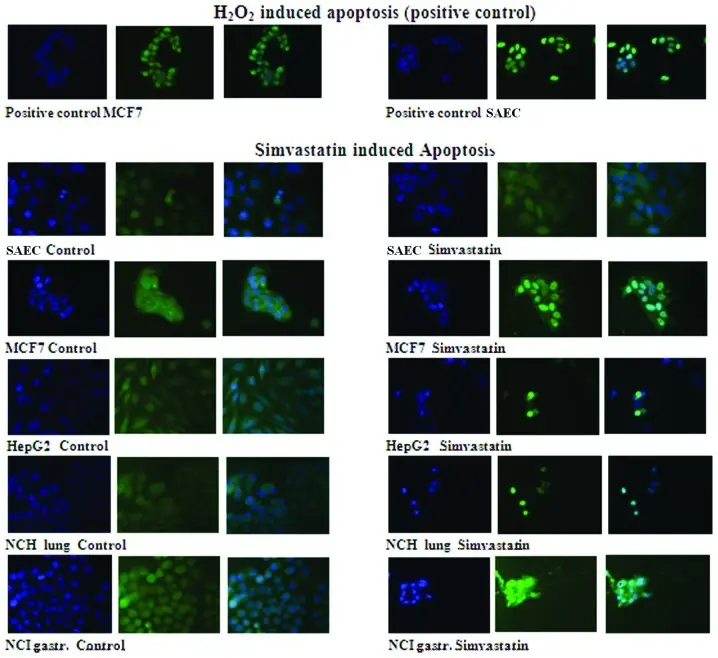
Simvastatin诱导细胞凋亡
2.2 Simvastatin induces cell cycle arrest and inhibits proliferation of bladder cancer cells via PPARγ signalling pathway

Simvastatin (T0687) 在本研究中表现出显著的抑制膀胱癌细胞作用。Simvastatin处理后,在5 μM浓度下,48小时内显著降低了膀胱癌细胞内的中性三酰甘油和脂质含量。MTT检测结果显示,Simvastatin以剂量和时间依赖的方式抑制了膀胱癌细胞的活力和增殖能力,克隆形成实验结果也证实其显著降低了细胞的克隆形成效率。
Simvastatin诱导膀胱癌细胞在G0/G1期发生细胞周期阻滞,其机制为下调细胞周期调控蛋白CDK4、CDK6和Cyclin D1的表达,该过程并未伴随细胞凋亡的显著变化。Simvastatin提高了PPARγ的mRNA及蛋白水平,并增强了PPARγ的DNA结合活性。此外,Simvastatin抑制了膀胱癌细胞的迁移和侵袭,相关EMT(上皮间质转化)相关蛋白包括β-连环蛋白、波形蛋白、N-钙粘蛋白、E-钙粘蛋白、Claudin-1和MMP-2的表达均发生变化。
进一步检测发现Simvastatin处理后,磷酸化AKT和p38水平下降,提示Simvastatin可能通过抑制PI3K/AKT和MAPK/ERK信号通路调控EMT过程。综上,Simvastatin通过调节PPARγ信号通路及其下游信号,抑制膀胱癌细胞的增殖、迁移和侵袭,并诱导细胞周期阻滞。[4]
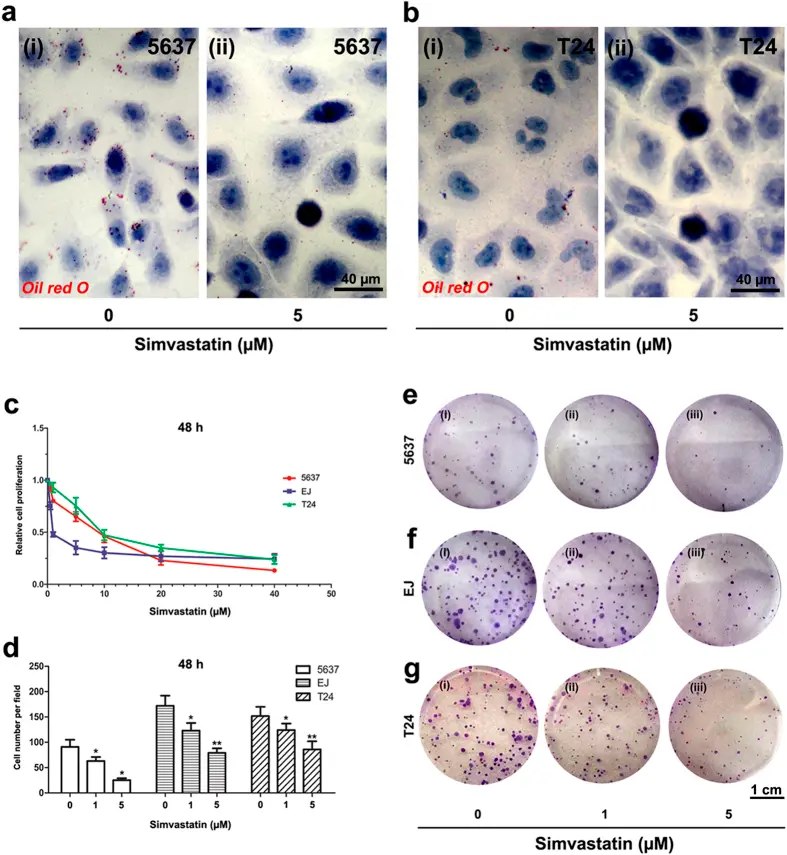
Simvastatin对BCa细胞中性甘油三酯和脂质水平的降低、细胞生长、活力和增殖的影响
2.3 PROTAC‑Mediated HMGCR Depletion Reprograms Lipid Metabolism in Breast Cancer to Potentiate Photoimmunotherapy via Ferroptosis

本研究中,Simvastatin (T0687) 通过抑制关键的胆固醇合成酶HMGCR发挥作用,该酶是甲戊酸途径的限速酶,维持GPX4的抗氧化能力。Simvastatin处理显著提高了HMGCR的表达,表现与洛伐他汀类似,但使用基于他汀的PROTAC则促进了HMGCR的降解。Simvastatin使辅酶Q10的产生降低了28%,对细胞抗氧化防御产生影响。GPX4蛋白表达亦明显被抑制,配合PROTAC处理使其降幅加大,导致脂质过氧化水平显著上升,超过90%的脂质过氧化累积表明铁死亡被强烈诱导。
同时,Simvastatin与还原型谷胱甘肽水平间接相关,GSH显著减少,线粒体膜电位下降95%以上,伴随线粒体形态损伤,包括线粒体缩小、膜致密和嵴减少。这些线粒体变化进一步表明铁死亡的发生。综上所述,Simvastatin通过抑制细胞抗氧化系统、增加脂质过氧化,引起细胞铁死亡机制在本实验中的显著激活。[5]
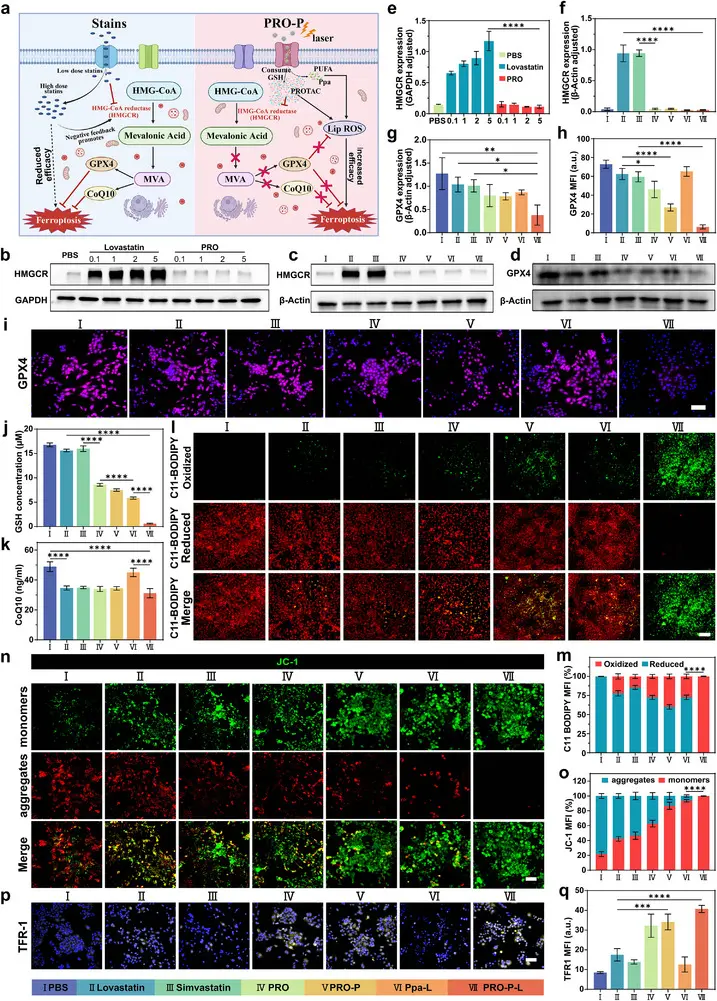
PRO-P 和他汀类药物通过靶向 HMGCR 诱导铁死亡并产生抗肿瘤效应的体外研究
结语:
Simvastatin主要通过竞争性抑制胆固醇生物合成限速酶HMG-CoA还原酶,减少对小GTP酶功能关键的异戊二烯类中间体合成,从而调控凋亡、自噬、线粒体自噬和铁死亡等多条细胞信号通路。文献显示,Simvastatin选择性诱导癌细胞凋亡,表现为促凋亡基因Bax上调和抗凋亡基因BCL-2下调;通过PPARγ信号通路诱导膀胱癌细胞周期阻滞,抑制其增殖和迁移;并通过抑制细胞抗氧化系统(GPX4、辅酶Q10)促进脂质过氧化及线粒体损伤,显著激活铁死亡机制。未来研究可进一步挖掘Simvastatin在癌症及代谢疾病治疗中的应用潜力,及其作为揭示脂质代谢与程序性细胞死亡交叉调控的分子工具的价值。
Q&A
Q1: Simvastatin的主要靶点是什么?它如何影响胆固醇生物合成?
A1: Simvastatin通过竞争性抑制HMG-CoA还原酶这一限速酶,减少肝脏胆固醇的合成,从而抑制胆固醇生物合成。
Q2: 文献中Simvastatin是如何诱导癌细胞凋亡的?
A2: Simvastatin通过上调促凋亡基因Bax并下调抗凋亡基因BCL-2,选择性诱导癌细胞凋亡,伴随DNA断裂增加。
Q3: Simvastatin诱导铁死亡的机制有哪些?
A3: Simvastatin抑制抗氧化系统(GPX4和辅酶Q10),显著增加脂质过氧化,降低谷胱甘肽水平,破坏线粒体膜电位和形态,联合诱导铁死亡。
参考文献
[1] Istvan ES, Deisenhofer J. Structural mechanism for statin inhibition of HMG-CoA reductase. Science. 2001;292(5519):1160-1164.
[2] Wang Y, et al. Statins induce autophagy and ferroptosis in cancer cells through modulation of the mevalonate pathway. Cell Death Dis. 2020;11(3):234.
[3] SPAMPANATO C, DE MARIA S, SARNATARO M, GIORDANO E, ZANFARDINO M, BAIANO S, et al.. Simvastatin inhibits cancer cell growth by inducing apoptosis correlated to activation of Bax and down-regulation of BCL-2 gene expression. International Journal of Oncology. 2011;40(4):935-941.
[4] Wang G, Cao R, Wang Y, Qian G, Dan H, Jiang W, et al.. Simvastatin induces cell cycle arrest and inhibits proliferation of bladder cancer cells via PPARγ signalling pathway. Scientific Reports. 2016;6(1):.
[5] Su T, Li G, Guan Y, Tian Q, Qi Y, Zhang Y, et al.. PROTAC‑Mediated HMGCR Depletion Reprograms Lipid Metabolism in Breast Cancer to Potentiate Photoimmunotherapy via Ferroptosis. Advanced Science. 2026;13(13):.





 |
|