 您的购物车当前为空
您的购物车当前为空
【TargetMol 明星分子】- Dimethyl fumarate: 激活抗氧化防御,调控免疫与自噬的多功能分子探针
背景介绍:
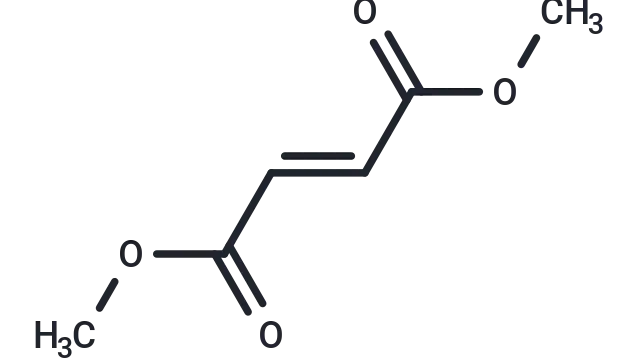
Dimethyl fumarate(T0492),CAS: 624-49-7,是一种具有显著生物活性的化合物,主要通过激活核因子红细胞2相关因子2(Nrf2)信号通路发挥作用。
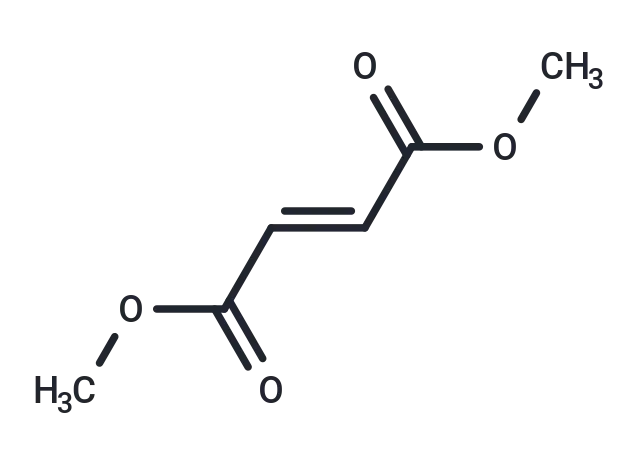
Dimethyl fumarate 分子结构式
Nrf2信号通路在细胞抵御氧化应激中起关键作用,Nrf2调控一系列抗氧化和细胞保护基因的表达。Dimethyl fumarate通过修饰Kelch样ECH相关蛋白1(KEAP1)上的半胱氨酸残基,抑制KEAP1对Nrf2的泛素化降解,促进Nrf2在细胞核内的积累和转录活性。核内的Nrf2结合抗氧化反应元件(ARE),启动多种与活性氧(ROS)清除和细胞内氧化还原稳态维持相关酶的表达。
除了经典的KEAP1-Nrf2调控机制外,Dimethyl fumarate还调节自噬途径,自噬作为细胞内质量控制和免疫调节的重要机制,与ROS水平密切相关。Dimethyl fumarate通过调控ROS和自噬流,影响细胞代谢及免疫反应,这一特性使其在神经炎症和HIV感染等研究中具有重要应用价值。其口服活性及穿越血脑屏障的能力,使其成为研究中枢神经系统氧化应激和炎症反应的理想工具。
在科研领域,Dimethyl fumarate被广泛用于解析氧化应激、免疫调节与自噬之间的相互作用。其抗菌和免疫调节特性在多发性硬化和HIV模型中被深入研究,这些疾病均以氧化应激和免疫功能失调为病理基础。通过激活Nrf2,Dimethyl fumarate降低ROS积累,减轻氧化损伤并调控炎症信号通路,体现了其对KEAP1-Nrf2通路的动态调节作用。此外,其对自噬的影响为理解细胞在应激条件下的稳态调节机制提供了重要视角。
总体而言,Dimethyl fumarate作为一种强效分子探针,有助于研究ROS信号、自噬及免疫调节之间的复杂联系。其多重生物学活性,包括抗菌和抗炎作用,凸显了其在氧化应激相关疾病及病毒发病机制研究中的潜在应用价值。该化合物在HIV蛋白酶活性及内源代谢物调控研究中的应用,进一步拓展了其在红氧敏感信号网络和细胞防御机制领域的科研意义。[1,2]
文献分享:
2.1 Effects of dimethyl fumarate on neuroprotection and immunomodulation

Dimethyl fumarate (T0492) 在本研究中表现出神经保护作用,其机制包括引起短暂的氧化应激,从而增加核红细胞生成因子2相关因子2(Nrf2)的水平及其核内定位,进而促进神经细胞内谷胱甘肽的合成和循环。用10 μM Dimethyl fumarate预处理24小时后,神经细胞和脾细胞内的谷胱甘肽含量均显著升高,但仅神经细胞在无半胱氨酸培养基中仍能维持谷胱甘肽的高水平,提示Dimethyl fumarate增强了神经细胞的谷胱甘肽分泌或循环能力。以Dimethyl fumarate预处理的神经细胞培养上清液能够提升新获神经细胞的谷胱甘肽水平,并对氧化性谷氨酸毒性具有保护作用,但对脾细胞活力无影响。
此外,Dimethyl fumarate抑制了来自不同小鼠品系脾细胞的促炎症细胞因子产生,且未导致脾细胞凋亡。值得注意的是,Dimethyl fumarate在多电极阵列检测中,无论浓度高低或作用时间长短,对神经网络的电活动指标(如尖峰频率、爆发频率及同步性)均未产生影响。综上,本研究结果表明Dimethyl fumarate通过增强抗氧化应答和免疫调节发挥保护作用,同时不改变神经元网络的功能活性。[3]
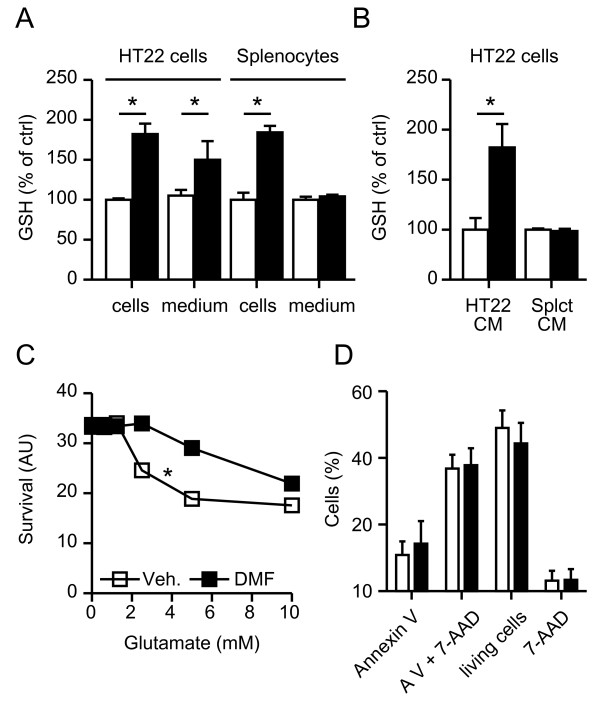
Dimethyl fumarate(DMF)处理的神经元细胞分泌神经保护性谷胱甘肽(GSH)
2.2 Dimethyl Fumarate, an Immune Modulator and Inducer of the Antioxidant Response, Suppresses HIV Replication and Macrophage-Mediated Neurotoxicity: A Novel Candidate for HIV Neuroprotection

Dimethyl fumarate (T0492) 在本研究中表现出对体外炎症细胞因子的抑制作用。同时,Dimethyl fumarate 降低了处理细胞中的氧化应激标志物,显示其减少了细胞氧化损伤。此外,Dimethyl fumarate 抑制了实验模型中的小胶质细胞激活,表明其在调节免疫反应方面的作用。以上结果表明,Dimethyl fumarate 主要通过抑制炎症反应、降低氧化应激指标以及减弱免疫细胞活化,发挥了其在本研究中的作用。[4]
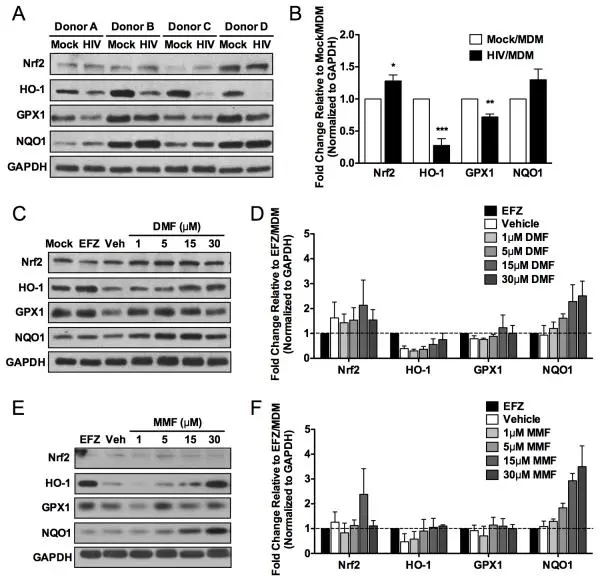
DMF恢复HIV感染引起的抗氧化反应失衡
2.3 The role of gasdermin-mediated mitochondrial RNA release in amplifying secondary immune response during microbial infection

本研究显示,Dimethyl fumarate(T0492)能够抑制GSDMD与GSDME的蛋白裂解,而这两种蛋白是先天免疫反应信号通路中的关键介导因子。在使用LPS预处理并用Nigericin激活的THP-1细胞中,Dimethyl fumarate处理显著抑制了GSDMD的裂解,同时降低了与促炎性细胞因子产生相关的重要信号分子TBK1的磷酸化。在小鼠腹腔巨噬细胞中也观察到了类似的效果。
在使用A549细胞感染囊泡性口炎病毒(VSV)的病毒感染模型中,Dimethyl fumarate预处理显著抑制了GSDME的裂解及其下游TBK1的磷酸化。这些分子变化与先天免疫激活后关键促炎细胞因子IFN-β和IL-6表达的明显降低相一致。综上所述,Dimethyl fumarate通过抑制GSDMD和GSDME的裂解及其介导的TBK1磷酸化,调节了先天免疫信号通路,导致促炎细胞因子的表达减少。[5]
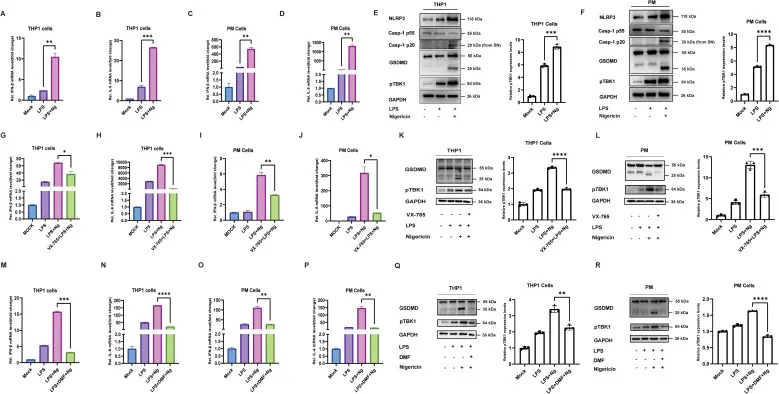
GSDMD抑制可调节LPS和Ng反应中的细胞因子产生
结语:
Dimethyl fumarate通过修饰KEAP1上的半胱氨酸残基,抑制KEAP1介导的Nrf2泛素化降解,促进Nrf2在细胞核内积累并结合抗氧化反应元件,激活抗氧化及细胞保护基因表达。文献显示,Dimethyl fumarate增强神经细胞内谷胱甘肽的合成及循环,抑制促炎细胞因子产生且不影响神经网络功能,降低氧化应激标志物,抑制小胶质细胞活化,并通过抑制GSDMD和GSDME的裂解及下游TBK1磷酸化,调节先天免疫信号通路。
这些多重作用使Dimethyl fumarate成为研究氧化应激、自噬与免疫调控交互的重要工具。未来研究可聚焦其在神经炎症及病毒性疾病中的治疗潜力,深入解析其调节先天免疫机制,并拓展其在氧化还原生物学及宿主-病原体相互作用中的应用。
Q&A
Q1: Dimethyl fumarate激活抗氧化反应的主要分子机制是什么?
A1: Dimethyl fumarate通过修饰KEAP1上的半胱氨酸残基,抑制KEAP1介导的Nrf2泛素化降解,稳定并促进Nrf2转入细胞核,激活抗氧化基因表达。
Q2: 文献中提到Dimethyl fumarate如何影响免疫细胞?
A2: Dimethyl fumarate抑制促炎细胞因子产生,降低氧化应激标志物,抑制小胶质细胞激活,并通过抑制GSDMD和GSDME蛋白裂解及TBK1磷酸化,调节先天免疫信号通路,减少炎症因子表达。
Q3: Dimethyl fumarate会影响神经网络活动吗?
A3: 不会。研究表明,Dimethyl fumarate在不同浓度和作用时间下均未改变神经网络的电活动指标,如尖峰频率、爆发频率及同步性。
参考文献
[1] Linker RA, Lee DH, Ryan S, et al. Fumaric acid esters exert neuroprotective effects in neuroinflammation via activation of the Nrf2 antioxidant pathway. Brain. 2011;134(Pt 3):678-692.
[2] Gold R, Kappos L, Arnold DL, et al. Placebo-controlled phase 3 study of oral BG-12 for relapsing multiple sclerosis. N Engl J Med. 2012;367(12):1098-1107.
[3] Albrecht P, Bouchachia I, Goebels N, Henke N, Hofstetter H, Issberner A, et al.. Effects of dimethyl fumarate on neuroprotection and immunomodulation. Journal of Neuroinflammation. 2012;9(1):.
[4] Cross S, Cook D, Chi A, Vance P, Kolson L, Wong B, et al.. Dimethyl Fumarate, an Immune Modulator and Inducer of the Antioxidant Response, Suppresses HIV Replication and Macrophage-Mediated Neurotoxicity: A Novel Candidate for HIV Neuroprotection. The Journal of Immunology. 2011;187(10):5015-5025.
[5] Afaq U, Qudus M, Liu S, Wu K, Chen Y, Tian M, et al.. The role of gasdermin-mediated mitochondrial RNA release in amplifying secondary immune response during microbial infection. Frontiers in Immunology. 2026;16():.





 |
|