 您的购物车当前为空
您的购物车当前为空
【TargetMol 明星分子】- Thalidomide: 作为分子胶调控蛋白降解与细胞命运的关键工具
背景介绍:
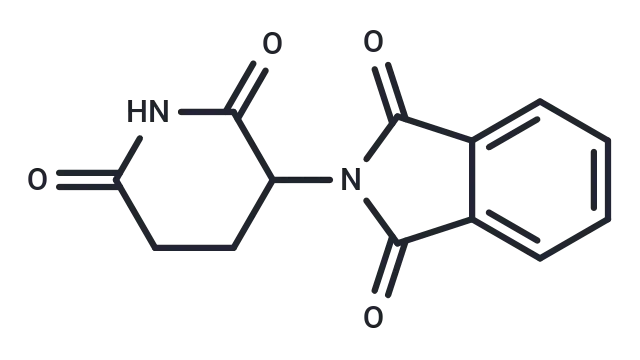
Thalidomide(T0213),CAS: 50-35-1,是一种合成的谷氨酸衍生物,具有致畸性、免疫调节、抗炎和抗血管生成等多重生物学功能。
Thalidomide分子结构式
Thalidomide作用机制主要通过作为分子胶(molecular glue),促进特定底物与E3泛素连接酶复合物,尤其是cereblon(CRBN)的结合,从而调节蛋白质的泛素化及其后续的蛋白酶体降解。通过这种机制,Thalidomide能够影响细胞凋亡和自噬等关键细胞过程,这些过程对于维持细胞稳态和调控免疫反应至关重要。Thalidomide与CRBN结合后,改变了E3连接酶的底物特异性,促使转录因子及炎症信号分子(如肿瘤坏死因子α,TNF-α)被选择性降解,从而调控TNF-α信号通路,发挥其抗炎作用,并进一步影响下游的凋亡和自噬途径,体现了其在细胞命运调控中的重要作用。
在科研领域,Thalidomide被广泛用于解析E3连接酶底物识别和降解的分子机制,以及探讨免疫细胞中自噬与凋亡之间的相互作用。作为E3连接酶的配体,Thalidomide是研究蛋白质稳态和泛素-蛋白酶体系统的重要工具。此外,Thalidomide对TNF-α信号通路的调控为研究炎症信号网络及其通过翻译后修饰调节机制提供了模型。其抗血管生成特性也使其在血管生物学和肿瘤微环境研究中具有应用价值。总体而言,Thalidomide作为分子探针,揭示了泛素化、炎症反应和程序性细胞死亡途径之间的动态相互作用,为新型分子胶和靶向蛋白降解策略的开发奠定了基础。
Thalidomide与E3连接酶复合物的动态结合展示了小分子如何重新编程泛素化机制,实现对特定蛋白的选择性降解,进而调控TNF-α介导的凋亡和自噬信号通路。这一特性使Thalidomide成为设计下一代高特异性分子胶的原型,其科研价值不仅限于历史背景,更为理解和利用泛素-蛋白酶体系统在细胞调控和免疫调节中的作用提供了重要工具。[1,2]
文献分享:
2.1 Synergistic Inhibition of Thalidomide and Icotinib on Human Non-Small Cell Lung Carcinomas Through ERK and AKT Signaling

Thalidomide (T0213) 在本研究中表现出多种生物学功能,包括通过阻断血管内皮生长因子(VEGF)和碱性成纤维细胞生长因子(bFGF)信号通路抑制血管生成,抑制肿瘤坏死因子-α(TNF-α)合成,促进T细胞增殖和淋巴激素产生,及阻断NF-κB激活。
实验结果显示,沙利度胺与依匹替尼联用对非小细胞肺癌细胞系PC9和A549具有协同抑制增殖的作用,并在PC9细胞中效果更明显。组合用药显著诱导细胞凋亡,凋亡细胞比例较单独用药显著增加,同时伴随凋亡执行蛋白caspase-3的激活及促凋亡蛋白Bax的上调。体内PC9异种移植模型中,沙利度胺与依匹替尼联合用药抑制肿瘤生长,表现为Ki-67增殖指数显著下降和TUNEL染色阳性细胞增加。这些结果表明,Thalidomide通过增强细胞凋亡和抑制细胞增殖,在实验中发挥了抑制非小细胞肺癌细胞生长的作用。[3]
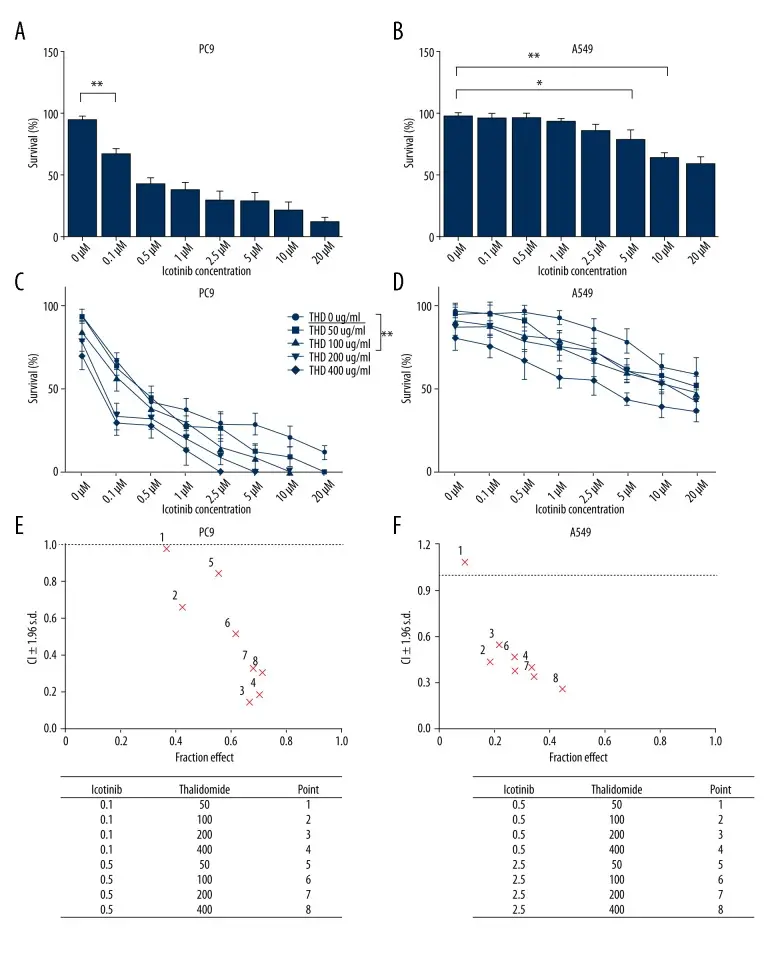
Thalidomide和Icotinib对PC9和A549细胞增殖的影响
2.2 Fangjihuangqi Decoction inhibits MDA‐MB‐231 cell invasion in vitro and decreases tumor growth and metastasis in triple‐negative breast cancer xenografts tumor zebrafish model
Thalidomide (T0213) 在三阴性乳腺癌异种移植瘤斑马鱼模型中显著抑制了肠道血管生成。与模型对照组相比,给予219 μg/mL Thalidomide处理的斑马鱼,其肠道血管结构和血管直径恢复至接近正常水平。Thalidomide处理组肠道新生血管芽的数量从模型组的2.30显著减至0.90,血管生成抑制率达45%。该结果表明,Thalidomide (T0213) 能够抑制肿瘤诱导的肠道血管形成,减少了对肿瘤进展具有促进作用的不成熟血管的生成。 [4]
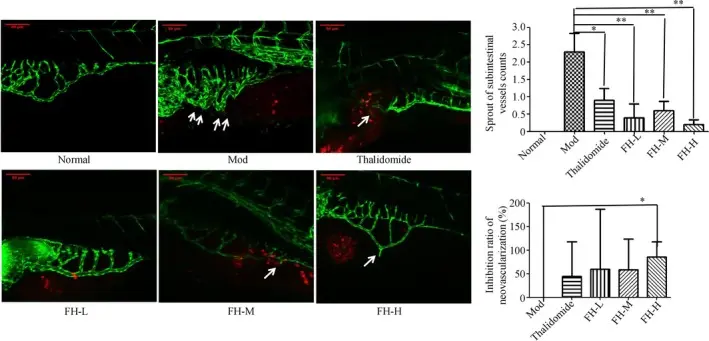
FH减少了TNBC异种移植物斑马鱼的肿瘤血管新生
结语:
Thalidomide作为一种分子胶,通过促进特定底物与E3泛素连接酶复合物cereblon(CRBN)的结合,实现蛋白质的选择性泛素化及蛋白酶体降解。这一机制使其能够调控细胞凋亡和自噬等关键通路,靶向降解转录因子及炎症信号分子如TNF-α。文献中显示,Thalidomide与依匹替尼联合用药在非小细胞肺癌模型中协同抑制细胞增殖并促进凋亡;在三阴性乳腺癌斑马鱼异种移植瘤模型中显著抑制肿瘤诱导的肠道血管生成。未来研究可利用Thalidomide的分子胶特性,开发高特异性的靶向蛋白降解剂,并深入探讨泛素化、炎症与程序性细胞死亡之间的相互作用,推动新型治疗策略的创新。
Q&A
Q1: Thalidomide主要通过何种机制发挥其生物学功能?
A1: Thalidomide作为分子胶,促进特定底物与E3泛素连接酶复合物cereblon(CRBN)的结合,调节蛋白质泛素化及蛋白酶体降解,从而影响细胞凋亡和自噬等关键通路。
Q2: 文献中Thalidomide如何影响非小细胞肺癌模型中的肿瘤生长?
A2: Thalidomide与依匹替尼联合使用,对非小细胞肺癌细胞系协同抑制细胞增殖,显著诱导细胞凋亡,伴随caspase-3激活和Bax上调,在PC9异种移植瘤模型中抑制肿瘤生长。
Q3: Thalidomide在三阴性乳腺癌斑马鱼异种移植瘤模型中对血管生成有何影响?
A3: Thalidomide显著抑制肿瘤诱导的肠道血管生成,新生血管芽数量减少45%,血管结构和直径恢复接近正常水平。
参考文献
[1] Ito T, Ando H, Suzuki T, et al. Identification of a primary target of thalidomide teratogenicity. Science. 2010;327(5971):1345-1350.
[2] Lu G, Middleton RE, Sun H, et al. The myeloma drug lenalidomide promotes the cereblon-dependent destruction of Ikaros proteins. Science. 2014;343(6168):305-309.
[3] Sun X, Xu Y, Wang Y, Chen Q, Liu L, Bao Y. Synergistic Inhibition of Thalidomide and Icotinib on Human Non-Small Cell Lung Carcinomas Through ERK and AKT Signaling. Medical Science Monitor. 2018;24():3193-3203.
[4] Guo Y, Fan Y, Pei X. Fangjihuangqi Decoction inhibits MDA‐MB‐231 cell invasion in vitro and decreases tumor growth and metastasis in triple‐negative breast cancer xenografts tumor zebrafish model. Cancer Medicine. 2020;9(7):2564-2578.





 |
|