 您的购物车当前为空
您的购物车当前为空
【TargetMol 明星分子】- Chloroquine phosphate: 调控自噬与免疫信号,揭示病毒与肿瘤研究新机遇
背景介绍:
Chloroquine phosphate(T0194),CAS: 50-63-5,是一种经典的氨基喹啉类化合物,广泛用于抗疟疾研究,同时也是一种有效的自噬抑制剂。
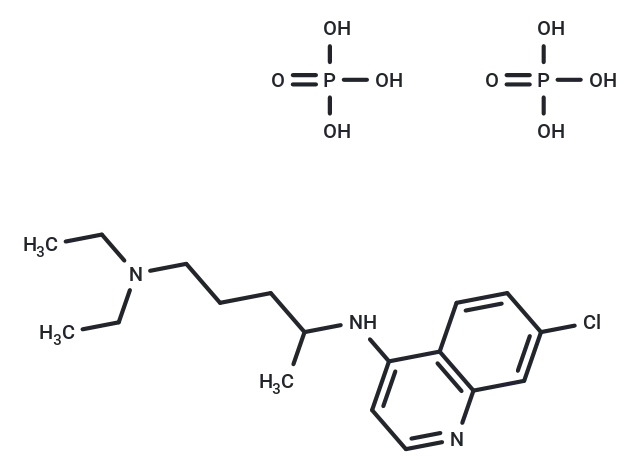
Chloroquine phosphate分子结构式
Chloroquine phosphate主要作用机制是通过在细胞内酸性隔室(如溶酶体)中积累,提升这些隔室的pH值,从而破坏溶酶体功能。溶酶体碱化导致自噬小体与溶酶体融合受阻,进而抑制自噬流。这种对自噬过程的调控使Chloroquine phosphate成为研究细胞内降解途径和细胞稳态的重要工具。除此之外,Chloroquine phosphate还能抑制Toll样受体(TLRs),尤其是TLR7和TLR9,这些受体在先天免疫系统中识别病毒核酸并启动免疫信号通路,调节炎症反应和抗病毒免疫。
在TLR信号通路中,TLR7和TLR9位于内体,识别病毒RNA和DNA,激活下游的NF-κB和IRF7等转录因子,诱导I型干扰素及促炎细胞因子的产生。Chloroquine phosphate通过阻断内体酸化,抑制TLR7/9的活化,从而调节免疫反应的强度。这种机制在研究HIV和SARS-CoV等病毒感染的免疫应答中具有重要意义。通过抑制TLR信号,Chloroquine phosphate帮助科学家解析病毒与宿主免疫系统的相互作用及炎症调控机制。
此外,Chloroquine phosphate还通过影响细胞内运输和自噬过程,间接干扰HIV蛋白酶相关的病毒复制途径。其对寄生虫和病毒(包括SARS-CoV)的广谱活性,正是基于其多靶点调控机制。在科研领域,Chloroquine phosphate被广泛用作自噬抑制剂和TLR信号通路的调节剂,帮助研究者深入理解细胞稳态、炎症疾病及病毒发病机制。
综上所述,Chloroquine phosphate通过调节溶酶体pH值,动态干预自噬和TLR信号通路的关键环节,影响细胞对感染和应激的反应。其双重功能使其成为研究免疫调控、病原体与宿主相互作用及细胞内运输机制的重要工具。[1,2]
文献分享:
2.1 Chloroquine has tumor-inhibitory and tumor-promoting effects in triple-negative breast cancer

Chloroquine phosphate (T0194) 在本研究中表现出对TLR9表达的双重作用:其可上调TLR9的mRNA表达水平,但在常氧和缺氧条件下均可降低TLR9蛋白水平。该药物对MMP-2和MMP-9的mRNA表达及蛋白酶活性具有抑制作用,然而却提升了MMP-13的mRNA表达及其蛋白酶活性。Chloroquine phosphate能够剂量依赖性地抑制MDA-MB-231细胞在缺氧诱导下的活力增加,这种抑制作用与细胞TLR9表达状态无关。尽管在体外表现出对细胞生长和浸润的抑制作用,但Chloroquine phosphate在体内并未阻止由相同细胞形成的局部肿瘤生长。[3]
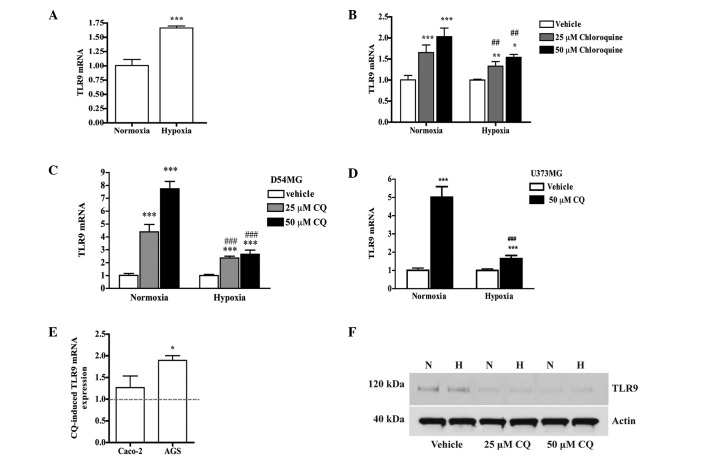
氯喹对缺氧诱导TLR9表达的影响
2.2 Hepatoma cell-intrinsic TLR9 activation induces immune escape through PD-L1 upregulation in hepatocellular carcinoma

Chloroquine phosphate (T0194),即文献中所述的磷酸氯喹,作为TLR9的拮抗剂,在Huh7细胞中抑制了STAT3蛋白的PAR化水平。实验结果显示,磷酸氯喹能够降低野生型和TLR9过表达的Huh7细胞中STAT3的PAR化,说明其能够抑制由TLR9激活所引发的STAT3 PAR化修饰。此外,实验中外源性PARP1的过表达能够恢复STAT3的PAR化,而磷酸氯喹则能降低该修饰水平,支持磷酸氯喹对该信号通路的调节作用。上述数据表明磷酸氯喹在该实验体系中抑制了STAT3的PAR化过程,这一过程与TLR9信号的状态相关。综上所述,研究明确指出磷酸氯喹具有抑制STAT3 PAR化的作用。[4]
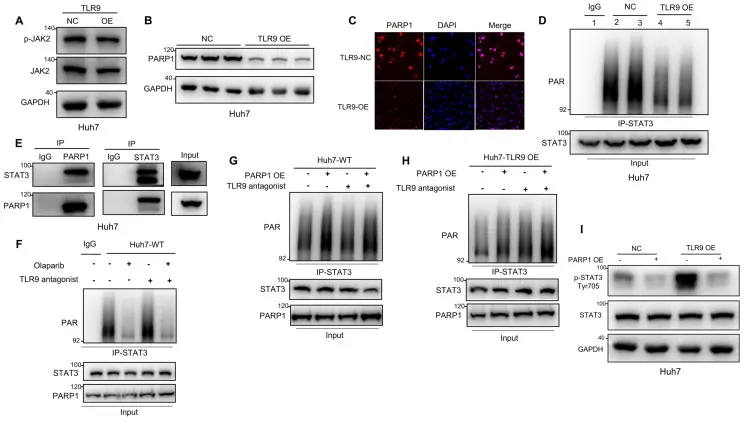
TLR9激活通过PARP1介导的STAT3磷酸化促进了STAT3 Tyr705磷酸化
2.3 A covalent peptide-based lysosome-targeting protein degradation platform for cancer immunotherapy

Chloroquine phosphate (T0194) 在本研究中被发现能够抑制由共价Pep-TAC诱导的B16细胞和MC38细胞中PD-L1的降解。在pH 7.4的条件下,使用共价肽v9x显著降解PD-L1,而添加chloroquine phosphate后,这种降解作用被逆转,表明chloroquine phosphate阻断了TFRC依赖的溶酶体介导的降解过程。相比之下,蛋白酶体抑制剂MG132未能逆转PD-L1的降解,进一步支持chloroquine phosphate对溶酶体降解途径的特异性抑制作用。由此可见,chloroquine phosphate在该实验中通过干预溶酶体途径,抑制了共价Pep-TAC介导的PD-L1降解作用。这一结果明确表明chloroquine phosphate能够抑制Pep-TAC诱导的靶向蛋白溶酶体降解过程。[5]
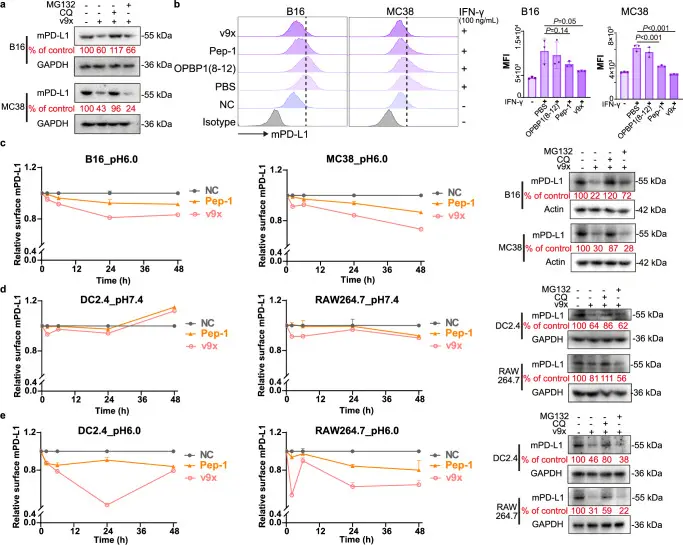
在肿瘤、DC或巨噬细胞系中,评估的IFN-γ或其他pH条件下,
共价Pep-TAC降解PD-L1的情况
结语:
Chloroquine phosphate通过在溶酶体内积累并提升pH值,破坏溶酶体功能,抑制自噬小体与溶酶体融合,从而阻断自噬流。同时,其通过阻断内体酸化抑制TLR7和TLR9的活化,调节下游免疫信号通路。文献报道其在癌细胞中双向调控TLR9及多种金属基质蛋白酶表达,抑制与免疫逃逸相关的STAT3 PAR化,并阻断PD-L1的溶酶体介导降解。虽然其在体外抑制癌细胞活力,但对肿瘤体内生长抑制有限,可能与其促侵袭作用有关。未来研究可聚焦于优化其自噬与TLR双重调控功能,提升抗病毒及抗肿瘤治疗效果,并深入探索其在靶向蛋白降解及免疫检查点调节中的潜力。
Q&A
Q1: Chloroquine phosphate抑制自噬的主要机制是什么?
A1: 它通过在溶酶体内积累并提升pH值,破坏溶酶体功能,阻止自噬小体与溶酶体融合,从而抑制自噬流。
Q2: Chloroquine phosphate如何影响TLR7和TLR9信号通路?
A2: 它阻断内体酸化,抑制TLR7和TLR9的活化,调节免疫反应强度。
Q3: 在肿瘤相关研究中,Chloroquine phosphate表现出了哪些作用?
A3: 它调节TLR9的mRNA和蛋白表达,抑制部分金属基质蛋白酶的表达与活性,抑制STAT3的PAR化修饰,并阻断PD-L1的溶酶体介导降解,但未能抑制肿瘤体内生长。
参考文献
[1] Mauthe M, Orhon I, Rocchi C, et al. Chloroquine inhibits autophagic flux by decreasing autophagosome-lysosome fusion. Autophagy. 2018;14(8):1435-1455.
[2] Kuznik A, Bencina M, Svajger U, et al. Mechanism of endosomal TLR inhibition by antimalarial drugs and imidazoquinolines. J Immunol. 2011;186(8):4794-4804.
[3] TUOMELA J, SANDHOLM J, KAUPPILA J, LEHENKARI P, HARRIS K, SELANDER K. Chloroquine has tumor-inhibitory and tumor-promoting effects in triple-negative breast cancer. Oncology Letters. 2013;6(6):1665-1672.
[4] Zhou B, Yan J, Guo L, Zhang B, Liu S, Yu M, et al.. Hepatoma cell-intrinsic TLR9 activation induces immune escape through PD-L1 upregulation in hepatocellular carcinoma. Theranostics. 2020;10(14):6530-6543.
[5] Xiao Y, He Z, Li W, Chen D, Niu X, Yang X, et al.. A covalent peptide-based lysosome-targeting protein degradation platform for cancer immunotherapy. Nature Communications. 2025;16(1):.





 |
|