图1. 经典的Wnt/Fz信号通路(改编自《未来药物化学》(2015年),第7卷,第18期,第2485–2505页),图中显示了Enamine公司可提供的特异性靶向偏向性集中化合物库。
尽管已有大量文献报道Wnt抑制剂的鉴定及其作为潜在抗肿瘤疗法的临床进展,但关于Wnt激活剂和/或增强剂治疗应用的研究报道却十分有限。这类小分子调节剂通常通过抑制与β-连环蛋白稳定性相关的激酶(即GSK3β和CK1)发挥作用。例如,CHIR-99021(CT99021)是一种GSK-3α/β抑制剂,其对GSK-3α和GSK-3β的IC50分别为10 nM和6.7 nM,且相较于其最近同源物CDC2、ERK2以及其他蛋白激酶,其选择性超过500倍。在小鼠或人造血干细胞移植实验中,给予CHIR-99021可显著增强受体小鼠的造血重建能力。该化合物通过影响支架蛋白APC和Axin,诱导Wnt靶基因表达。然而,GSK3参与细胞内多种信号传导过程,可能导致基于其作用机制的毒性。PF-670462是CK1ε的一种高效选择性抑制剂(IC50 = 7.7 ± 2.2 nM),其对42种其他激酶的选择性超过30倍,而CK1ε是Wnt信号通路中磷酸化Dvl蛋白的关键激酶。
目前,对于具有新型作用机制的Wnt信号通路抑制剂、激活剂和增强剂(即调节和/或增强内源性Wnt配体效应的化合物)的需求仍然持续存在。我们结合新型化学结构和基于结构的设计方法,构建了一个包含约10,000个类先导化合物的化合物库,以靶向Wnt/Fz信号通路的不同环节。该库涵盖Wnt/Fz信号级联的关键靶点,包括sFRP1、Dkk1、DyrK1A/B,以及β-连环蛋白与Tcf-4、Bcl-9等多种转录因子的相互作用界面。该化合物库适用于基于靶点、基于报告基因或表型筛选等多种检测方法。所发现的苗头化合物应具有易于优化特性(即可行的构效关系研究和先导化合物开发潜力),适合作为开发治疗肿瘤、骨病、心血管/代谢、胃肠道及中枢神经系统/神经退行性疾病的药物起点。
用于化合物库设计的Fz/Wnt信号通路特异性靶点与节点如下:
Wnt/sFRP-1相互作用抑制剂:sFRP-1蛋白家族包含一类能够同时结合Wnt配体和卷曲蛋白(Fz)受体的内源性分子。抑制sFRP-1可能导致Wnt信号通路的代偿性激活。此外,WAY 316606是一种sFRP-1抑制剂(Ki = 80 nM),据报道,在小鼠颅盖器官培养实验中,其浓度低于1 nM时即可增加骨总面积。它也被报道为一种抗骨质疏松剂。WAY-262611是一种Wnt通路激动剂,在TCF-荧光素酶报告基因实验中,其增加骨形成率的EC50为0.63 uM。WAY-262611表现出良好的药代动力学特性,在卵巢切除大鼠模型中口服给药后,可观察到骨小梁形成率呈剂量依赖性增加。需要特别注意监测与长期干扰Wnt通路相关的特定器官毒性,包括肿瘤形成,不过近期数据给出了不同的观点。代表此靶点的化合物库约有1200个化合物。
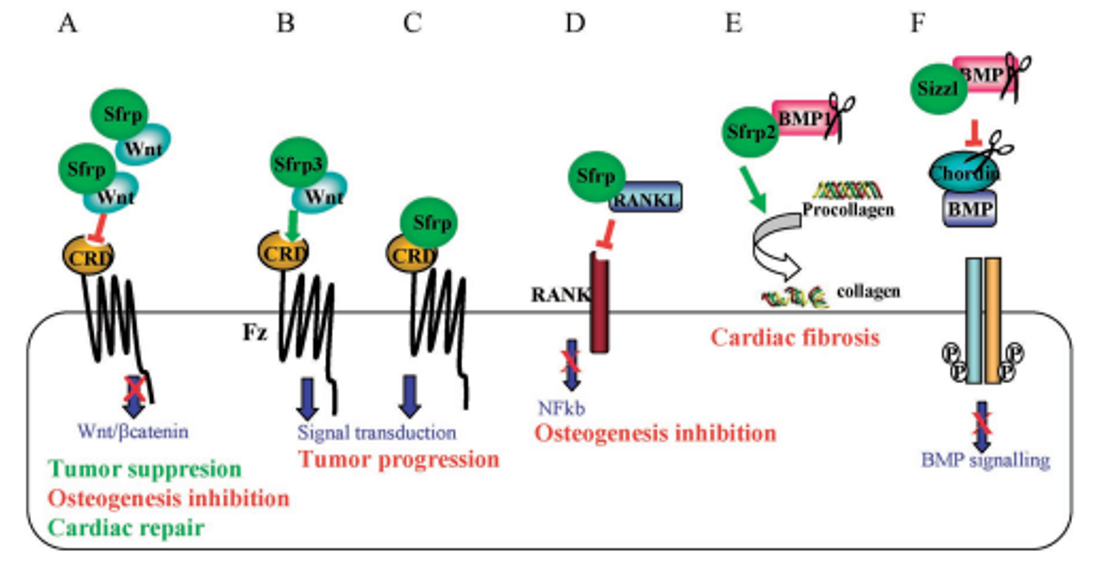
图2. sFRP1/2的多功能分子相互作用及其在病理事件中的意义。A) sFRP1/2隔离Wnt蛋白,从而拮抗Wnt/β-catenin信号通路;B) Frzb (sFRP3) 和 Crescent促进Wnt蛋白扩散,扩大其信号范围;C) sFRP1/2与Fz受体结合,激活细胞内信号传导;D) sFRP1结合RANKL,阻止其与RANK受体相互作用;E) sFRP2结合并增强BMP1/Tollpid样金属蛋白酶的胶原蛋白酶原活性,加速前胶原蛋白的加工;F) Sizzled结合并抑制BMP1/Tolloid样金属蛋白酶的Chordinase活性;未受裂解的Chordin结合并隔离BMPs (摘自Tohoku J. Exp. Med. 2010, 221, 11-17)。
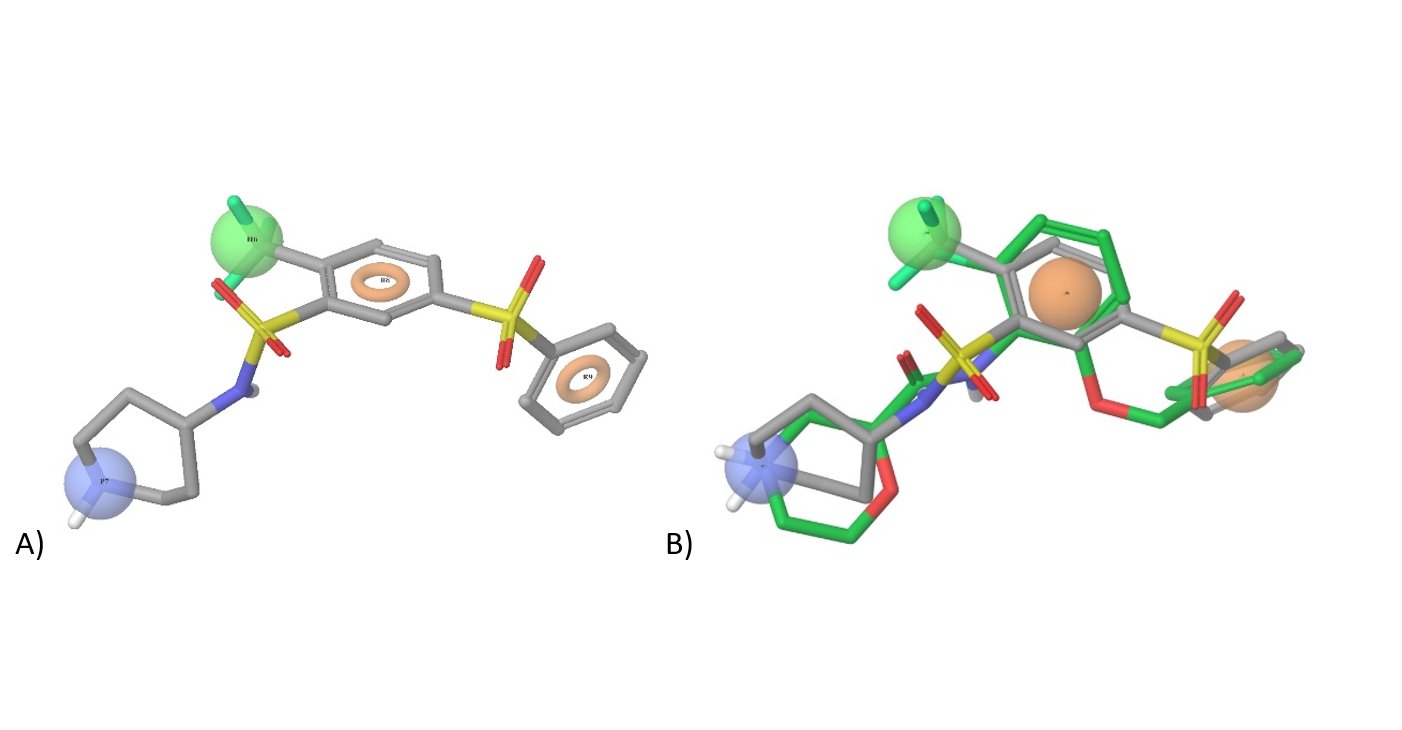
图3. A) 基于WAY 316606的药效团模型;橙色 – 芳香/杂芳香基团,绿色 – 疏水性药效团(卤素、CF3、CHF2、Me、Et、iPr等),蓝色 – 带正电荷部分(+NH3Alk、+NH2Alk2、+NHAlk3等);B) WAY-316606与我们用于(亚)文库设计的药效团构象的叠合图。
DKK-1抑制剂的研究:我们综合运用了分子对接和基于配体的方法,以寻找潜在的DKK-1结合剂。具体而言,我们利用DKK1/LRP6的蛋白质-蛋白质相互作用界面,从整个Enamine筛选化合物库中筛选相匹配的配体。同时,基于已知的DKK-1/LRP6相互作用抑制剂NCI8642及其类似物的结构,我们进行了基于配体的搜寻和药效团建模。在对接计算中,我们重点关注与LRP6结合的Dkk-1关键环区的拓扑结构和电荷分布特征。我们推断,阻断或破坏DKK-1/LRP6 PPI中这一环状结构的特征,可能会在维持“正常”Wnt-Fz-LRP6信号传导的同时,产生调节和/或激活Wnt信号通路的化合物。
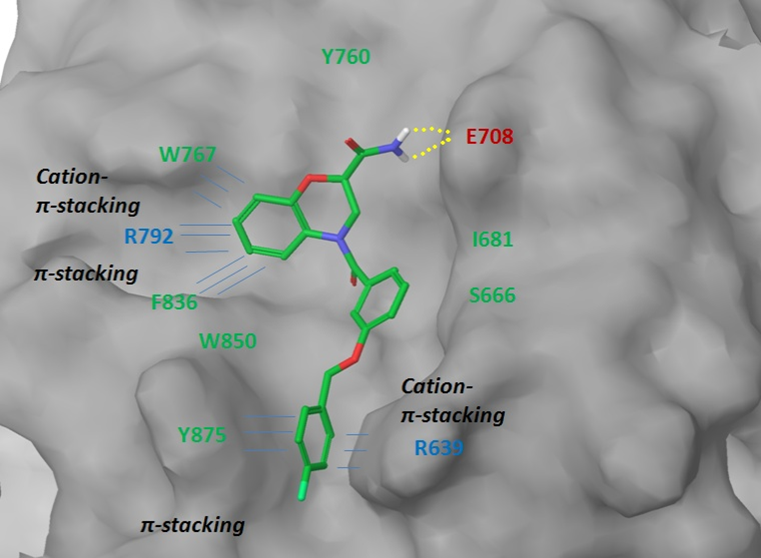
图4. LRP6蛋白与重点子集中代表性配体之间的结合界面。
我们利用已知的DKK-1抑制剂WAY 262611及其三维药效团,通过基于配体的方法,筛选出3000多种类先导化合物作为潜在的结合物。
图5. A) 基于WAY-262611的药效团模型;橙色 – 芳香/杂芳基团,蓝色 – 带正电荷部分(+NH3Alk, +NH2Alk2, +NHAlk3等),洋红色 – 脂肪环;B) WAY-262611与我们用于(子)库设计的药效团结构之间的叠合图。
Dvl-Axin 抑制剂:Dvl 与 Axin 的相互作用是由一个特定的 PDZ 结构域介导的。由于没有关于此蛋白质-蛋白质相互作用界面的结构信息,我们利用 AlphaFold2 和大量关于 PDZ 结构域的 SBio 数据构建了一个同源模型。所得模型被用于对整个筛选库进行对接计算,以识别最有前景的"命中"化合物。最终,大约 2500 种最终偏向 Dvl 的化合物被添加到了化合物库中。一个假定的 Dvl 结合剂的代表性实例如下图所示。
图6. 我们筛选集中一个Dvl/PDZ结构域结合配体的代表性示例。
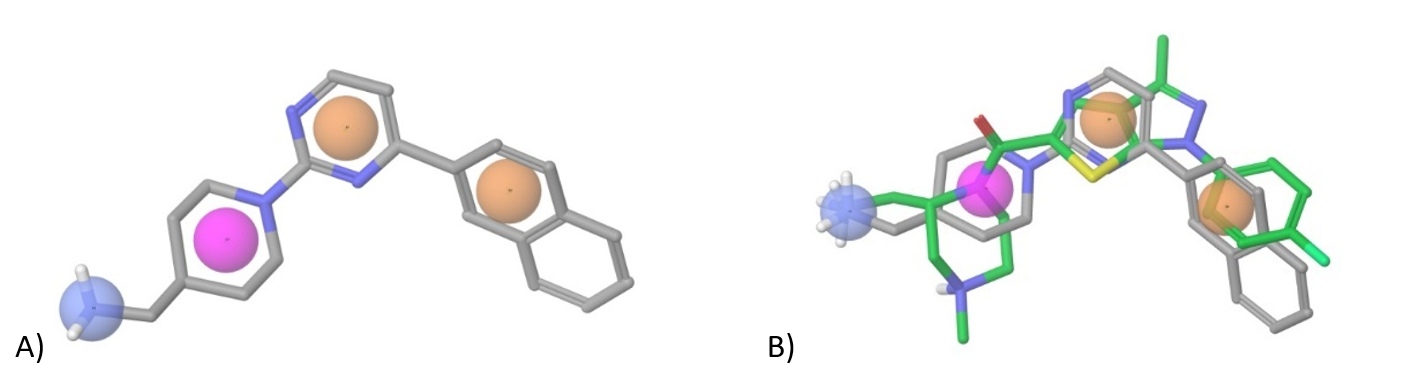
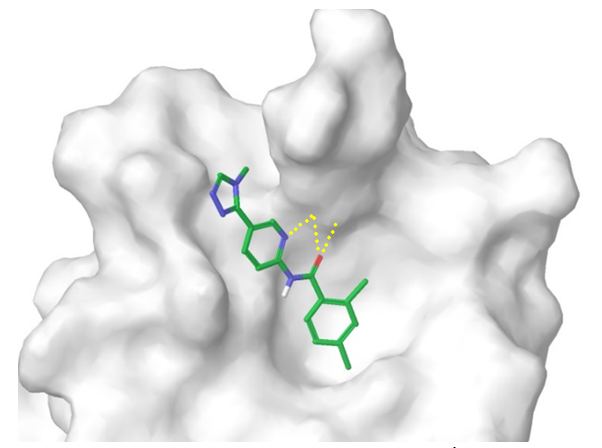
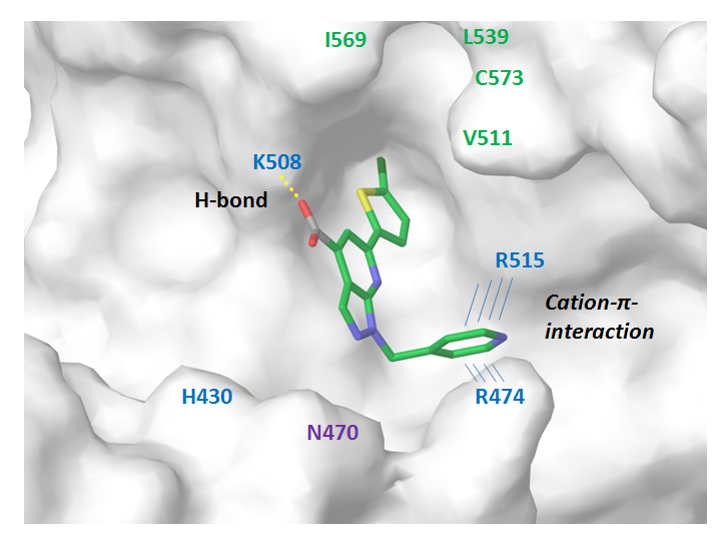
β-Catenin/TCF4 蛋白质-蛋白质相互作用建模:为模拟 β-catenin 与 Tcf-4 之间的相互作用界面,我们依据已报道的结构数据(ACS Chem. Biol. 2014, 9, 193-201),识别了关键接触点,包括对接配体与 Arg474/515 钳之间引人注目的质子化吡啶(阳离子)-π 相互作用。该疏水口袋的拓扑结构以及芳香氨基 NH2 与蛋白质 Lys508 残基形成的氢键,支持我们构建了相应的药效团模型(图 7)。经过对接计算和打分筛选,我们精选了约 1800 个小分子,并将其整合为 β-Catenin/TCF4 子库。
图7. β-连环蛋白与聚焦子集代表性配体间的结合界面。
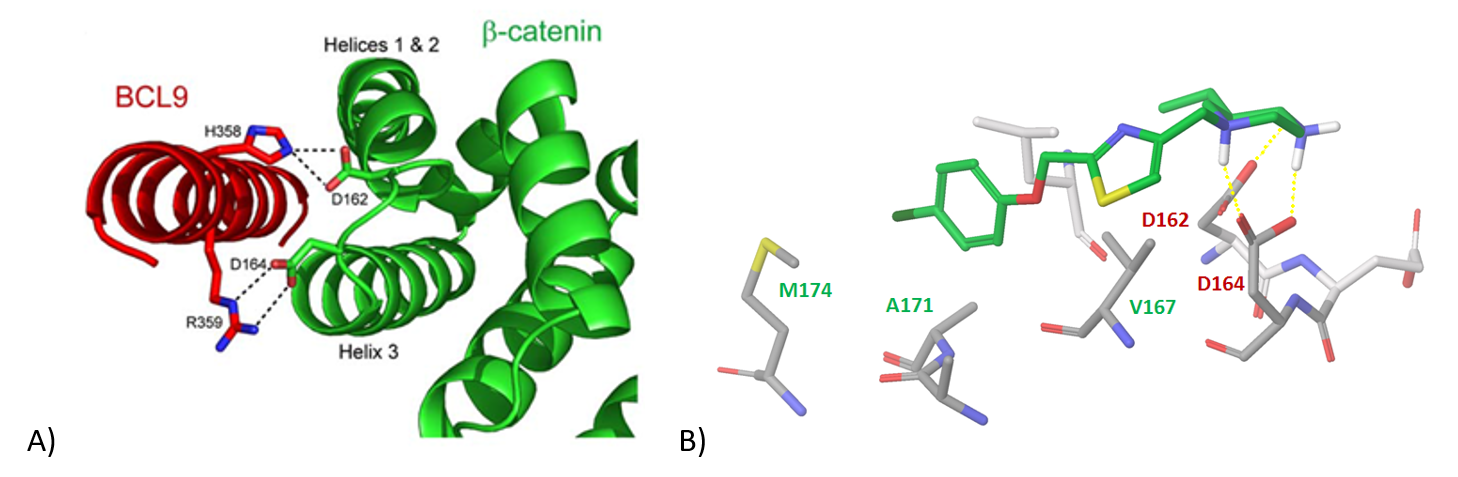
β-连环蛋白/Bcl9蛋白-蛋白相互作用界面:我们重点关注了已有文献报道的两种生物分子之间螺旋-螺旋相互作用的结构数据。具体而言,我们研究了H358、R359(Bcl9)与D162、D164(β-连环蛋白)之间的关键氢键(图8)。在完成对接计算并优先考虑结合构象后,我们筛选出能与D162/D164形成稳定氢键、并与β-连环蛋白存在显著π-π堆积/疏水相互作用的分子,最终构建了包含1779个化合物的分子库。
图 8. A) β-连环蛋白/BCL9 螺旋-螺旋相互作用界面,展示关键氢键;B) β-连环蛋白与聚焦子集中一个代表性配体的结合。
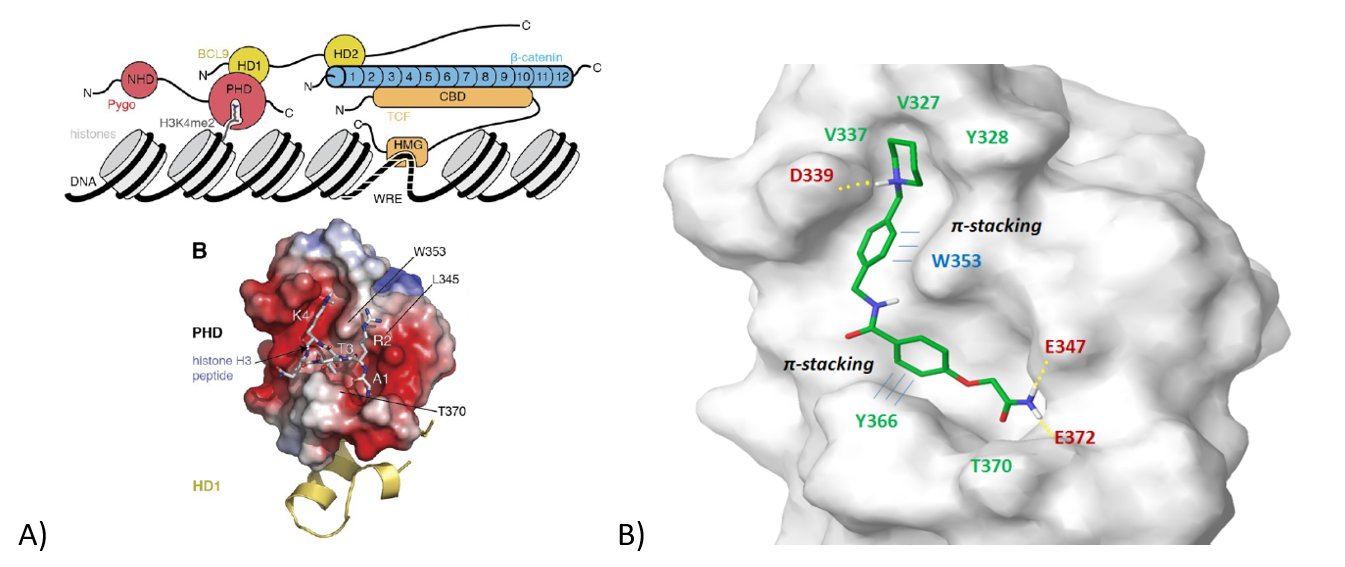
Bcl9/PYGO/组蛋白H3相互作用界面:阻断Wnt/Fz信号传导的另一途径是破坏PYGO与组蛋白H3的相互作用(图9A)。值得注意的是,已有研究表明,小分子能够与PYGO的PHD结构域结合,该结构域可与甲基化的组蛋白H3残基结合,从而破坏β-连环蛋白/Bcl9的相互作用。通过分子对接计算和打分排序,最终筛选出318个小分子作为该复合物的潜在PPI抑制剂。图9B展示了一个代表性配体的实例,该配体可介导多个亲水性相互作用、与Phe366形成p-π堆积以及形成氢键。
图9. A) BCL9/PYGO/组蛋白3的相互作用界面;B) 结合到H3K4me2关键氨基酸上的代表性分子结构。
 您的购物车当前为空
您的购物车当前为空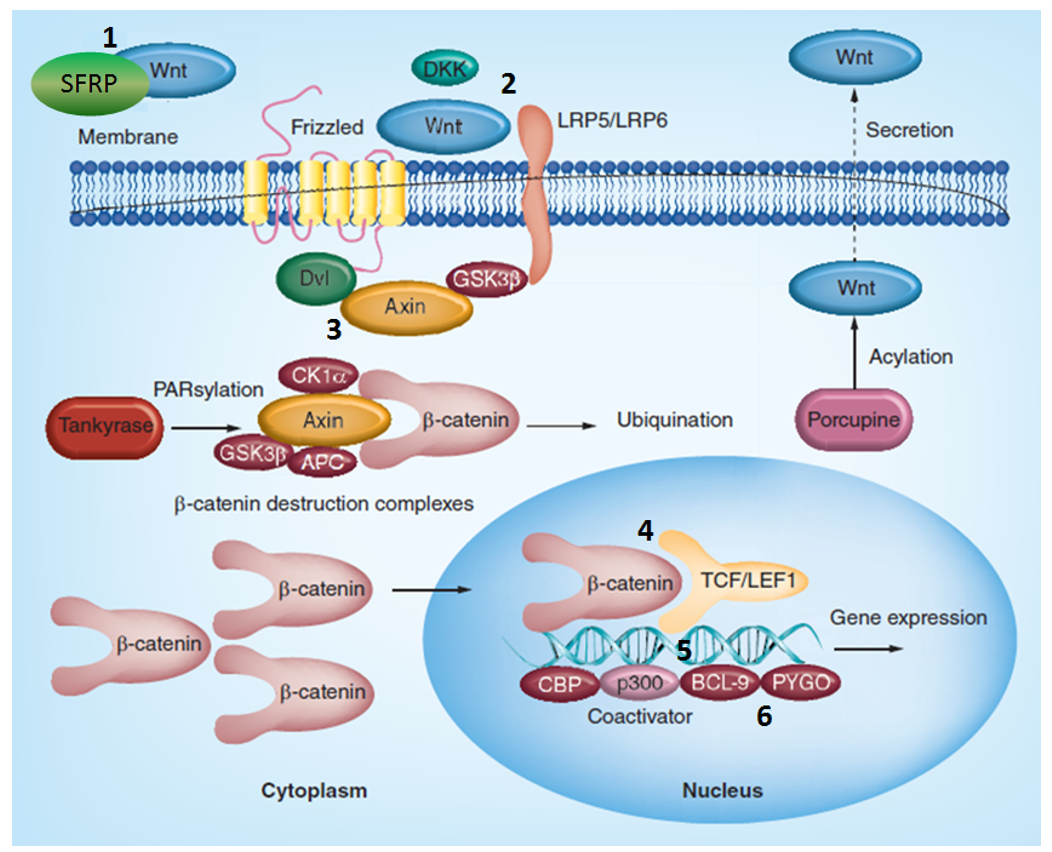



 很棒
很棒


 |
|