 您的购物车当前为空
您的购物车当前为空
【TargetMol 明星分子】- Sulfasalazine: 多重信号通路调控与铁死亡研究的关键工具
背景介绍:
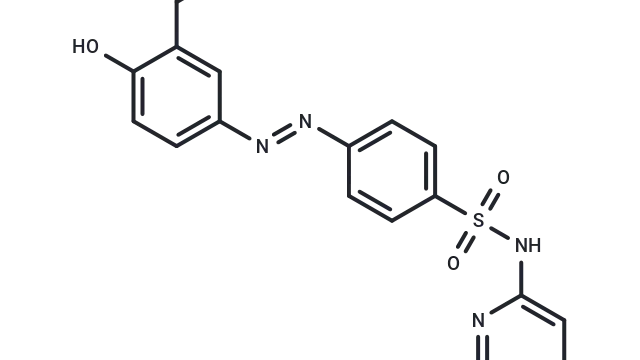
Sulfasalazine(T0907),CAS: 599-79-1,是一种合成的水杨酸衍生物,作为前药设计,具有对弹性蛋白含量丰富的结缔组织的亲和力。
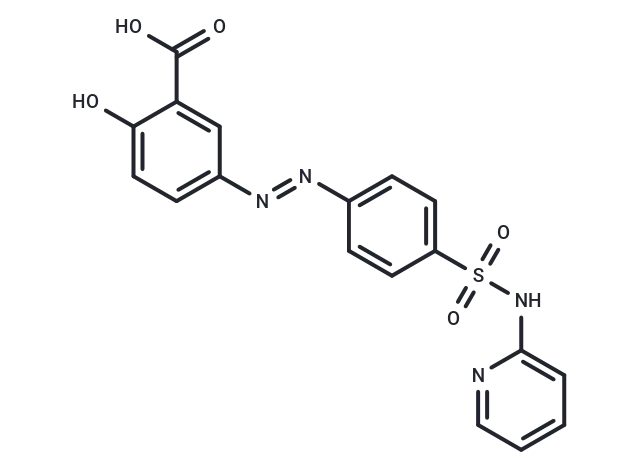
Sulfasalazine分子结构式
其作用机制多样,主要表现为诱导铁死亡(ferroptosis),这是一种依赖铁的调控性细胞死亡形式,同时抑制关键的信号分子如NF-κB、TGF-β和COX-2。这些分子靶点使Sulfasalazine处于多个重要生物通路的交汇点,包括细胞凋亡、自噬、炎症信号传导及铁死亡。通过抑制NF-κB这一调控炎症和免疫反应的核心转录因子,Sulfasalazine调节下游涉及细胞存活和炎症的基因表达。同时,抑制TGF-β信号通路影响细胞增殖及细胞外基质重塑,而COX-2的抑制则减少促炎性前列腺素的合成。Sulfasalazine诱导铁死亡的能力进一步使其区别于传统的凋亡或坏死,通过促进铁依赖的脂质过氧化导致细胞死亡。这种对炎症和细胞死亡通路的双重调控,凸显了Sulfasalazine在解析复杂生物过程中的研究价值。
在科研领域,Sulfasalazine常被用作工具化合物,研究自噬、凋亡与铁死亡之间的相互作用,尤其是在炎症和肿瘤生物学模型中。其对COX-2和NF-κB通路的抑制作用也使其成为研究炎症信号级联反应及其调控机制的重要工具。此外,Sulfasalazine诱导铁死亡的特性引起了对铁代谢和氧化应激机制的关注,适用于多种细胞类型的研究。Sulfasalazine独特的作用谱使研究者能够动态调节多个相互关联的信号通路,有助于阐明细胞死亡、免疫反应及组织重塑的分子机制。因此,Sulfasalazine作为一种多功能的生化探针,在揭示炎症、细胞存活及调控性细胞死亡模式的相互作用方面具有重要的实验研究价值。[1,2]
文献分享:
2.1 MYCN mediates TFRC-dependent ferroptosis and reveals vulnerabilities in neuroblastoma

Sulfasalazine (T0907) 通过诱导铁死亡增强MYCN扩增的神经母细胞瘤细胞对铁死亡的敏感性。该药物的作用部分依赖于铁转运受体基因TFRC的上调,进而促进细胞内铁的积累。实验结果显示,在MYCN过表达的细胞中敲低TFRC会显著提高细胞对Sulfasalazine的抗性,说明TFRC对于药物的作用至关重要。此外,Sulfasalazine在MYCN扩增细胞中能够诱导约70%的细胞死亡,而敲低System Xc(−)的相关组分仅引起约25%的细胞死亡,表明Sulfasalazine作用存在较大非特异性效应。
研究还发现,TFRC的缺失能够抑制MYCN介导的铁死亡并降低细胞内游离铁水平,而TFRC的过表达则模拟MYCN扩增效应,促进细胞内铁积累并提高对铁死亡的敏感性。这些结果说明,Sulfasalazine通过调控TFRC表达水平,增强细胞铁代谢,从而增强MYCN扩增神经母细胞瘤细胞对铁死亡的易感性。[3]

Sulfasalazine诱导的铁死亡由TFRC介导
2.2 Sulfasalazine, an inhibitor of the cystine-glutamate antiporter, reduces DNA damage repair and enhances radiosensitivity in murine B16F10 melanoma

Sulfasalazine (T0907) 是一种抑制 xCT 半胱氨酸-谷氨酸反向转运蛋白 的化合物。在B16F10黑色素瘤细胞中,它能够增加细胞氧化应激水平。研究显示,Sulfasalazine显著降低了黑色素瘤细胞内的谷胱甘肽含量,谷胱甘肽的减少导致细胞内活性氧(ROS)水平升高,并增强了过氧化氢的毒性作用,而对正常小鼠胚胎成纤维细胞几乎没有影响。
此外,Sulfasalazine能够增强X射线对黑色素瘤细胞的杀伤效果。它通过抑制DNA损伤修复并延长照射后的细胞周期停滞,从而提高辐射敏感性。在体内黑色素瘤移植模型中,Sulfasalazine同样降低了肿瘤内的谷胱甘肽水平,使肿瘤对放射治疗更加敏感。
总体而言,Sulfasalazine通过降低谷胱甘肽、增加氧化应激、抑制DNA修复及延长细胞周期停滞,显著增强了黑色素瘤细胞对放射的敏感性,同时在所测试条件下对正常细胞几乎无影响,为肿瘤放疗提供了潜在辅助策略。[4]
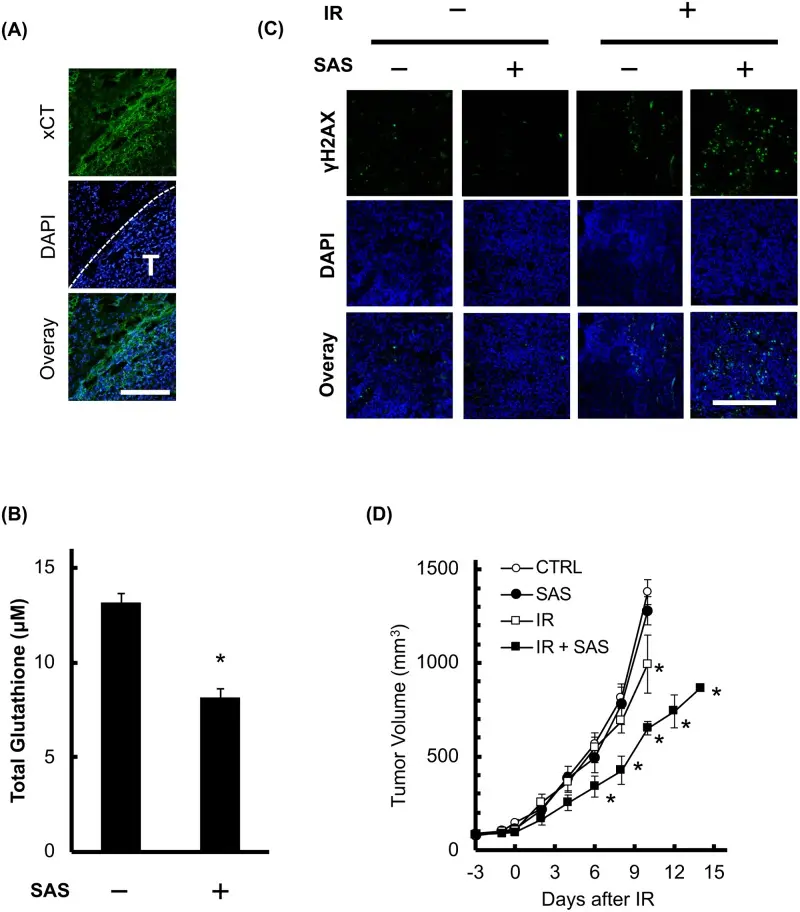
Sulfasalazine可增强移植的B16F10肿瘤对放射线的敏感性
2.3 Sulfasalazine impacts on ferroptotic cell death and alleviates the tumor microenvironment and glioma-induced brain edema

Sulfasalazine (T0907) 抑制谷氨酸转运体xCT并诱导胶质瘤细胞的铁死亡,但对自噬通量无影响。本研究中,低于200 µM浓度的Sulfasalazine对胶质瘤细胞的存活率无明显影响,且在胶质瘤植入脑切片中未诱导显著的肿瘤细胞死亡。而高浓度时,Sulfasalazine表现出胶质瘤毒性作用。Sulfasalazine与替莫唑胺联合使用时,在人胶质瘤细胞系U251中显示出显著的细胞死亡叠加效应,但在大鼠胶质瘤细胞中未见明显叠加效应。
体内实验中,Sulfasalazine显著减轻了胶质瘤相关的周围脑水肿,T2加权MRI显示水肿区体积显著减小。同时,Sulfasalazine处理组动物的神经功能缺损发作时间稍有延迟。综上所述,本研究结果表明Sulfasalazine能够缓解肿瘤相关脑水肿,但对胶质瘤的直接细胞毒性作用有限。[5]
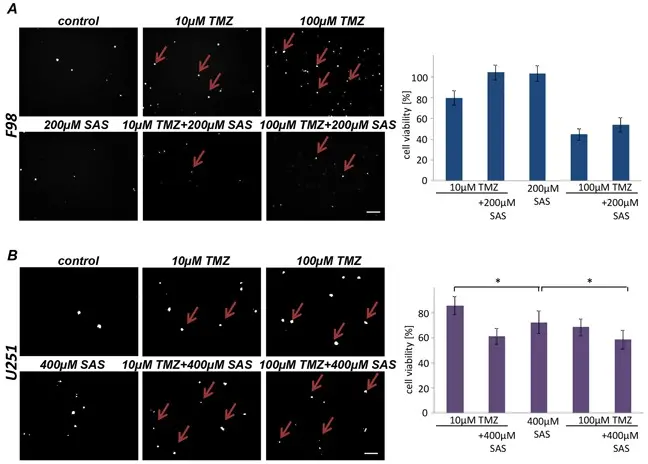
Sulfasalazine与 Temozolomide联合使用的效果
2.4 GPX4-dependent ferroptosis sensitivity is a fitness trade-off for cell enlargement

本研究探讨了Sulfasalazine (T0907) 对不同大小细胞铁死亡敏感性的影响。结果显示,Sulfasalazine通过抑制胞膜上的半胱氨酸-谷氨酸反向转运系统Xc- 来诱导铁死亡。研究特别指出,Sulfasalazine诱导铁死亡的敏感性与细胞大小无关,表明该药物对铁死亡的作用不受细胞体积变化的影响。与其他表现出细胞大小依赖性的铁死亡诱导剂不同,Sulfasalazine在不同细胞大小条件下均维持了稳定的一致性效果。本研究的实验数据明确表明,Sulfasalazine诱导的铁死亡机制与细胞大小无显著关联,其作用效果在本研究所分析的细胞模型中未因细胞体积的变化而有所改变。[6]
结语:
Sulfasalazine主要通过抑制半胱氨酸-谷氨酸反向转运系统Xc-诱导铁死亡,同时抑制NF-κB、TGF-β和COX-2等关键信号通路。文献显示,Sulfasalazine通过TFRC介导的铁摄取增强MYCN扩增神经母细胞瘤细胞的铁死亡敏感性,降低黑色素瘤细胞谷胱甘肽含量并抑制DNA修复,从而提高放射敏感性,同时缓解胶质瘤相关脑水肿但对胶质瘤细胞直接毒性有限。此外,Sulfasalazine诱导铁死亡的效应与细胞大小无关。这些研究成果凸显了Sulfasalazine在调控细胞死亡、炎症反应及肿瘤微环境中的独特作用。未来研究可聚焦其联合癌症治疗的潜力,探讨其在铁代谢和氧化应激中的作用机制,以及其System Xc(−)抑制以外的非特异性效应。
Q&A
Q1: Sulfasalazine诱导细胞死亡的主要机制是什么?
A1: Sulfasalazine主要通过抑制半胱氨酸-谷氨酸反向转运系统x_C^-,诱导铁依赖性的脂质过氧化而引发铁死亡。
Q2: Sulfasalazine如何影响MYCN扩增的神经母细胞瘤细胞?
A2: Sulfasalazine通过上调铁转运受体基因TFRC,促进细胞内铁积累,增强MYCN扩增神经母细胞瘤细胞对铁死亡的敏感性。
Q3: Sulfasalazine诱导铁死亡的效应是否依赖于细胞大小?
A3: 不依赖,研究显示Sulfasalazine在不同大小的细胞中均能稳定诱导铁死亡,其效应与细胞体积无显著关联。
参考文献
[1] Dixon SJ, Lemberg KM, Lamprecht MR, et al. Ferroptosis: An iron-dependent form of nonapoptotic cell death. Cell. 2012;149(5):1060-1072.
[2] Kaplan MJ. Role of NF-κB in inflammation and immunity: Implications for therapeutic targeting. J Clin Invest. 2013;123(7):2733-2735.
[3] Lu Y, Yang Q, Su Y, Ji Y, Li G, Yang X, et al.. MYCN mediates TFRC-dependent ferroptosis and reveals vulnerabilities in neuroblastoma. Cell Death & Disease. 2021;12(6):.
[4] Nagane M, Kanai E, Shibata Y, Shimizu T, Yoshioka C, Maruo T, et al.. Sulfasalazine, an inhibitor of the cystine-glutamate antiporter, reduces DNA damage repair and enhances radiosensitivity in murine B16F10 melanoma. PLOS ONE. 2018;13(4):e0195151.
[5] Sehm T, Fan Z, Ghoochani A, Rauh M, Engelhorn T, Minakaki G, et al.. Sulfasalazine impacts on ferroptotic cell death and alleviates the tumor microenvironment and glioma-induced brain edema. Oncotarget. 2016;7(24):36021-36033.
[6] Chan K, Yu Y, Kong Y, Cheng L, Yao R, Yin Chair P, et al.. GPX4-dependent ferroptosis sensitivity is a fitness trade-off for cell enlargement. iScience. 2025;28(5):112363.





 |
|