 您的购物车当前为空
您的购物车当前为空
【TargetMol 明星分子】- Metformin hydrochloride: 激活AMPK,调控代谢与细胞命运的多功能利器
背景介绍:
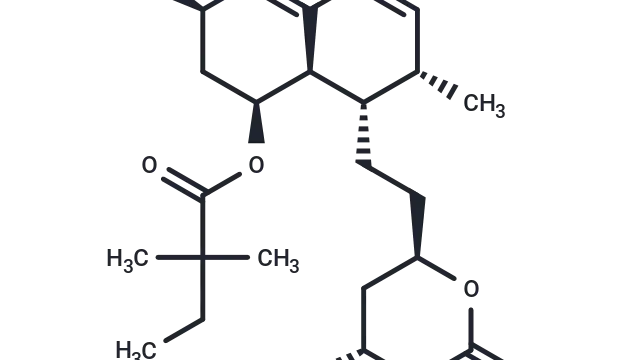
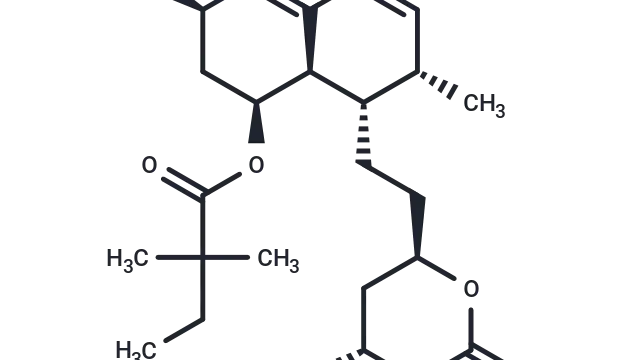
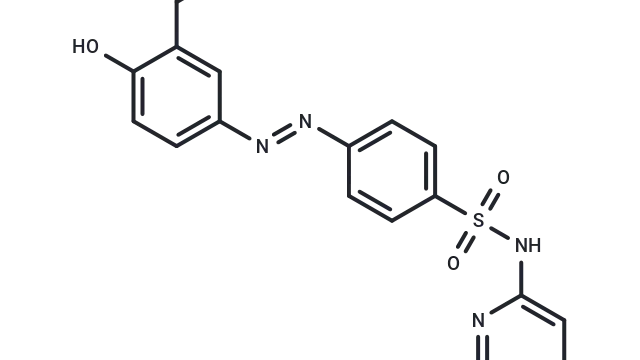
Metformin hydrochloride(T0740),CAS: 1115-70-4,是一种公认的AMPK激活剂,具有穿透血脑屏障的能力,使其在代谢和神经生物学研究中具有重要价值。
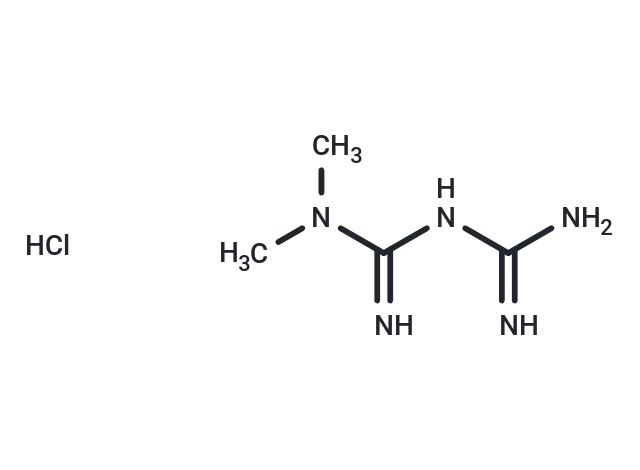
Metformin hydrochloride分子结构式
其主要作用机制是激活AMPK,作为细胞内能量的核心感应器,AMPK通过促进分解代谢途径和抑制合成代谢过程,调控细胞代谢稳态。Metformin hydrochloride通过激活AMPK,调节下游关键信号通路,包括抑制mTOR(机械靶标雷帕霉素)通路,mTOR是细胞生长、增殖及自噬的关键调控因子。该调控促进自噬和线粒体自噬(mitophagy)的启动,这些过程对于细胞稳态至关重要,通过降解受损的细胞器和蛋白质,维持线粒体质量控制,防止在代谢应激条件下细胞凋亡的发生。
在血糖调节方面,Metformin hydrochloride通过AMPK依赖性途径增强胰岛素敏感性并减少肠道葡萄糖吸收。其穿透血脑屏障的特性使其在神经退行性疾病研究中具有潜在应用价值,这些疾病通常伴随着自噬失调和线粒体功能障碍。通过促进线粒体自噬,Metformin hydrochloride支持线粒体的更新换代,这对于神经元的存活和功能维护至关重要。此外,该化合物通过AMPK激活和mTOR抑制调节细胞凋亡路径,为研究细胞应激反应和存活机制提供了分子基础。
Metformin hydrochloride在研究中的应用广泛,涵盖代谢疾病、衰老、肿瘤生物学及神经退行性疾病等领域。其调控AMPK及其下游信号通路的能力,使其成为解析能量代谢、自噬及细胞命运决策相互作用的多功能工具。特别是其对线粒体自噬的促进作用,使其成为研究线粒体动力学和质量控制机制的重要化合物。该化合物通过激活AMPK、抑制mTOR、诱导自噬和线粒体自噬以及调节细胞凋亡,动态调控多个相互关联的信号通路,为细胞适应代谢应激和维持稳态提供了综合性的研究平台。
综上所述,Metformin hydrochloride(T0740)作为探究AMPK-mTOR-自噬轴及其在细胞代谢和存活中的作用的关键生化工具,其多重调控能量感应、线粒体质量控制及细胞死亡路径的能力,彰显了其在代谢调控和神经生物学等多领域研究中的重要应用价值。[1,2]
文献分享:
2.1 Pretreatment with metformin protects mice from whole-body irradiation

Metformin hydrochloride (T0740) 在本研究中显示出保护作用,在全身照射前后给予该药能提高小鼠的存活率。该药物具有自由基清除活性,能够直接清除自由基或通过刺激抗氧化酶的活性发挥作用。Metformin hydrochloride (T0740) 还能够降低活性氧(ROS)的产生,并通过激活AMP激酶刺激DNA损伤反应。该药物显著减少了辐射所致的DNA损伤和ROS水平,表现为降低NADPH氧化酶4(NOX4)表达,并提高超氧化物歧化酶、过氧化氢酶和谷胱甘肽过氧化物酶等抗氧化酶的活性,特别是在小鼠造血干细胞中。
此外,在人淋巴细胞中,Metformin hydrochloride (T0740) 减少了放射线照射后诱导的细胞凋亡,表现为降低BAX与Bcl-2的比率。这些结果表明,Metformin hydrochloride (T0740) 能够增强细胞抵御辐射引起的氧化损伤和细胞凋亡,从而在实验模型中发挥辐射保护作用。[3]
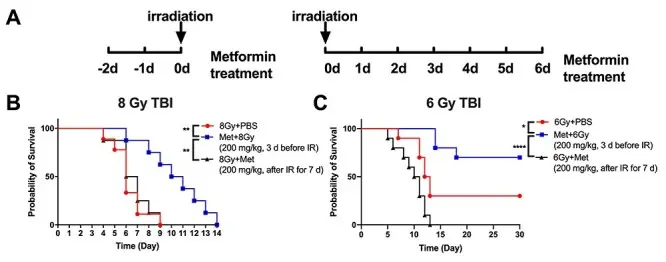
Metformin hydrochloride对TBI后小鼠存活率的影响
2.2 Metformin transiently inhibits colorectal cancer cell proliferation as a result of either AMPK activation or increased ROS production
Metformin hydrochloride (T0740) 在本研究中通过诱导细胞周期停滞于G0/G1期,暂时性抑制了结直肠癌细胞的增殖,且伴随着c-Myc表达显著下降和IGF1R蛋白下调。Metformin hydrochloride的抗增殖作用机制涉及AMPK的激活及活性氧(ROS)生成的增加,从而抑制了mTOR通路及其下游靶点S6和4EBP1的活性。此外,该药物降低了结直肠癌干细胞标志物CD44和LGR5的RNA表达,提示其对具有干细胞特性的肿瘤细胞产生影响。Metformin hydrochloride还通过减少细胞迁移和侵袭能力,抑制了肿瘤细胞的运动能力。
实验结果显示,该药物的细胞静止效应在停药后可逆,表现为mTOR通路和IGF1R蛋白的重新活化以及细胞形成克隆能力的恢复。研究未发现Metformin hydrochloride诱导细胞凋亡、自噬或衰老,但观察到了线粒体去极化和ROS释放,且该现象在HCT116及其p53缺失细胞株中更为明显。综上,本研究显示Metformin hydrochloride在结直肠癌细胞中发挥了暂时性的抑制作用,影响细胞增殖和迁移,但未导致细胞死亡。[4]
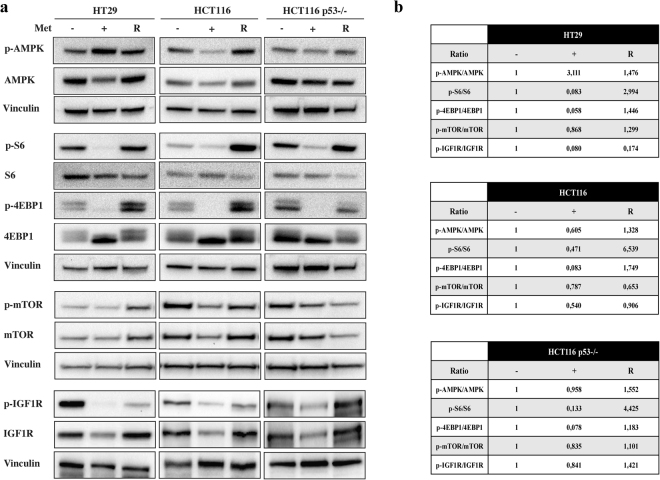
Metformin hydrochloride可逆性地抑制mTOR通路和IGF1R蛋白
2.3 Metformin potentiates nephrotoxicity by promoting NETosis in response to renal ferroptosis

Metformin hydrochloride (T0740) 在小鼠急性肾损伤(AKI)模型中表现出加剧肾损伤和提高死亡率的作用,即使低剂量亦然。研究显示,Metformin hydrochloride处理后,肾实质细胞死亡和中性粒细胞数量显著增加。研究确定Metformin hydrochloride诱导肾实质细胞的铁死亡(ferroptosis),这一凋亡机制促进了中性粒细胞通过CXCR4受体迁移至损伤位置,该受体与Metformin hydrochloride-铁-NGAL复合物结合,进而诱导NETosis,加重AKI。阻断铁死亡或耗竭中性粒细胞均能有效缓解Metformin hydrochloride引发的肾毒性。
此外,通过降低铁含量对肾损伤具有保护作用,表明铁在Metformin hydrochloride诱导的AKI中起重要作用。本文结果表明,Metformin hydrochloride通过促进ferroptosis和NETosis机制,增强了肾脏毒性反应。[5]
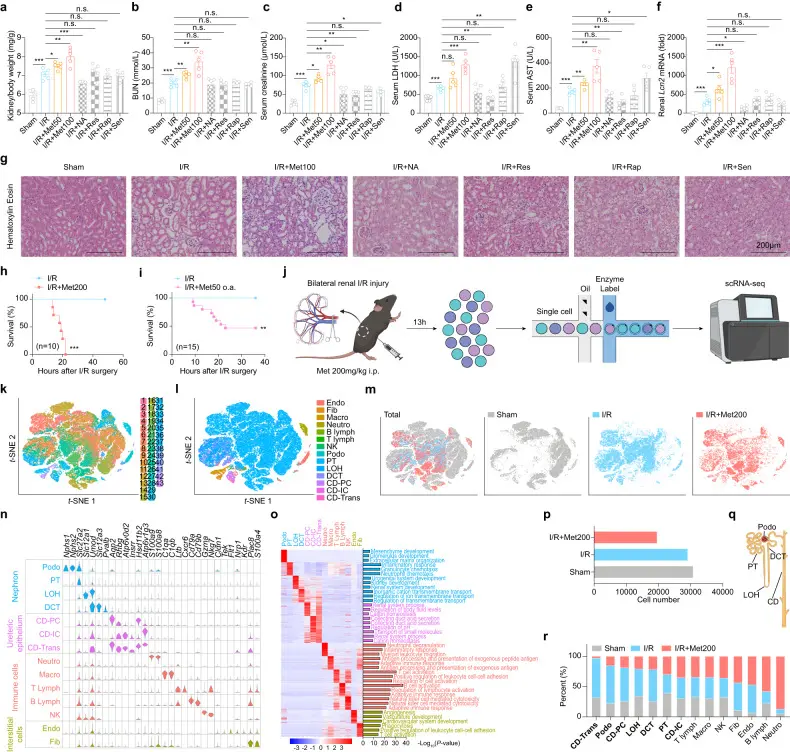
Metformin hydrochloride在小鼠模型中以剂量依赖性方式加重急性肾损伤
结语:
Metformin hydrochloride的主要作用机制是激活AMPK,调节细胞能量稳态,促进分解代谢并抑制合成代谢。通过AMPK激活,该化合物抑制mTOR通路,促进自噬和线粒体自噬,从而维持线粒体质量控制,防止代谢应激下的细胞凋亡。文献显示其能保护小鼠免受辐射引起的氧化损伤和细胞凋亡,暂时抑制结直肠癌细胞增殖,并通过诱导铁死亡和NETosis加剧肾毒性。未来研究可聚焦于优化该药物的治疗窗口,发挥其代谢和神经保护作用,同时减少肾毒性等不良反应,并深入探讨其在线粒体动力学及细胞命运调控中的作用。
Q&A
Q1: Metformin hydrochloride调控细胞代谢的主要机制是什么?
A1: Metformin hydrochloride通过激活AMPK,促进分解代谢路径并抑制合成代谢,调节细胞能量稳态,并通过抑制mTOR通路发挥下游调控作用。
Q2: 研究中Metformin hydrochloride对结直肠癌细胞有哪些影响?
A2: 它通过诱导细胞周期停滞于G0/G1期,降低c-Myc和IGF1R表达,增加ROS生成,抑制mTOR通路,暂时性抑制癌细胞增殖,但未诱导细胞凋亡、自噬或衰老。
Q3: Metformin hydrochloride在肾损伤模型中表现出什么不良作用?
A3: 它通过促进肾实质细胞铁死亡和诱导中性粒细胞NETosis,加剧急性肾损伤并提高死亡率,表现出肾毒性增强作用。
参考文献
[1] Zhou G, Myers R, Li Y, et al. Role of AMP-activated protein kinase in mechanism of metformin action. J Clin Invest. 2001;108(8):1167-1174.
[2] Kim J, Kundu M, Viollet B, Guan KL. AMPK and mTOR regulate autophagy through direct phosphorylation of Ulk1. Nat Cell Biol. 2011;13(2):132-141.
[3] Da F, Guo J, Yao L, Gao Q, Jiao S, Miao X, et al.. Pretreatment with metformin protects mice from whole-body irradiation. Journal of Radiation Research. 2021;62(4):618-625.
[4] Mogavero A, Maiorana M, Zanutto S, Varinelli L, Bozzi F, Belfiore A, et al.. Metformin transiently inhibits colorectal cancer cell proliferation as a result of either AMPK activation or increased ROS production. Scientific Reports. 2017;7(1):.
[5] Cai Z, Wu X, Song Z, Sun S, Su Y, Wang T, et al.. Metformin potentiates nephrotoxicity by promoting NETosis in response to renal ferroptosis. Cell Discovery. 2023;9(1):.





 |
|