基因毒性化疗药物,如顺铂,可通过DNA损伤应答(DDR)干扰DNA复制和细胞分裂,引发肿瘤细胞死亡。然而,患者易对化疗药物产生耐药性,因此我们需要更好地了解患者对基因毒性化疗敏感性的生物学基础,以助于为患者提供更有效的治疗策略。
近年来,越来越多的研究揭示了氨基酸在肿瘤生长和治疗敏感性方面的重要影响,将氨基酸代谢作为治疗靶点也逐渐获得认可,展现了显著改善癌症治疗效果的巨大潜力。
2023 年 10 月 26 日,中山大学潘超云团队在 Cell Metabolism 上发表题为: Tyrosine catabolism enhances genotoxic chemotherapy by suppressing translesion DNA synthesis in epithelial ovarian cancer 的研究性论文,首次发现 酪氨酸分解代谢可显著增强化疗效果,并揭示了酪氨酸代谢产物富马酸在跨损伤 DNA 合成(TLS)调控中的独特作用,或可通过简单的膳食补充酪氨酸改善化疗效果。
▲点击图片可跳转原文
在最新研究中,为了了解氨基酸代谢对基因毒性化疗药物的影响,研究人员在上皮性卵巢癌(EOC)细胞系 SKOV3 中进行了 RNAi 筛选。结果发现,酪氨酸分解代谢途径中的基因(FAH、HGD 和 GSTZ1)是抑制 DNA 损伤最有效的靶点。
进一步的实验表明,富马酸乙酰乙酸水解酶 (FAH) 的敲除在多种基因毒性药物处理的 EOC 细胞系中特异性地降低了 gH2AX 水平(磷酸化的γ-组蛋白H2AX,可用于评估DNA损伤程度),FAH 的敲低减轻了这些化疗药物引起的 DNA 损伤并减少了细胞毒性、降低了各种癌细胞系对顺铂治疗的敏感性。提示 FAH 表达降低可能与基因毒性化疗耐药特异性相关。
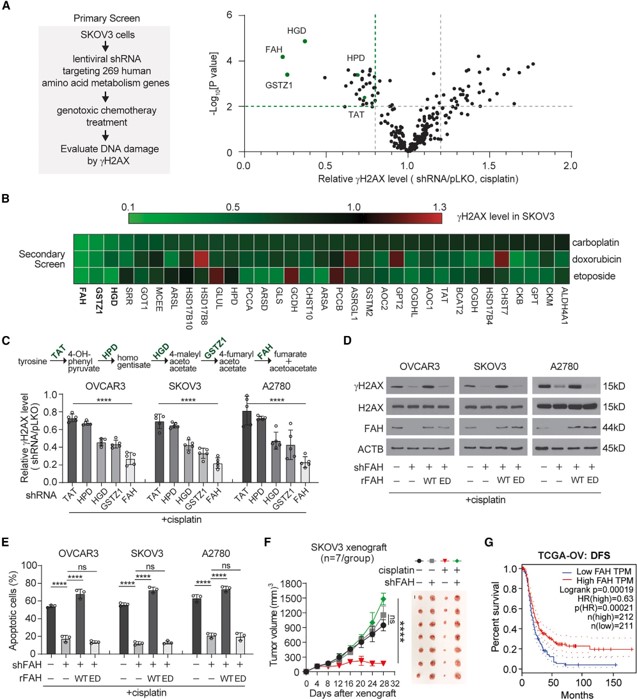
▲酪氨酸分解途径与 EOC 对基因毒性化疗的反应相关
接下来,研究人员评估了 FAH 表达与 EOC 患者临床治疗结果的相关性。他们对来自 57 名卵巢癌患者肿瘤组织中衍生的原发性 EOC 细胞进行了定量,然后再用基因毒性化疗药物 顺铂(cisplatin)或 依托泊苷(etoposide)处理后监测了细胞凋亡情况。
结果显示,在接受基因毒性药物治疗的 EOC 细胞中,FAH 表达与细胞凋亡率呈显著正相关。同时,对接受新辅助化疗(NACT)的 36 名 EOC 患者肿瘤中 FAH 表达的免疫组织化学分析显示,与对 NACT 有更有利反应的患者相比,肿瘤中 FAH 水平显著更高,表明肿瘤中 更高水平的 FAH 表达与 EOC 患者基因毒性化疗取得更好的治疗结果相关。
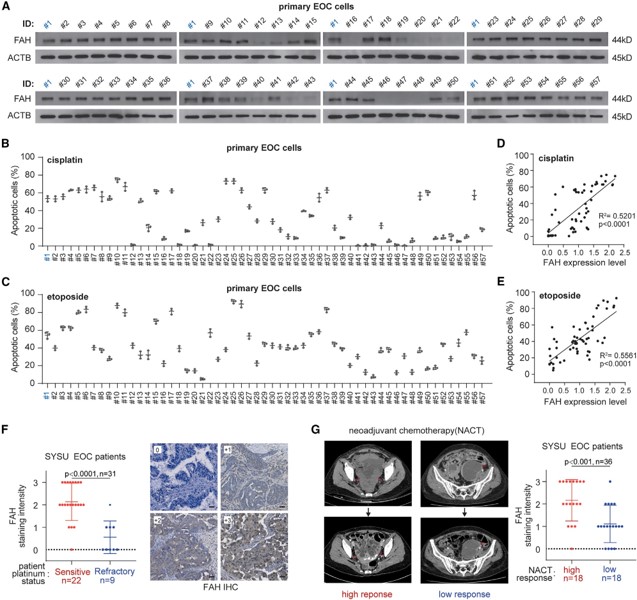
▲高FAH表达与卵巢上皮癌对基因毒性化疗的更好反应相关
此外,研究人员发现虽然 FAH 敲除不影响顺铂或依托泊苷的靶标作用,但在基因毒性药物处理的 EOC 细胞中,它可以显著降低 DNA 损伤,特别是双链断裂(DSBs)。
为了确定 FAH 影响 DSB 的形成机制,研究人员进行了 DNA 损伤修复和 DNA 损伤容忍两方面的实验,发现在 FAH 缺失的 EOC 细胞中,使用 TLS 抑制剂治疗导致复制叉显著减速,几乎完全消除了 FAH 敲除造成的不良影响。同样,在基因毒性药物处理的 EOC 细胞中,FAH 的下调显著降低了 gH2AX 水平并减少了细胞凋亡,而与 TLS 抑制剂共同处理则显著恢复了 gH2AX 水平和细胞凋亡。这些数据表明,FAH 可作为 TLS 抑制因子,在 EOC 细胞中赋予化疗敏感性。
而这种抑制效果是通过酪氨酸降解的代谢产物富马酸(fumarate)实现的。
在基因毒性化疗药物的使用下,肿瘤细胞内活性氧水平升高,导致 FAH M308 位点发生甲硫氨酸残基氧化而大量入核,细胞核内的 FAH 被募集到染色质上并产生富马酸,富马酸直接结合到 REV1 R516 位点,破坏 REV1 与 REV7 相互作用,导致 TLS 受到抑制。(PS: REV1(DNA repair protein REV1)和 REV7(DNA repair protein REV7)参与调控 TLS)
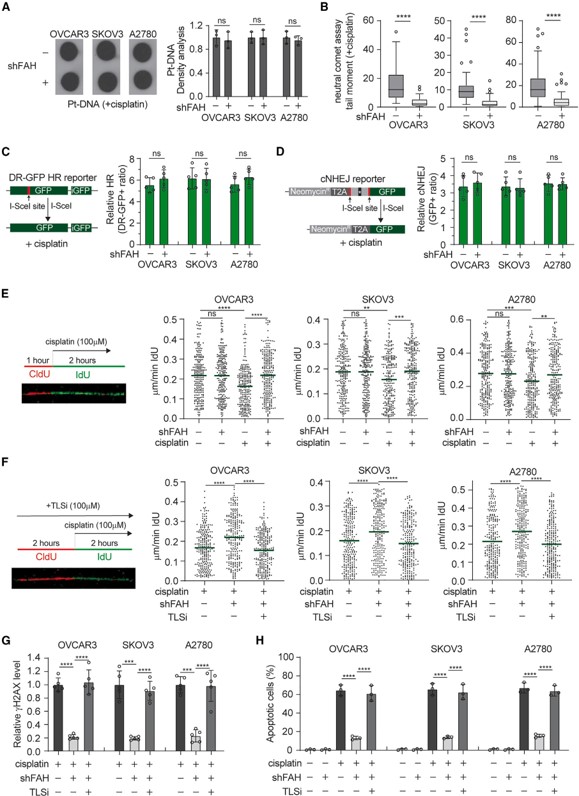
▲FAH抑制基因毒性药物处理的EOC细胞的TLS
研究人员还深入探讨了酪氨酸补充是否能够改善体内的化疗效果。通过选择不同 FAH 表达水平的患者的肿瘤组织进行移植,发现在未经治疗的肿瘤中,FAH 水平似乎不影响生长。然而,在顺铂治疗下,低 FAH 表达的肿瘤表现出显著的耐药性,而体内的酪氨酸补充可显著抑制肿瘤的耐药性,并提高血清酪氨酸水平。
通过在同种异体卵巢癌小鼠模型中复制卵巢癌的完整化疗过程,研究评估了酪氨酸补充的治疗效益。结果显示,与酪氨酸补充结合的治疗方案显著抑制了肿瘤的生长,延长了响应时间,阻止了肿瘤复发,并提高了小鼠的生存率。这些发现表明,膳食酪氨酸补充可能是一种有前途的干预策略,可提高卵巢上皮癌基因毒性癌症治疗的有效性。
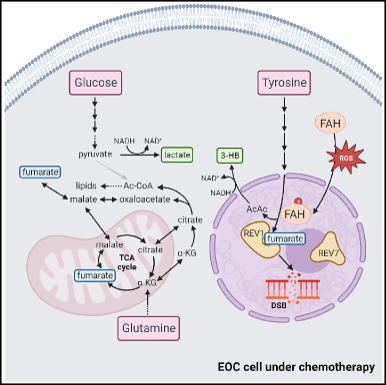
▲研究简介图
小结
综上,该研究深入探讨了氨基酸代谢作为抗肿瘤治疗靶点的潜力,并揭示了其在基因毒性化疗中的影响机制。研究发现,在卵巢上皮癌(EOC)中,酪氨酸降解的最后一步酶,富马酸乙酰乙酸水解酶 (FAH) 的缺失会导致化疗敏感性下降。机制上,基因毒性化疗条件下,FAH 通过酪氨酸降解产生的富马酸结合 REV1,抑制了跨损伤 DNA 合成(TLS),提高了化疗的敏感性。此外,通过膳食补充酪氨酸可改善对基因毒性化疗药物的敏感性,并减少治疗抵抗的发生。研究结果揭示了酪氨酸代谢的富马酸在 TLS 调控中的独特作用,并为通过膳食酪氨酸补充提高基因毒性化疗效果提供了新的途径。
陶术生物拥有 800+ 化合物库,其中有一些是致力于抗肿瘤研究的,例如 抗癌细胞代谢库、谷氨酰胺代谢化合物库、表观遗传库、核苷类化合物库 等,欢迎私信咨询~
参考文献:
Li J, Zheng C, Mai Q, et al. Tyrosine catabolism enhances genotoxic chemotherapy by suppressing translesion DNA synthesis in epithelial ovarian cancer. Cell Metab. 2023;35(11):2044-2059.e8. doi:10.1016/j.cmet.2023.10.002
